Clear Sky Science · pt
A lactilação de histonas aumenta a expressão de CXCL1 para infiltração de neutrófilos e escape imune no câncer de pâncreas
Por que este estudo sobre câncer é importante
O câncer de pâncreas está entre os mais letais, em parte porque frequentemente resiste às imunoterapias modernas que funcionam em outros tumores. Este estudo revela como tumores pancreáticos redesenham seu próprio metabolismo de glicose para desarmar silenciosamente o sistema imunológico, e como bloquear esse processo pode reabrir um caminho para as defesas do corpo — e para medicamentos já existentes — combaterem a doença.
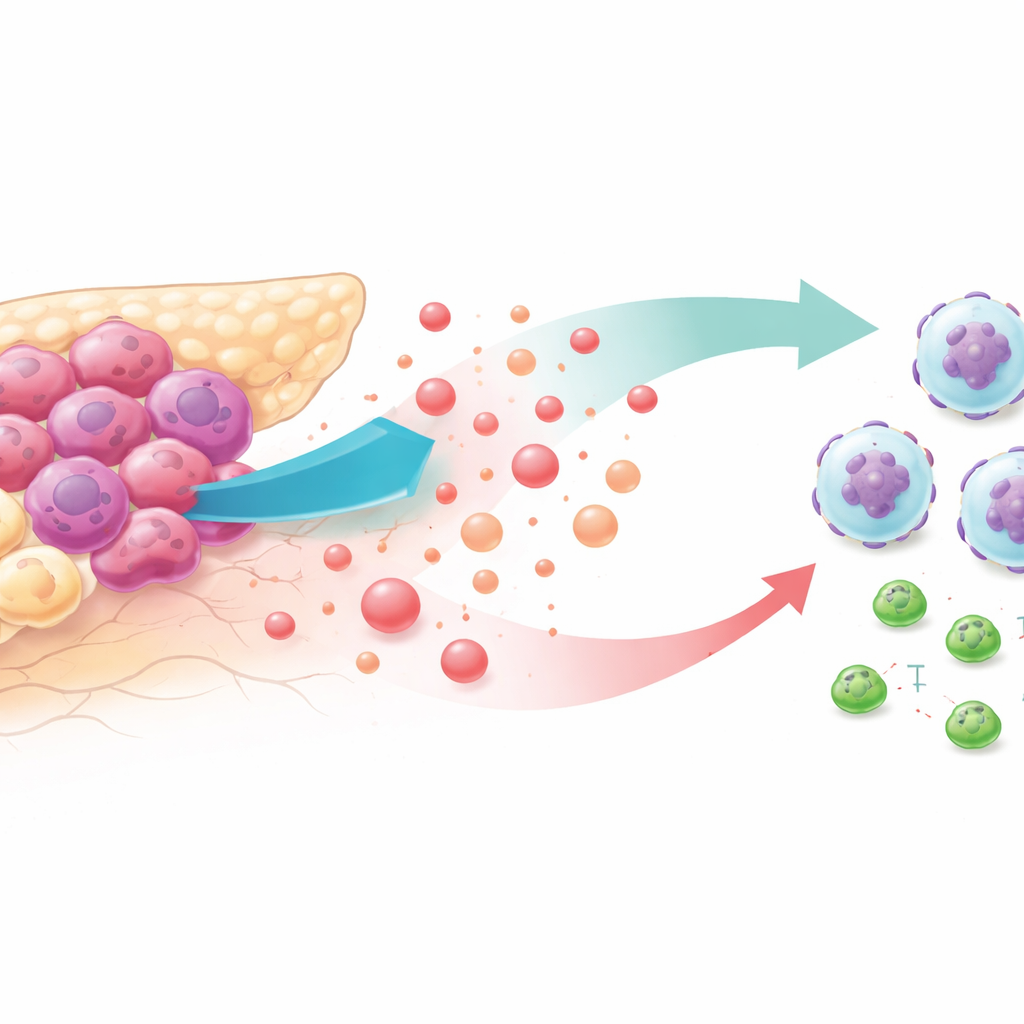
Tumores famintos por açúcar e um entorno hostil
Células cancerosas são notórias por queimar glicose em alta velocidade, mesmo quando há oxigênio disponível. Esse estilo de vida de “glicólise alta” inunda o microambiente tumoral com lactato, um subproduto antes descartado como resíduo metabólico. Ao analisar bancos de dados de tumores de pacientes e modelos de camundongo, os pesquisadores descobriram que cânceres pancreáticos com glicólise mais intensa estavam repletos de neutrófilos — glóbulos brancos que, nesse contexto, ajudam o tumor a crescer — e apresentavam menos células T CD8 citotóxicas. Pacientes cujos tumores exibiam esse perfil tendiam a ter sobrevida menor, sugerindo que metabolismo alterado e escape imune estão fortemente ligados.
Como os tumores usam o lactato para atrair a ajuda errada
Para entender como a glicólise atrai neutrófilos, a equipe reduziu a glicólise tumoral com drogas ou artifícios genéticos em linhagens de câncer pancreático e em camundongos. Quando a quebra do açúcar foi bloqueada, as células tumorais liberaram muito menos de um sinal químico chamado CXCL1, e os níveis circulantes desse sinal caíram em camundongos e em amostras de pacientes. Em testes de migração in vitro, neutrófilos moveram-se com entusiasmo em direção ao meio proveniente de células cancerosas altamente glicolíticas, mas não em direção ao meio de células com glicólise bloqueada — a menos que os pesquisadores adicionassem CXCL1 purificado de volta. Em camundongos vivos, restaurar CXCL1 em tumores com glicólise reduzida trouxe os neutrófilos de volta e enfraqueceu o efeito anti-tumoral da inibição da glicólise.
Um novo interruptor epigenético impulsionado pelo lactato
O estudo então aprofundou até o nível do empacotamento do DNA. Nossos genes estão enrolados em torno de proteínas semelhantes a carretéis chamadas histonas, cujas marcas químicas atuam como interruptores liga/desliga da atividade gênica. Os autores mostram que, no câncer de pâncreas, o lactato produzido pela glicólise adiciona uma marca específica de “lactil” em uma posição da histona conhecida como H3K18. Essa modificação, denominada lactilação da histona H3K18, estava marcadamente mais elevada nos tecidos tumorais do que no pâncreas normal. Quando a glicólise foi bloqueada, a lactilação em H3K18 diminuiu, especialmente perto da região de controle do gene CXCL1, e a produção de CXCL1 caiu. A adição de lactato restaurou tanto a marca na histona quanto a expressão de CXCL1. Em amostras de pacientes, tumores com mais lactilação em H3K18 também mostraram níveis maiores de CXCL1, ligando essa marca molecular a um panorama imune pró-tumoral.
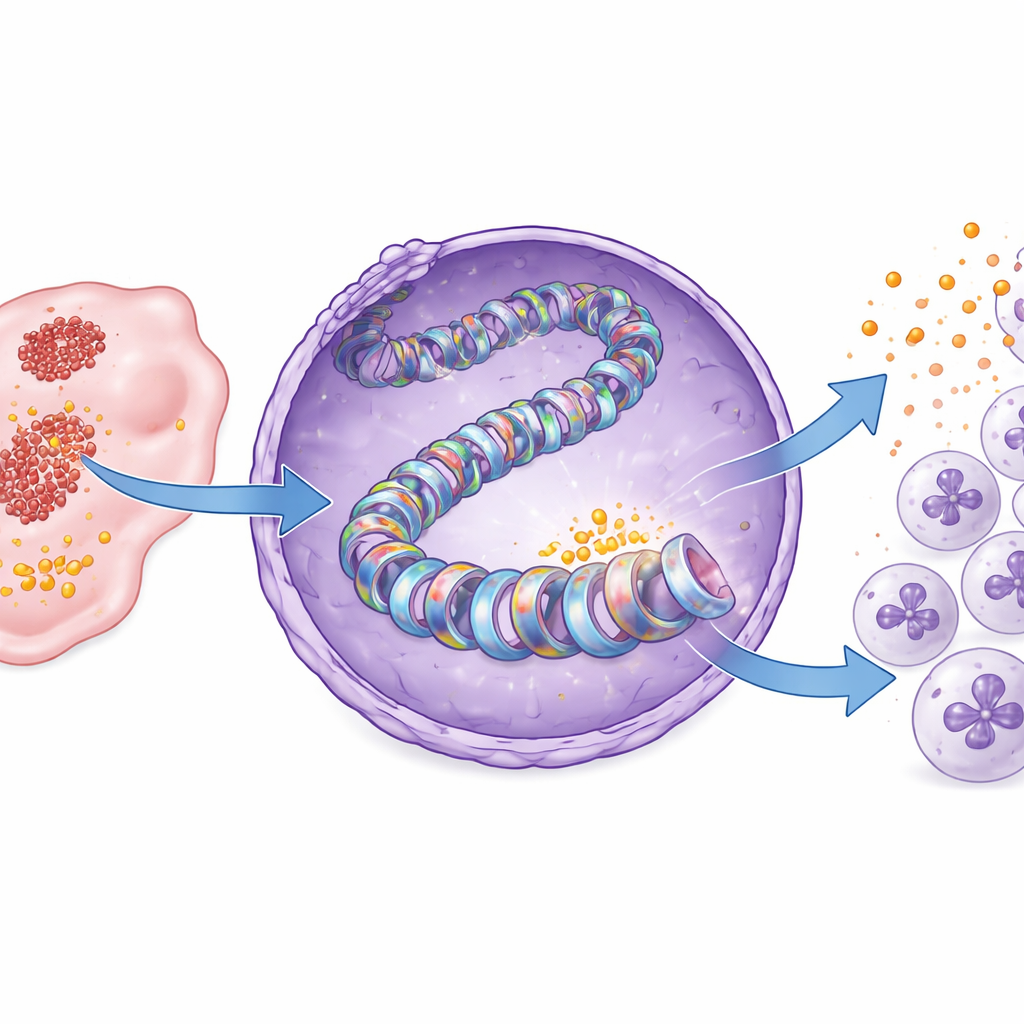
Identificando a enzima e uma vulnerabilidade passível de drogas
Marcas em histonas são escritas por enzimas especializadas. Ao rastrear inibidores de proteínas conhecidas por modificar histonas, os pesquisadores identificaram uma chamada PCAF como escritora chave da marca H3K18 lactilada no câncer de pâncreas. Modelagens estruturais sugeriram que a PCAF pode ligar-se à lactil-CoA, a forma ativada do lactato usada para a marcação, e ensaios bioquímicos confirmaram que a PCAF purificada pode adicionar diretamente grupos lactil à histona H3. Bloquear a PCAF com uma pequena molécula, a bromosporina, reduziu a lactilação em H3K18 e a produção de CXCL1 em células cancerosas e em tumores de camundongo. Como resultado, menos neutrófilos infiltraram os tumores, mais células T CD8 se acumularam e o crescimento tumoral desacelerou, tudo sem perda de peso óbvia ou toxicidade nos animais.
Tornando um tumor “frio” mais quente com terapia combinada
Como drogas padrão que bloqueiam pontos de verificação imunológicos, como anticorpos anti–PD-1, têm mostrado sucesso limitado no câncer de pâncreas, a equipe testou se desmontar a via lactato–PCAF–CXCL1 poderia tornar esses tumores mais responsivos. Em modelos de camundongo subcutâneos e ortotópicos pancreáticos, a combinação de bromosporina com terapia anti–PD-1 encolheu tumores mais do que cada tratamento isoladamente, reduziu a infiltração de neutrófilos, aumentou as células T CD8 ativas e prolongou significativamente a sobrevida. Isso sugere que cortar a “sirene” metabólica do tumor para neutrófilos ajuda a transformar um tumor imunologicamente “frio” em um mais “quente”, que a terapia de checkpoint consegue engajar melhor.
O que isso significa para tratamentos futuros
Em termos simples, o estudo revela uma reação em cadeia: tumores pancreáticos queimam açúcar, liberam lactato, usam esse lactato para acionar um interruptor epigenético nas proteínas de empacotamento do DNA, aumentam CXCL1 e, assim, convocam neutrófilos que os ajudam a se esconder de células T assassinas. Interromper essa cadeia no passo da PCAF com um fármaco não apenas desacelera os tumores, mas também torna a imunoterapia existente mais potente em camundongos. Embora sejam necessários mais estudos para garantir segurança e encontrar a melhor forma de atacar essa via em pessoas, esses achados destacam uma estratégia promissora: reprogramar o metabolismo e os interruptores gênicos do tumor para dar ao sistema imunológico uma chance justa.
Citação: Zhang, P., Ma, J., Wan, Y. et al. Histone lactylation increases CXCL1 expression for neutrophil infiltration and immune escape in pancreatic cancer. Nat Commun 17, 2526 (2026). https://doi.org/10.1038/s41467-026-69311-5
Palavras-chave: câncer de pâncreas, metabolismo tumoral, lactilação de histonas, microambiente tumoral, imunoterapia contra o câncer