Clear Sky Science · pt
Adgrg6/Gpr126 é necessário para a integridade da parede compacta e para estabelecer a identidade trabecular durante a trabeculação cardíaca
Por que a arquitetura da parede cardíaca importa
Cada batida do coração depende de uma parede interna finamente esculpida. Em embriões em desenvolvimento, essa parede se forma inicialmente como uma camada lisa e depois gera uma floresta de cristas musculares chamadas trabéculas, que ajudam o coração a bombear com eficiência. Quando esse processo falha, crianças e adultos podem desenvolver cardiomiopatias graves. Este estudo investiga como um receptor pouco conhecido, Gpr126, ajuda as células cardíacas a decidir se permanecem na parede compacta lisa ou se tornam parte dessas cristas internas.
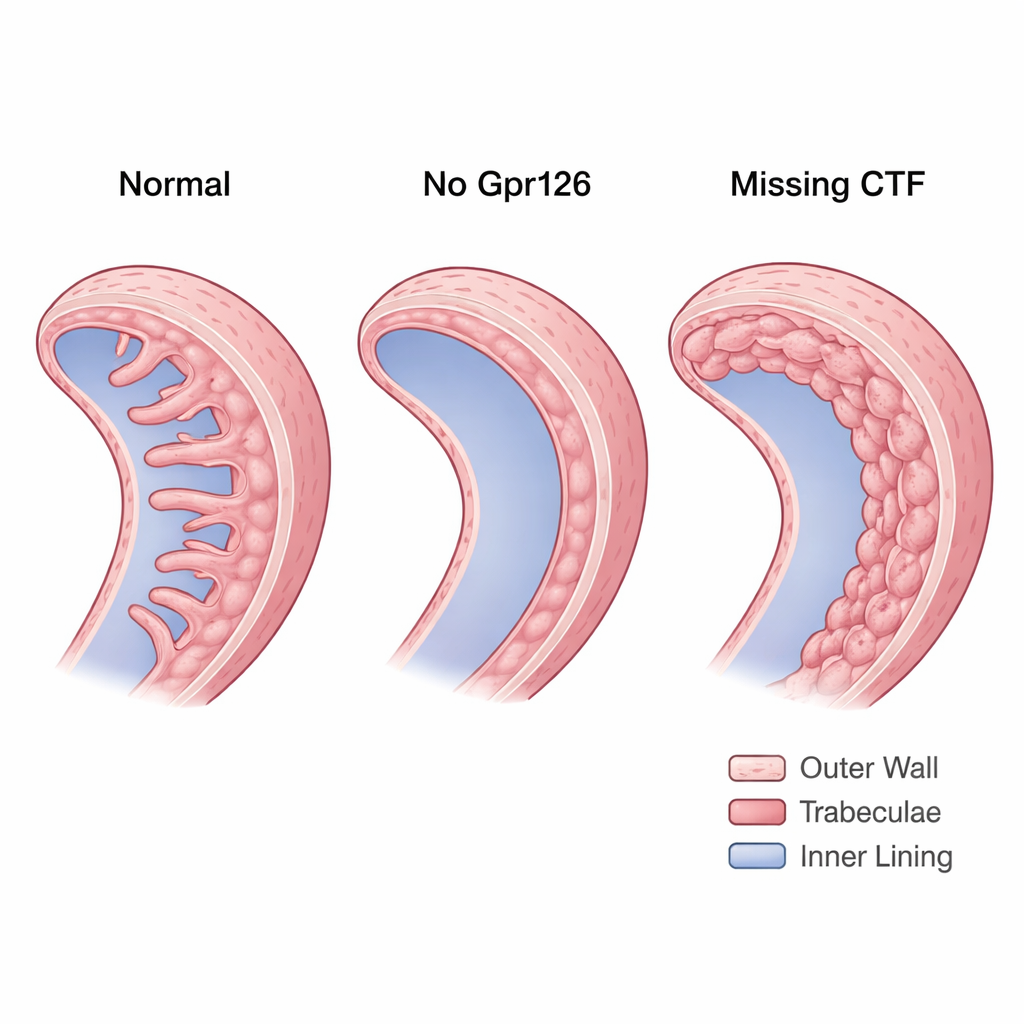
Um receptor com função dupla no coração
Gpr126 pertence a uma família de receptores acoplados à proteína G do tipo adesão que se situam na membrana celular e percebem o ambiente ao redor da célula. Esses receptores são particularmente interessantes porque muitos fármacos existentes já têm como alvo receptores relacionados, o que os torna candidatos terapêuticos atraentes. Gpr126 é incomum por ser naturalmente cortado em duas partes principais: um fragmento N-terminal (NTF), que fica voltado para fora da célula e pode ajudar na adesão célula–célula, e um fragmento C-terminal (CTF), que atravessa a membrana e desencadeia sinalização interna. Trabalhos prévios associaram Gpr126 ao desenvolvimento cardíaco, mas não estava claro o que cada fragmento faz durante a formação das trabéculas.
Usando o peixe-zebra para ver o coração tomando forma
Os pesquisadores usaram o peixe-zebra, cujos embriões transparentes permitem imagens em tempo real do coração batendo. Eles estudaram duas variantes genéticas de gpr126. Uma (stl47) produz apenas uma proteína minúscula e severamente truncada; a outra (st49) produz um NTF secretado e estável que carece da parte de sinalização CTF. Ao combinar esses mutantes com linhagens relatórias fluorescentes, a equipe pôde visualizar células cardíacas individuais, acompanhar a formação das trabéculas e monitorar moléculas-chave como N-caderina (que ajuda as células a aderirem) e Notch (uma via de sinalização que informa às células que identidade adotar).
Manter a parede unida versus formar as cristas
Os mutantes stl47, que essencialmente carecem de ambos os fragmentos funcionais, mostraram que Gpr126 é necessário para formar trabéculas normais. Em embriões materno-zygoticos stl47 — onde nenhum Gpr126 funcional vem de qualquer dos progenitores — muitos corações se desenvolveram com trabéculas ausentes ou fortemente reduzidas. A N-caderina, que em corações saudáveis fica concentrada nas laterais dos cardiomiócitos da parede compacta, apareceu espalhada pela superfície celular. Essa desorganização sugeriu que, sem o NTF, a adesão célula–célula na parede compacta fica instável, minando a base sobre a qual as trabéculas deveriam se formar.
Muita parede, pouca identidade
Os mutantes st49, que ainda produzem o NTF mas carecem do CTF, mostraram o problema oposto. Em vez de trabéculas ausentes, seus corações formaram uma parede interna espessa e em várias camadas. As camadas extras não eram trabéculas verdadeiras: as células permaneceram polarizadas como células da parede compacta e não remodelaram seus contatos de N-caderina para o padrão pontuado típico das células que formam cristas. Usando um repórter de atividade de Notch, a equipe constatou que esses corações apresentavam sinalização Notch anormalmente alta no miocárdio. Notch alto é conhecido por manter as células na parede compacta e impedir que se deslaminem em trabéculas. Importante: quando os pesquisadores reintroduziram apenas o CTF em células endocárdicas, as trabéculas reapareceram e a atividade de Notch voltou aos níveis próximos do normal, mostrando que a sinalização via CTF é crucial para conferir identidade trabecular aos cardiomiócitos.
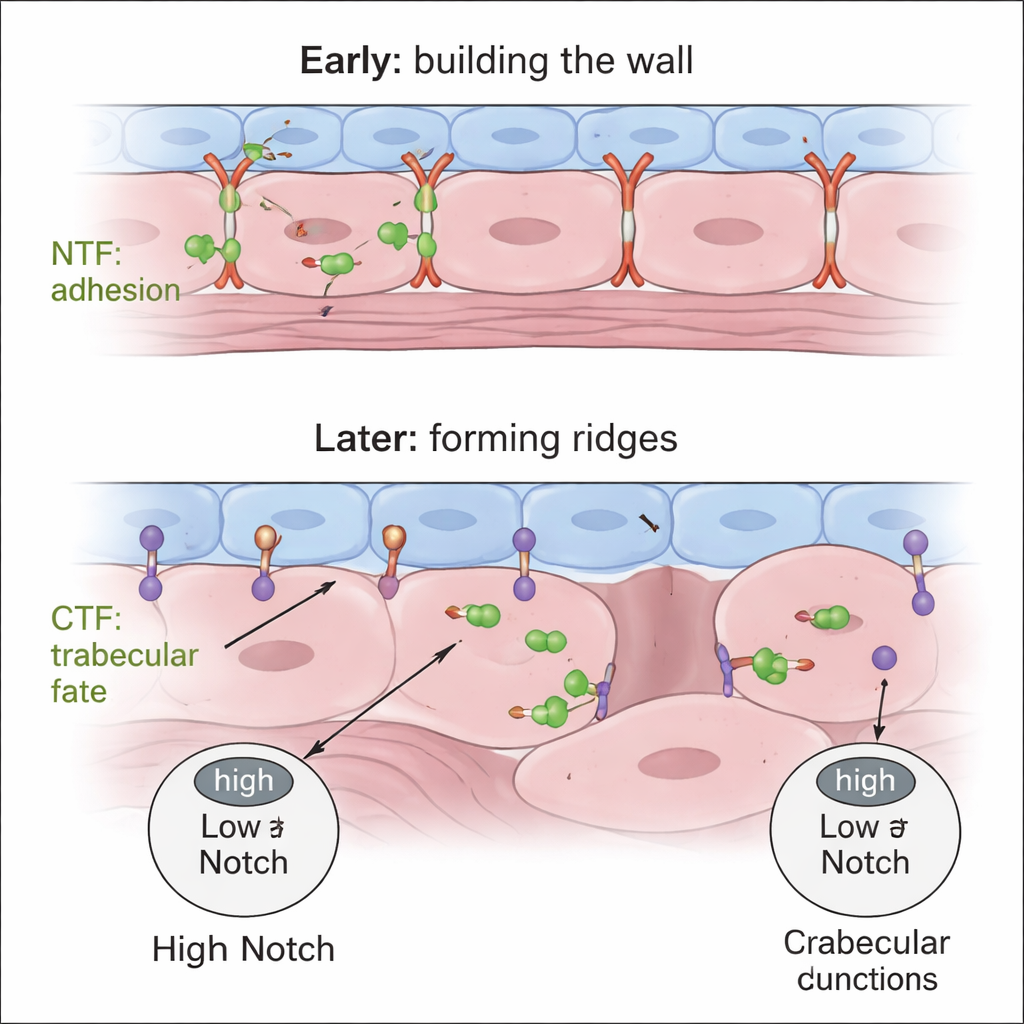
Equilibrando sinais para um coração saudável
Em conjunto, os achados apoiam um modelo em duas etapas e com duas partes. Primeiro, o NTF secretado de Gpr126 ajuda os cardiomiócitos da parede compacta a manterem junções apertadas e corretamente posicionadas, assegurando uma parede robusta de camada única. Depois, o CTF — atuando a partir de células endocárdicas — modula a sinalização Notch no miocárdio para que apenas alguns cardiomiócitos despolarizem, afrouxem suas junções e protraiam-se para formar trabéculas, enquanto suas células vizinhas permanecem na parede compacta. Se o NTF estiver ausente, a parede nunca se organiza corretamente; se o CTF estiver ausente, a parede cresce em excesso e as células não adotam a identidade trabecular. Esse controle específico por domínio da arquitetura da parede cardíaca ressalta Gpr126 como um possível elo entre adesão celular, vias de sinalização como Notch e doenças estruturais do coração, e sugere que ajustar diferentes partes do mesmo receptor poderá um dia ajudar a corrigir defeitos do desenvolvimento.
Citação: Srivastava, S., Gunawan, F., Vergarajauregui, S. et al. Adgrg6/Gpr126 is required for compact wall integrity and establishing trabecular identity during cardiac trabeculation. Nat Commun 17, 1484 (2026). https://doi.org/10.1038/s41467-026-69292-5
Palavras-chave: trabeculação cardíaca, Gpr126, desenvolvimento do coração, sinalização Notch, modelo de peixe-zebra