Clear Sky Science · pt
O condutor genético da encefalopatia necrótica aguda, RANBP2, regula a resposta inflamatória à infecção pelo vírus Influenza A
Quando a gripe prejudica o cérebro
A maioria das pessoas pensa na influenza como uma semana de febre, tosse e repouso. No entanto, em casos raros, especialmente em crianças, uma infecção rotineira por gripe pode, de repente, evoluir para um distúrbio cerebral potencialmente fatal chamado encefalopatia necrótica aguda (ANE). Famílias e médicos suspeitam há muito que fatores genéticos ajudam a determinar quem desenvolve essa complicação catastrófica. Este estudo revela como uma única proteína guardiã celular, RANBP2, normalmente mantém o vírus da gripe sob controle e impede que a resposta inflamatória do próprio corpo fuja do controle.
Uma complicação rara, porém devastadora da gripe
A ANE aparece de forma abrupta após uma doença febril, muitas vezes influenza, e pode causar rapidamente convulsões, coma e danos neurológicos permanentes. Aproximadamente metade dos episódios de ANE conhecidos no mundo está ligada ao vírus influenza A, particularmente à linhagem H1N1. Crianças que herdam certas alterações no gene RANBP2 enfrentam um risco muito maior, em uma condição conhecida como ANE1. Até agora, no entanto, os cientistas não entendiam o que essa proteína realmente faz durante a infecção pela gripe, nem por que sua alteração tornaria a inflamação no cérebro tão grave.
Portões celulares e genomas virais
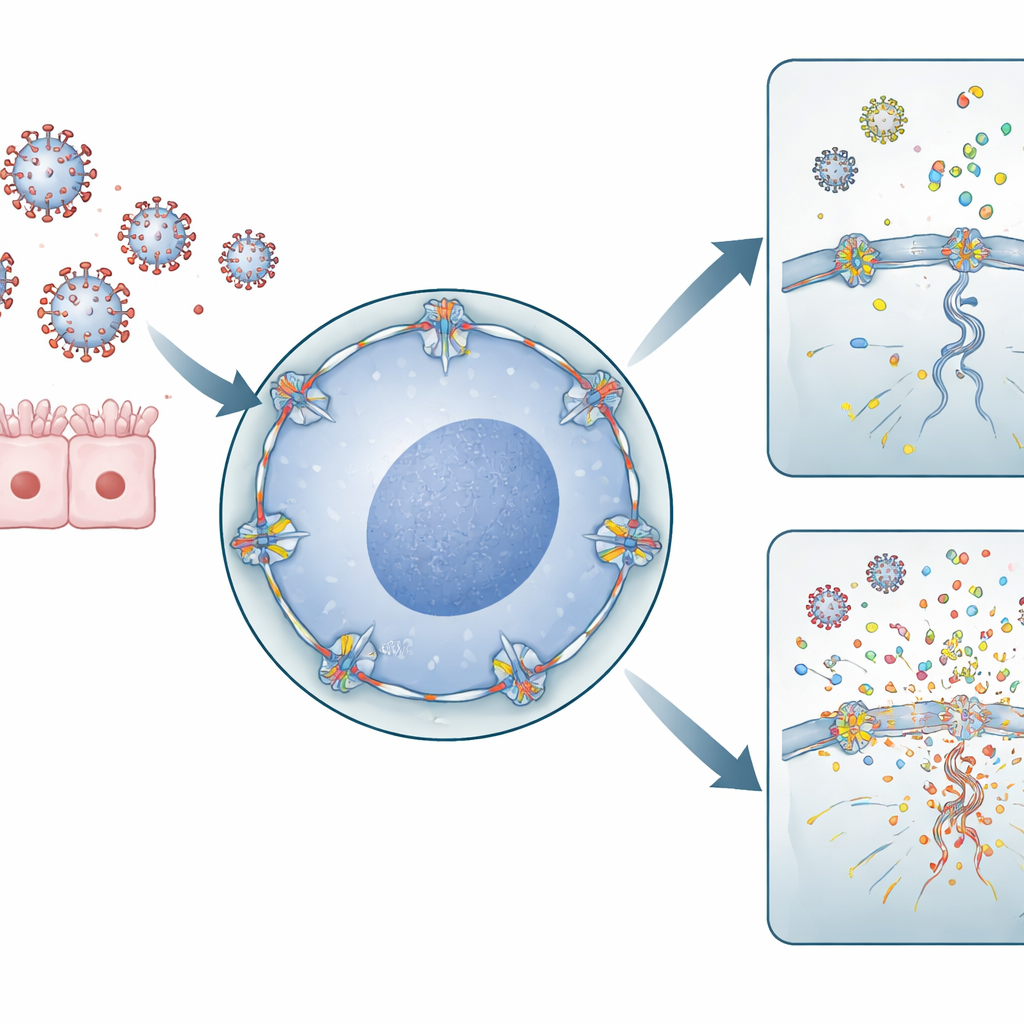
O vírus influenza A tem um modo de vida incomum para um vírus de RNA: precisa entrar no núcleo da célula para copiar seu material genético. Para isso, ele passa pelos poros nucleares — grandes portais no envelope nuclear que controlam o tráfego entre o núcleo e o citoplasma ao redor. RANBP2 é um componente importante no lado externo desses poros. Os autores usaram células derivadas de pulmão humano e células imunes para reduzir os níveis de RANBP2 ou introduzir a mutação associada à ANE. Eles descobriram que, quando RANBP2 estava ausente ou deslocado, os genomas da gripe eram copiados mais extensamente dentro do núcleo, e segmentos genéticos virais eram exportados para o citoplasma de forma desequilibrada. Surpreendentemente, esse excesso de RNA viral não gerou mais partículas virais infecciosas, mas alterou onde e como o material viral se acumulava dentro da célula.
Quando detritos virais alimentam o sistema de alarme
O sistema imunológico depende de sensores moleculares que detectam fragmentos errantes de RNA viral no citoplasma como sinais de perigo. A equipe mostrou que, em células sem RANBP2 normal, segmentos virais adicionais se acumulavam no citoplasma, criando exatamente os padrões que esses sensores reconhecem. Em células derivadas de pulmão, isso desencadeou níveis mais elevados de moléculas inflamatórias como IL‑6 e IL‑1β. Em macrófagos humanos primários — células imunes de primeira linha obtidas de doadores de sangue — a perda de RANBP2 levou a um aumento marcante de quimiocinas pró‑inflamatórias, incluindo CXCL8, CXCL10, CCL2, CCL3 e CCL4. Essas moléculas sinalizadoras recrutam e ativam células imunes adicionais, amplificando a reação geral à infecção.
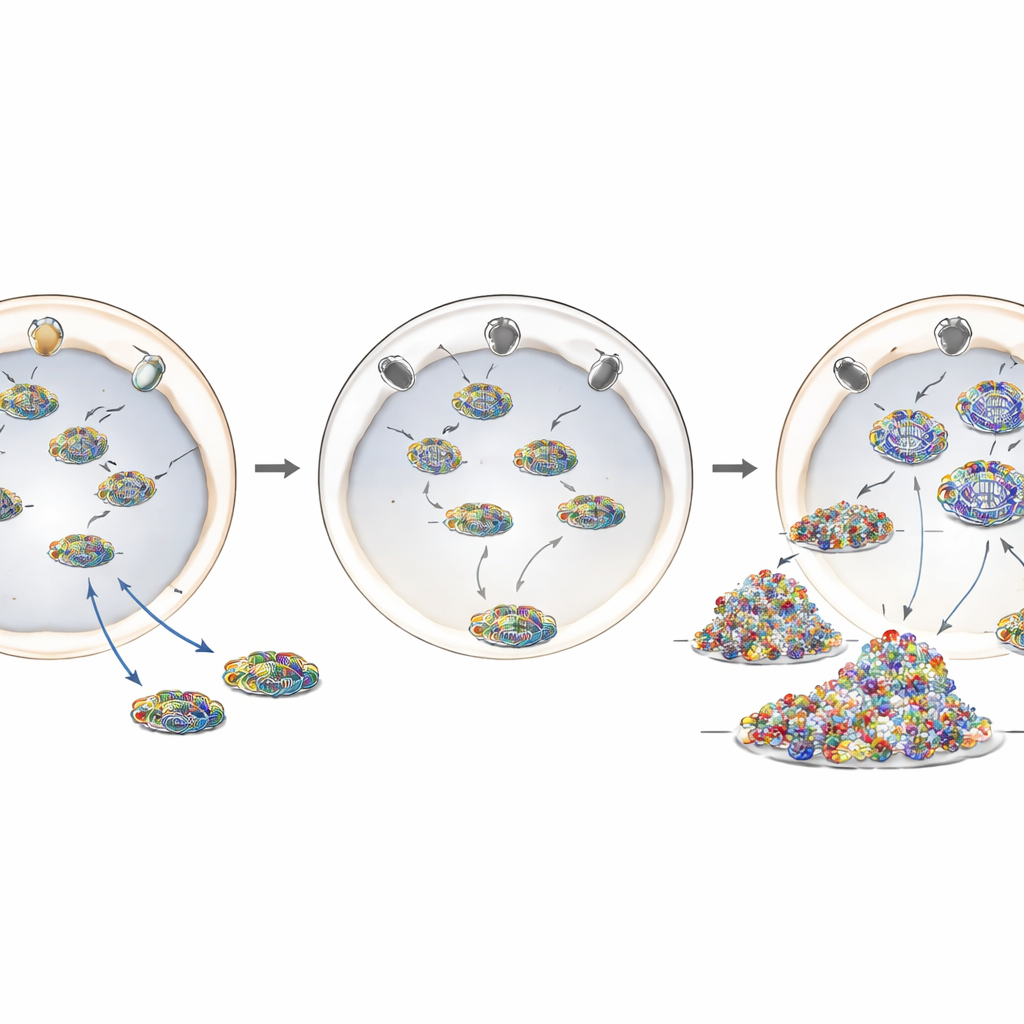
Uma mutação da doença que desloca um guardião
Para modelar mais de perto a ANE1, os pesquisadores usaram edição genômica CRISPR‑Cas9 para introduzir a alteração associada à doença mais comum, T585M, no gene humano RANBP2. Nessas células editadas, os níveis de proteína RANBP2 eram em grande parte normais, mas sua localização não: em vez de formar um contorno brilhante ao redor do envelope nuclear, grande parte da proteína foi deslocada para o interior da célula. Células portadoras dessa mutação, seja em uma ou em ambas as cópias do gene, comportaram‑se de maneira semelhante às células com deficiência de RANBP2. Elas apresentaram maior replicação do genoma da influenza, mostraram mais material viral no citoplasma e desencadearam uma resposta inflamatória mais intensa após a infecção. Isso sugere que posicionar corretamente o RANBP2 nos poros nucleares — em vez de sua abundância total — é crucial para seu papel protetor.
Por que isso importa para crianças em risco
Em conjunto, os achados pintam o RANBP2 como um guardião celular que ajusta finamente como o material genético da influenza se move para dentro e para fora do núcleo. Quando o RANBP2 está ausente ou mal localizado, o RNA viral é replicado em excesso e exportado de forma caótica, entupindo o citoplasma com detritos moleculares que intensificam muito a sinalização imune. Para a maioria dos tecidos, isso pode significar uma crise de gripe mais severa, porém sobrevivível. Em crianças vulneráveis com ANE1, contudo, essa inflamação descontrolada — especialmente se atingir o cérebro — pode ajudar a explicar os danos neurológicos súbitos e graves observados após infecções que, de outra forma, seriam rotineiras. Compreender essa via pode orientar estratégias futuras para identificar cedo pacientes em risco e para ajustar tratamentos anti‑inflamatórios antes que a resposta imune passe de protetora a destrutiva.
Citação: Desgraupes, S., Decorsière, A., Perrin, S. et al. The genetic driver of Acute Necrotizing Encephalopathy, RANBP2, regulates the inflammatory response to Influenza A virus infection. Nat Commun 17, 2427 (2026). https://doi.org/10.1038/s41467-026-69288-1
Palavras-chave: influenza, encefalopatia necrótica aguda, RANBP2, hiperinflação, poros nucleares