Clear Sky Science · pt
Montagem assimétrica de 4-alquil-butenolida catalisada por flavoenzima trifuncional na biossíntese de avenolida
Por que anéis pequenos em bactérias importam para nós
Muitos medicamentos que salvam vidas, desde agentes antiparasitários até protetores de culturas, dependem de um pequeno motivo químico chamado butenolida. Hoje esses anéis são em sua maioria produzidos a partir de matérias‑primas derivadas do petróleo em processos industriais multietapa que consomem energia e geram resíduos. Este estudo revela como bactérias do solo constroem um desses anéis, um hormônio chamado avenolida que liga a produção dos poderosos antiparasitários avermectinas. Entender essa rota natural aponta para formas mais limpas e baratas de fabricar compostos úteis e pode ajudar a abrir caminho para novos antibióticos.
O anel especial no coração de muitos fármacos
Butenolidas são anéis compactos de cinco membros que os químicos apreciam porque reagem de modos versáteis e aparecem em muitos produtos naturais e fármacos modernos. Elas contribuem para moléculas com atividades anticâncer, antifúngica, anti‑inflamatória e inseticida usadas na medicina e na agricultura. Ainda assim, rotas sintéticas tradicionais para esses anéis normalmente exigem várias etapas cuidadosamente controladas, catalisadores caros e insumos petroquímicos. Essa combinação eleva custos e impacto ambiental, levando pesquisadores a buscar atalhos biológicos que a natureza já aperfeiçoou.
Um hormônio bacteriano que ativa um fármaco blockbuster
No microrganismo do solo Streptomyces avermitilis, a molécula contendo butenolida avenolida atua como um hormônio minúsculo. Em concentrações extremamente baixas ela se liga a uma proteína reguladora e remove um freio molecular sobre os genes que produzem avermectinas, agentes potentes que paralisam vermes parasitas e alguns insetos. Trabalhos genéticos anteriores já sugeriam que duas enzimas, chamadas SavA e SavB, construíam a avenolida, mas as etapas reais eram desconhecidas. A equipe primeiro transferiu os genes relevantes para um parente mais cooperativo, Streptomyces albidoflavus, e otimizou as condições de cultivo até que a cepa modificada produzisse quantidades de miligramas de avenolida pura — suficiente para dissecar a via em detalhe. 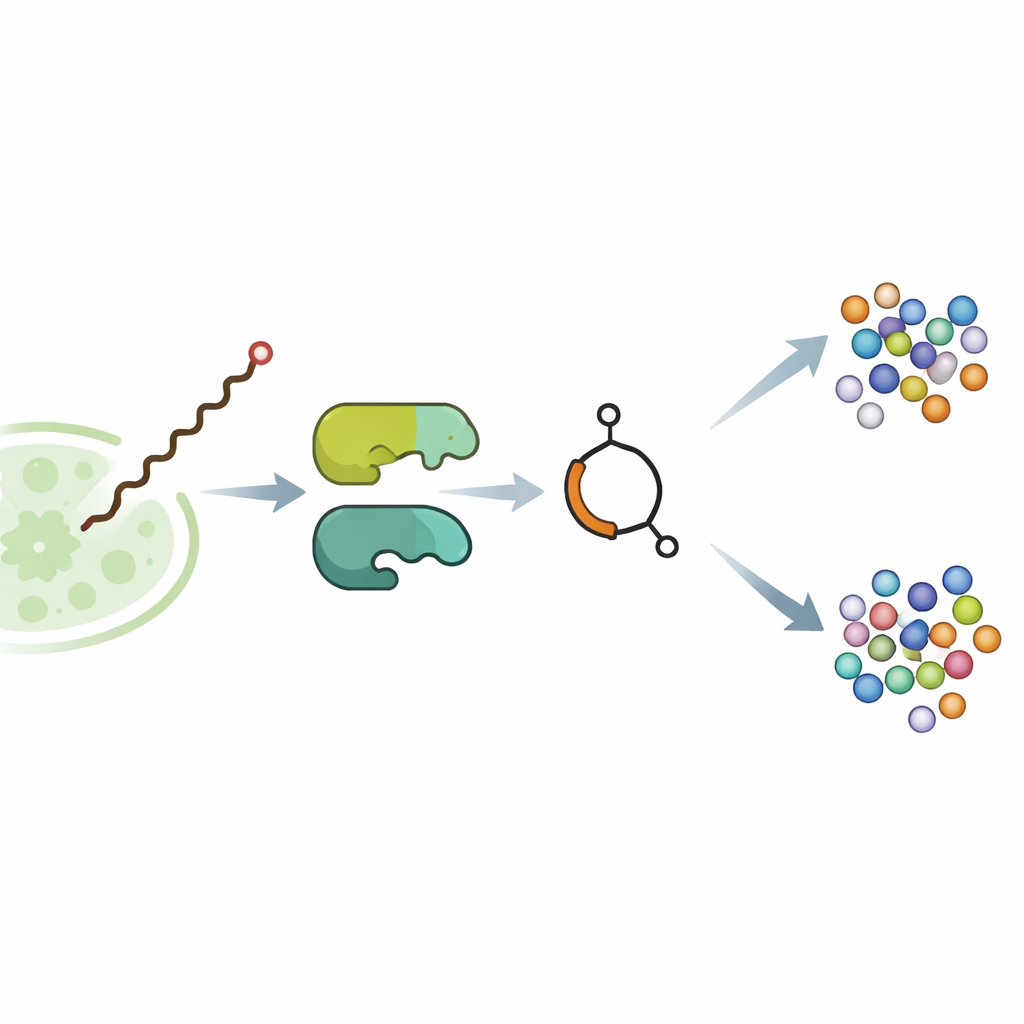
Uma única enzima que faz três trabalhos em sequência
A surpresa central do estudo é a SavA, uma enzima contendo flavina que realiza três transformações químicas distintas em um pedaço inicial parecido com ácido graxo extraído do metabolismo celular normal. Trabalhando em reações em tubo de ensaio com substratos miméticos cuidadosamente sintetizados, os pesquisadores mostraram que a SavA primeiro remove átomos de hidrogênio para introduzir uma dupla ligação, depois adiciona um grupo contendo oxigênio em uma posição específica e, finalmente, promove o fechamento da cadeia no anel butenolida. Experimentos isotópicos usando oxigênio gasoso enriquecido com uma forma mais pesada de oxigênio confirmaram que o oxigênio do anel vem diretamente do ar. Modelagem estrutural e mutações direcionadas identificaram um único aminoácido como a base que inicia a reação e revelaram como o cofator flavina ligado cicla entre formas oxidadas e reduzidas sem nunca ser consumido.
Uma enzima finalizadora que ajusta a cadeia lateral
Uma vez que a SavA constrói o esqueleto butenolida quiral, a SavB — uma enzima citocromo P450 — assume para decorar a cadeia de carbono ligada. Na presença de seus parceiros redox e de um cofator celular comum, a SavB realiza uma série precisa de oxidações em dois átomos de carbono adjacentes. Análises com resolução temporal revelaram dois intermediários: primeiro um produto monohidroxilado e em seguida uma forma ceto, antes que a avenolida totalmente funcional apareça. Medições por ressonância magnética nuclear confirmaram as posições e os arranjos tridimensionais desses novos grupos. O trabalho demonstra que a SavB introduz esses átomos de oxigênio em uma ordem definida e com controle rigoroso sobre a orientação, uma característica importante para a atividade biológica do hormônio. 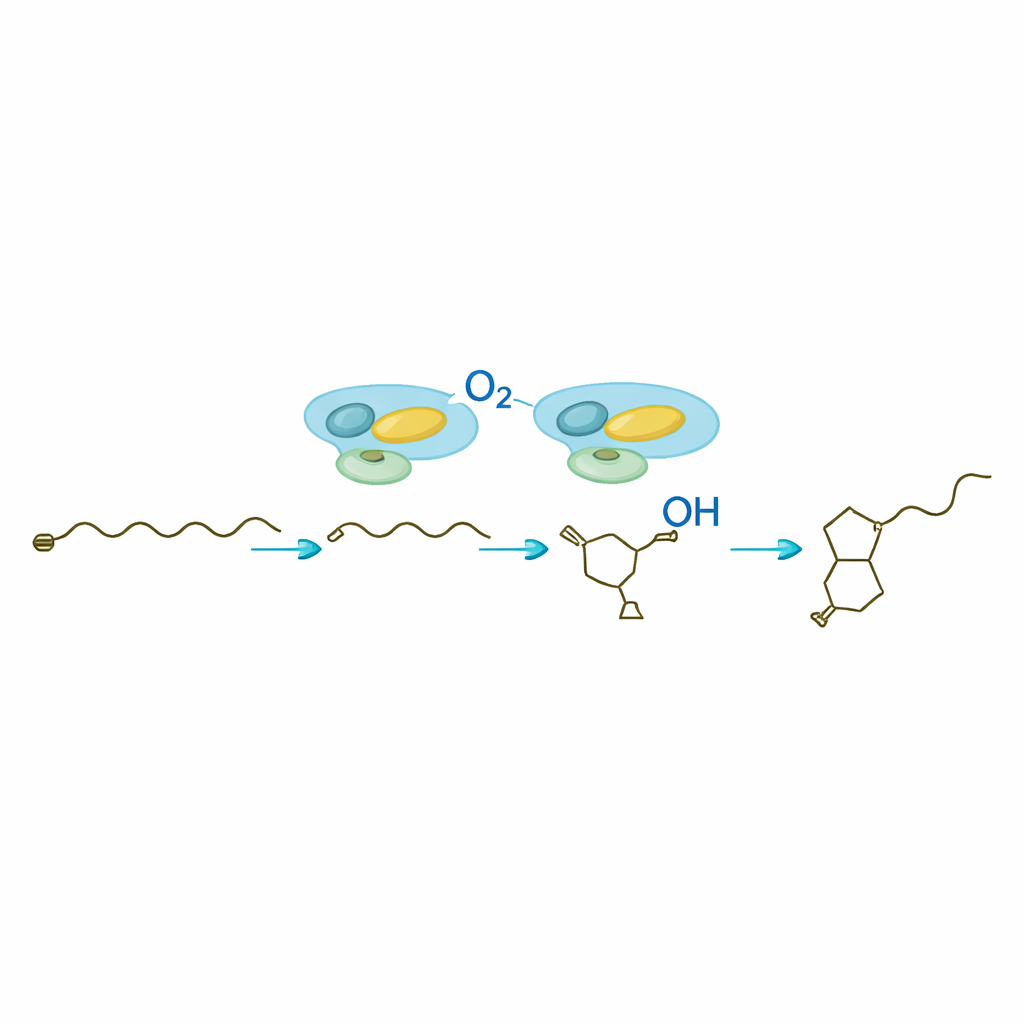
Lições de química verde a partir de enzimas bacterianas
Juntas, SavA e SavB convertem um bloco de construção comum derivado de ácido graxo em uma molécula sinalizadora finamente ajustada usando apenas oxigênio do ar e auxiliares celulares padrão. Ao contrário de muitos processos industriais, a SavA não precisa de agentes redutores extras nem de reagentes sacrificial; seu cofator flavina simplesmente transporta elétrons enquanto o próprio substrato fornece a força motriz. Os autores destacam a SavA como um novo tipo de flavoenzima multifuncional com forte potencial como biocatalisador para a fabricação sustentável de butenolidas e motivos relacionados. Em termos práticos, aproveitar ou engenheirar tais enzimas poderia um dia permitir que fábricas — ou microrganismos projetados — produzissem fragmentos importantes de fármacos e químicos agrícolas a partir de insumos renováveis em condições brandas, reduzindo tanto custo quanto pegada ambiental.
Citação: Li, W., Zhao, J., Zeng, W. et al. Trifunctional flavoenzyme-catalyzed asymmetric 4-alkyl-butenolide assembly in avenolide biosynthesis. Nat Commun 17, 2459 (2026). https://doi.org/10.1038/s41467-026-69265-8
Palavras-chave: biossíntese de butenolida, flavoenzima SavA, hormônio avenolida, biocatálise, sinalização de Streptomyces