Clear Sky Science · pt
Degradadores da proteína capsídeo do vírus da dengue exibem farmacologia diferenciada em relação a inibidores do capsídeo
Virar a casca do vírus contra ele mesmo
A febre da dengue infecta centenas de milhões de pessoas a cada ano, e ainda assim os médicos não dispõem de antivirais confiáveis para tratá‑la. Este estudo explora uma nova maneira de desarmar o vírus da dengue destruindo um dos seus blocos de construção mais importantes dentro das células infectadas, em vez de apenas tentar bloquear sua atividade. O trabalho mostra que moléculas cuidadosamente projetadas podem marcar uma proteína viral chave para eliminação pelo próprio sistema de gestão de resíduos da célula, reduzindo a produção do vírus e atenuando sua capacidade de se esconder das defesas imunológicas.
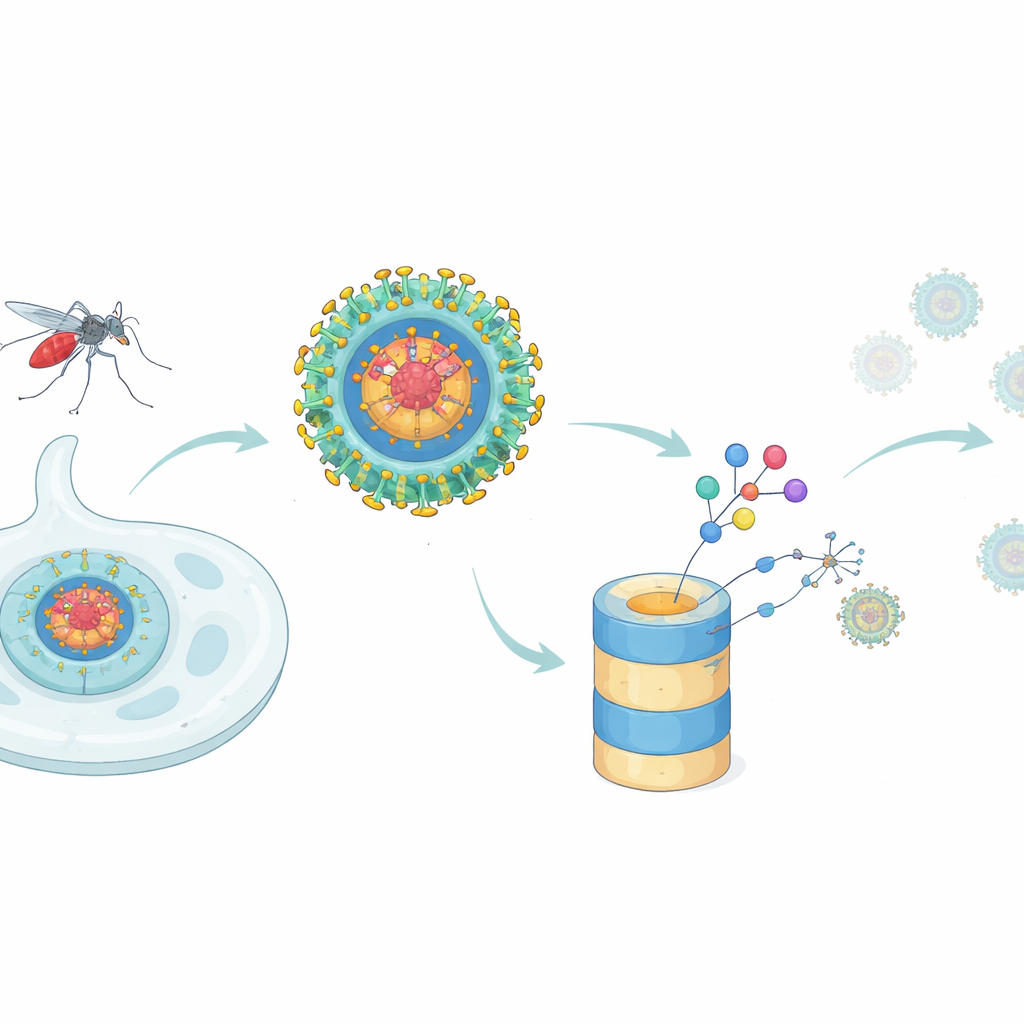
Uma nova tática para deter a dengue
A maioria dos antivirais age como tampões numa máquina: posicionam‑se em um sítio funcional de uma proteína viral e tentam bloqueá‑la. Essa abordagem encontra dificuldades quando uma única proteína viral desempenha muitas funções diferentes, ou quando pequenas mutações enfraquecem a aderência do fármaco. A proteína capsídeo da dengue é um exemplo claro. Ela forma a concha central que embala o material genético viral em novas partículas, mas também interfere com a célula hospedeira ao interagir com várias proteínas humanas e ao suprimir a resposta por interferon do organismo, um alarme antiviral de linha de frente. Os autores se perguntaram se um conceito farmacológico mais recente — a degradação proteica direcionada — poderia ir além dos inibidores clássicos ao realmente remover a proteína capsídeo das células infectadas.
Projetando um “caçador de recompensas” molecular
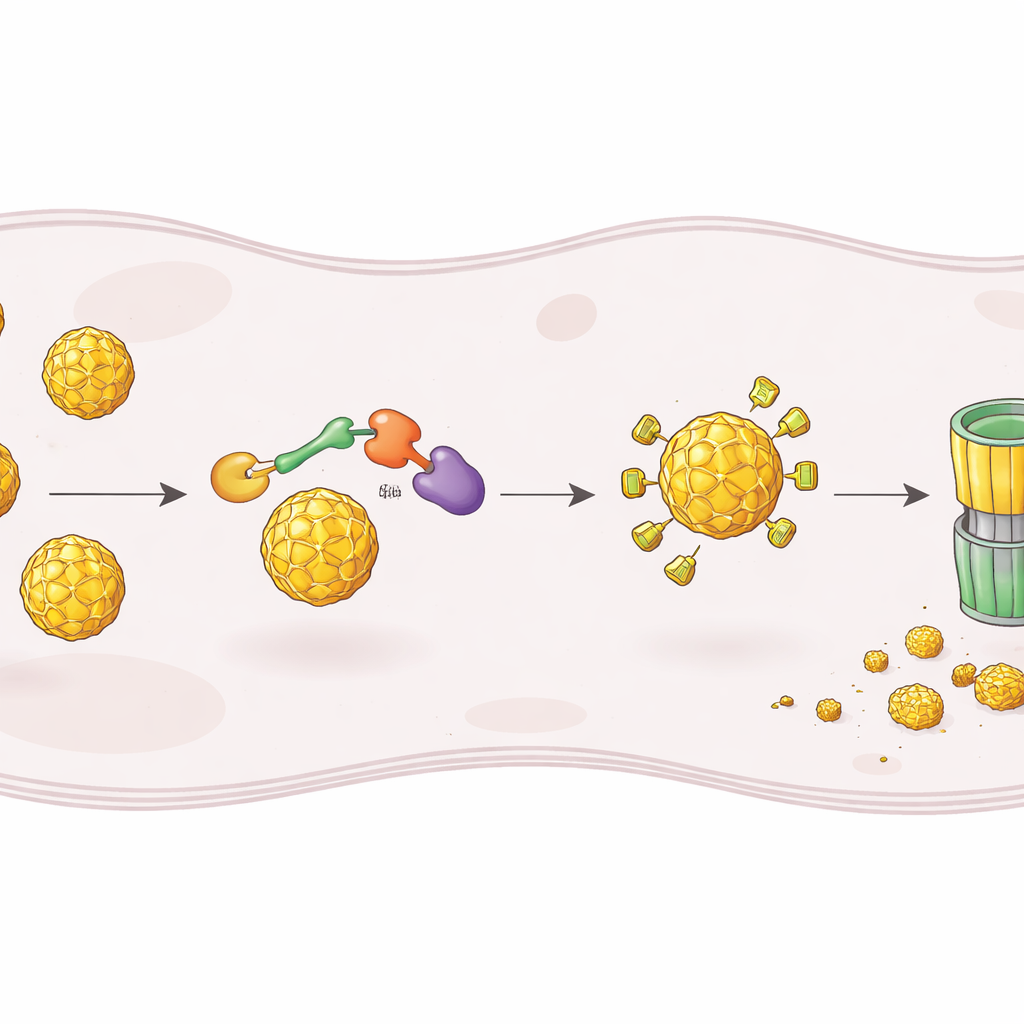
Para construir esse degradador, os pesquisadores partiram do ST148, uma pequena molécula conhecida que se liga ao capsídeo da dengue e interfere na montagem de novas partículas virais. Eles ligaram quimicamente o ST148 a um segundo módulo que recruta um complexo enzimático humano responsável por marcar proteínas para destruição. As moléculas quiméricas resultantes, chamadas PROTACs, são desenhadas para agarrar o capsídeo por uma extremidade e um complexo E3 ligase pela outra, aproximando‑os para que o capsídeo seja marcado com etiquetas de ubiquitina e entregue ao proteassoma da célula, o principal triturador de proteínas. Ao testar vários comprimentos de ligação e grupos recrutadores de ligase, identificaram um composto de destaque, denominado RPG‑01‑132, que reduziu de forma consistente os níveis de capsídeo em células infectadas de maneira dependente da forma CRBN da ligase e do funcionamento normal do proteassoma.
Interrompendo a produção viral e a evasão imune
Com um degradador funcional em mãos, a equipe examinou o que ele realmente fazia na infecção por dengue. Em células derivadas do fígado infectadas pelo vírus da dengue, o RPG‑01‑132 provocou uma queda acentuada no número de vírus infecciosos liberados, em concentrações nas quais ele apenas reduzia parcialmente os níveis totais de capsídeo. Importante: outras proteínas virais e o RNA viral permaneceram inalterados, mostrando que o composto não estava simplesmente envenenando a replicação geral, mas agindo de forma específica por meio da perda do capsídeo. A microscopia eletrônica forneceu uma leitura visual: células tratadas com o inibidor original ST148 acumularam pilhas de partículas virais parcialmente formadas no retículo endoplasmático, compatível com um bloqueio na montagem, enquanto células tratadas com o degradador praticamente não exibiram vírions visíveis. O degradador também aliviou a capacidade do capsídeo de silenciar a sinalização de interferon‑β em um sistema repórter, sugerindo que o papel não estrutural do capsídeo em desarmar a imunidade inata pode ser revertido ao degradá‑lo.
Superando a diversidade viral e a resistência a fármacos
O vírus da dengue apresenta quatro sorotipos principais que diferem na forma como respondem a inibidores direcionados ao capsídeo, e a resistência pode surgir por mutações pontuais. Os autores compararam o degradador com o ST148 em cepas representativas dos quatro sorotipos e contra um vírus portador de uma mutação (S34L no capsídeo) previamente demonstrada como tornando o ST148 ineficaz. Como esperado, o ST148 funcionou melhor em um sorotipo e perdeu atividade contra o mutante resistente. O RPG‑01‑132, em contraste, mostrou potência antiviral similar entre todos os sorotipos e manteve atividade contra o mutante S34L, agindo ainda pela mesma via de degradação dependente de CRBN. Isso ilustra uma vantagem chave da farmacologia “dirigida por evento”: o degradador não precisa se agarrar firmemente a cada molécula de capsídeo o tempo todo, desde que consiga desencadear eventos de degradação suficientes para alterar o equilíbrio.
O que isso significa para futuros tratamentos da dengue
Este estudo demonstra que a proteína capsídeo da dengue pode ser atacada não apenas como um componente estrutural do vírus, mas como um centro removível que sustenta múltiplas etapas da infecção e da evasão imune. Ao converter um inibidor tradicional em um degradador, os pesquisadores criaram um composto que bloqueia a produção viral, reverte parte da supressão da imunidade inata pelo vírus e permanece eficaz em diferentes linhagens virais e contra uma mutação de resistência conhecida. O RPG‑01‑132 em si precisará de otimização — melhor entrada celular, atividade mais forte em modelos animais e verificações rigorosas de segurança —, mas fornece uma prova de conceito convincente. Mais amplamente, o trabalho sugere que sequestrar a própria maquinaria de eliminação da célula pode abrir novas rotas para antivirais que são mais difíceis para os vírus evitarem e que podem neutralizar proteínas com muitos papéis diferentes dentro das células infectadas.
Citação: Chakravarty, A., Wang, LN., Golden, R.P. et al. Degraders of the dengue virus capsid protein exhibit differentiated pharmacology relative to capsid inhibitors. Nat Commun 17, 2594 (2026). https://doi.org/10.1038/s41467-026-69263-w
Palavras-chave: vírus da dengue, proteína capsídeo, degradação proteica direcionada, desenho de fármacos antivirais, PROTACs