Clear Sky Science · pt
Ativação cooperativa de ânions em um centro de cobalto por meio de emparelhamento iônico e desenho de ligante
Por que pequenos parceiros ao redor dos metais importam
Químicos costumam concentrar-se no “ator” principal de uma reação — um átomo metálico que ajuda a quebrar e formar ligações. Mas este artigo mostra que os parceiros discretos que pairam por perto, invisíveis a olho nu, podem alterar completamente o papel do metal. Ao modelar cuidadosamente o espaço ao redor de um átomo de cobalto, os autores revelam como dois ânions quase intercambiáveis, frequentemente tratados como espectadores passivos na química e em baterias, podem conduzir a resultados radicalmente diferentes. 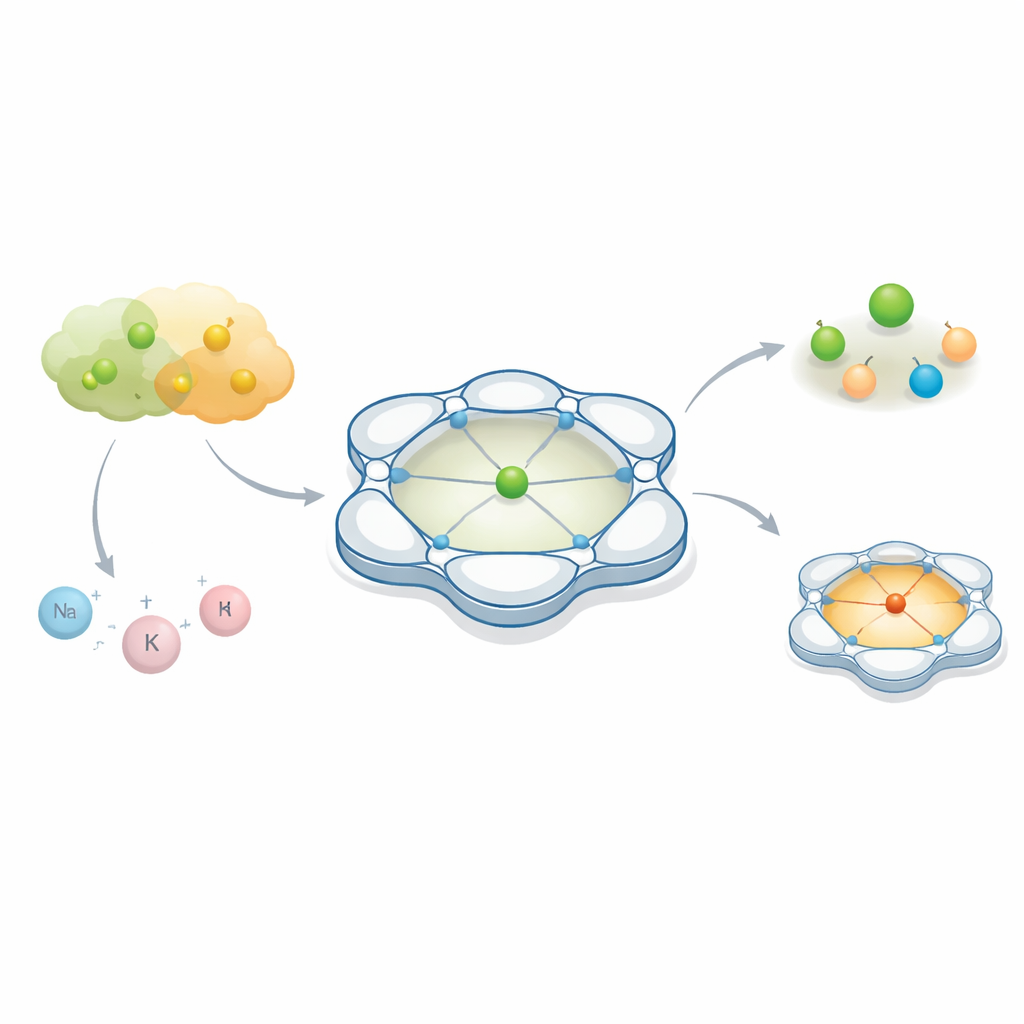
Construindo um bolso sob medida em torno do cobalto
Os pesquisadores projetaram uma estrutura orgânica em forma de gaiola chamada Py4Im que envolve firmemente um íon de cobalto. Essa estrutura é composta por vários anéis de piridina ligados e uma unidade imidazolidina, que juntas criam uma cavidade rígida, em forma de tigela, contendo um único grupo N–H. Essa pequena cavidade é “protica”, ou seja, pode formar ligações de hidrogênio, e aponta em uma direção específica, como uma pequena baía de acoplamento para ânions entrantes. Quando o cobalto é combinado com esse ligante, o resultado é uma família de complexos carregados positivamente cuja forma geral e bolso interno permanecem os mesmos enquanto o contraíon — o parceiro carregado negativamente — pode ser trocado. Isso torna o sistema um banco de testes ideal para observar como ânions diferentes se comportam no mesmo ambiente controlado.
Dois ânions parecidos, dois comportamentos muito diferentes
A equipe comparou dois ânions amplamente usados, tetrafluoroborato (BF4−) e hexafluorofosfato (PF6−), conhecidos como ânions fracamente coordenantes. Eles são populares porque normalmente se mantêm à distância dos centros metálicos, ajudando a estabilizar espécies altamente carregadas sem se envolver diretamente. Surpreendentemente, dentro da cavidade Py4Im eles não se comportam da mesma forma. Em condições brandas, PF6− doa um íon fluoreto ao cobalto, rompendo uma forte ligação P–F e formando um complexo bem definido de cobalto–fluoreto. Em contraste, BF4−, que costuma ser considerado o mais “frágil” dos dois, recusa-se a ceder fluoreto na mesma situação. Em vez disso, acomoda‑se em um arranjo estável ligado ao centro de cobalto sem completar o passo de quebra da ligação.
Observando íons se emparelhar e se mover
Para entender esses comportamentos contrastantes, os autores usaram uma combinação de técnicas de RMN de alta resolução e cálculos quântico‑químicos. Experimentos de RMN de difusão mediram a rapidez com que as espécies positiva e negativa se movem em solução, revelando o quão fortemente estão emparelhadas. Essas medidas mostraram que BF4− forma um par iônico mais próximo e persistente com o complexo de cobalto do que PF6−. A cavidade Py4Im posiciona o ânion diretamente sob o anel imidazolidina, onde ligações de hidrogênio do N–H e de grupos C–H próximos o mantêm no lugar. Cálculos computacionais confirmaram que esse emparelhamento mais forte e direcional com BF4− estabiliza tanto o estado inicial que a quebra da ligação B–F se torna ligeiramente desfavorável, mesmo que essa ligação seja intrinsecamente mais fraca que a P–F em PF6−. PF6−, emparelhando de forma mais frouxa, pode se aproximar, transferir fluoreto ao cobalto e partir como PF5, levando a um complexo de cobalto contendo fluoreto que é termodinamicamente acessível. 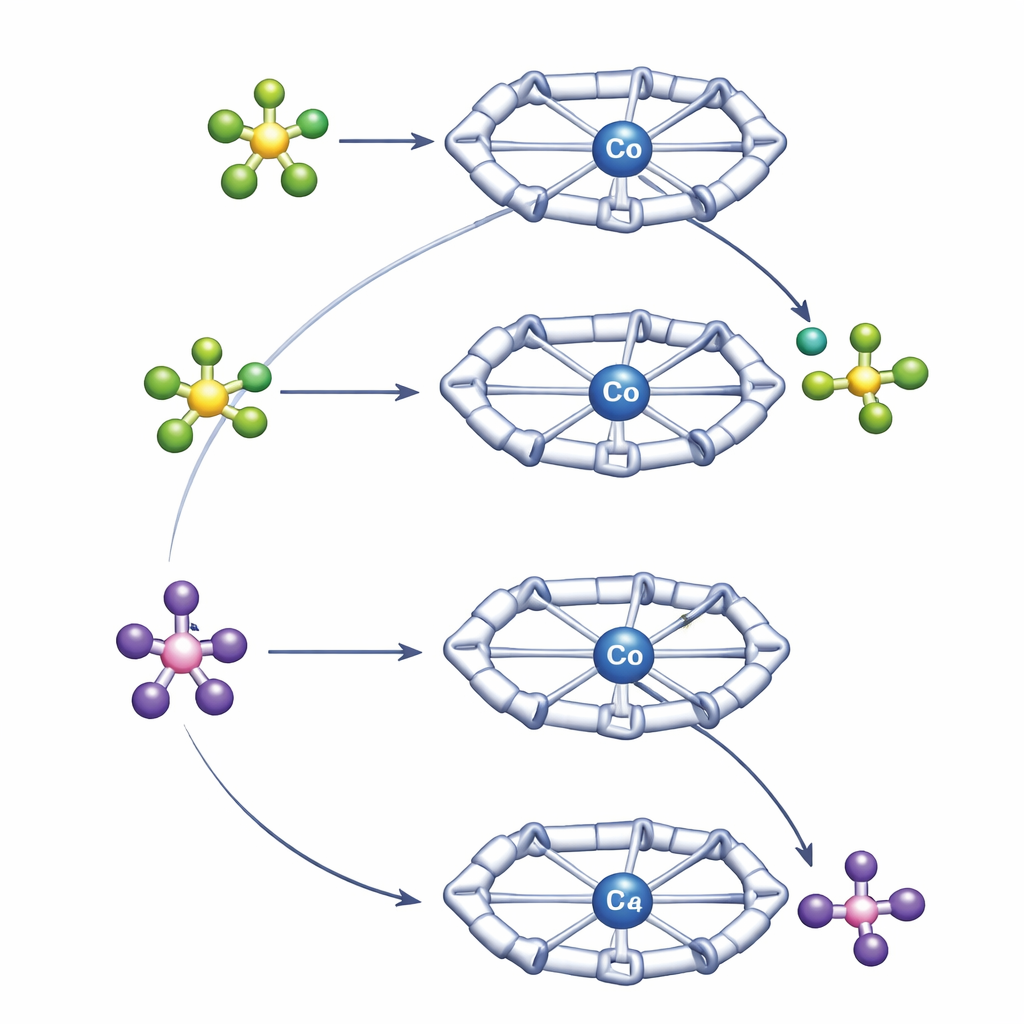
Transformando um fluoreto ligado em uma ferramenta útil
Uma vez formado, o complexo cobalto–fluoreto não é um beco sem saída. Os autores mostram que ele se comporta como uma fonte nucleofílica de fluoreto — em termos mais simples, pode fornecer fluoreto a parceiros positivamente carregados ou pobres em elétrons. Em solução, essa espécie cobalto–fluoreto transfere limpidamente fluoreto para centros carbônicos reativos, para átomos de silício em clorosilanos e para cloretos de acila, gerando fluoretos orgânicos enquanto o complexo de cobalto retorna à sua forma cloreto ou se liga ao novo parceiro. Em um movimento engenhoso, a equipe também demonstra que BF4− pode ser induzido a ceder fluoreto se uma base separada estiver presente para “capturar” o fragmento BF3 que fica para trás. Isso converte a via relutante de BF4− em uma que também produz o mesmo produto cobalto–fluoreto.
O que isso significa para projetar catalisadores mais inteligentes
Para um não especialista, a mensagem principal é que íons antes tratados como sais de fundo inertes podem, de fato, direcionar reações químicas de maneiras poderosas. Ao esculpir um bolso preciso em torno de um centro metálico e controlar quão firmemente os ânions se emparelham a ele, os autores inverteram a reatividade esperada de duas espécies quase idênticas. PF6−, normalmente visto como muito robusto, torna‑se a fonte de fluoreto mais fácil, enquanto BF4− fica preso por um emparelhamento mais forte, a menos que o sistema receba ajuda. Este trabalho fornece um roteiro para usar conjuntamente o desenho de ligantes e a escolha do contraíon para ajustar quão reativo é um complexo metálico — uma ideia que pode influenciar campos que vão da catálise homogênea ao desenho de eletrólitos para baterias avançadas, onde os “parceiros silenciosos” em solução podem estar longe de ser passivos.
Citação: Tarifa, L., Cano-Asensio, J., López, J.A. et al. Cooperative anion activation at a cobalt center through ion pairing and ligand design. Nat Commun 17, 2469 (2026). https://doi.org/10.1038/s41467-026-69257-8
Palavras-chave: complexos de cobalto, ânions fracamente coordenantes, transferência de fluoreto, emparelhamento iônico, desenho de ligante