Clear Sky Science · pt
O sulfeto de molibdênio metálico catalisa redes protometabólicas de reações de dióxido de carbono sob condições extremas
Como as rochas podem ter impulsionado a química da vida
Muito antes de as células vivas desenvolverem enzimas, a Terra ainda precisava de maneiras de converter gases simples, como o dióxido de carbono, em moléculas orgânicas das quais a vida depende. Este estudo investiga se certos minerais naturais, semelhantes aos encontrados perto de fontes hidrotermais submarinas, poderiam ter atuado como “motores químicos” primitivos. Ao mostrar que uma forma metálica de sulfeto de molibdênio pode transformar dióxido de carbono em uma teia surpreendentemente rica de compostos orgânicos, o trabalho oferece um cenário concreto de como a química central da vida pode ter começado em um planeta sem vida.

Respiradouros quentes e motores químicos ocultos
A vida moderna funciona com redes complexas de reações que deslocam carbono através de células e ecossistemas. Essas redes dependem de proteínas chamadas enzimas, que por sua vez são produtos da evolução. A grande questão é o que veio antes. Os autores buscaram inspiração em respiradouros hidrotermais—chaminés naturais de água quente no fundo do oceano ricas em sulfetos metálicos e gás hidrogênio—como cenários prováveis para a química de carbono mais primitiva. Nesses locais, água quente e pressurizada encontra rochas contendo metais como ferro, níquel e molibdênio. Experimentos anteriores mostraram que alguns desses metais podem converter dióxido de carbono em pequenos compostos orgânicos, mas geralmente apenas em fragmentos das vias metabólicas, não em redes completas.
Um imitador mineral de enzimas ancestrais
A equipe concentrou-se em uma forma particular de sulfeto de molibdênio, chamada fase 1T′, cujo arranjo atômico imita os centros metal-enxofre encontrados em enzimas modernas que processam dióxido de carbono. Em alta temperatura e pressão em água, com hidrogênio como combustível, esse mineral catalisou a conversão de dióxido de carbono dissolvido (modelado como bicarbonato) em uma gama surpreendentemente ampla de ácidos orgânicos. Ao variar cuidadosamente temperatura, tempo de reação e pressão de gás, e ao rastrear produtos por cromatografia, espectrometria de massa e RMN, identificaram 32 intermediários e produtos finais diferentes emergindo da mesma fonte simples de carbono.
Reconstruindo as vias centrais de carbono da vida sem enzimas
Esses 32 compostos não são aleatórios. Muitos são as mesmas moléculas que ocupam o núcleo do metabolismo moderno—como acetato, piruvato, oxaloacetato, succinato e alfa-cetoglutarato. Coletivamente, eles se alinham a cinco rotas principais de fixação de carbono usadas por microrganismos contemporâneos: a via acetil–CoA e variantes do ciclo de Krebs e ciclos relacionados. Nos experimentos, essas vias apareceram como uma rede interconectada: o acetato ligava vários ciclos; moléculas maiores se degradavam e se reformavam; e intermediários-chave desapareciam e reapareciam conforme as condições mudavam. A produção de ácidos com múltiplos carbonos atingiu alta eficiência, com até cerca de 70% do carbono convertido terminando em moléculas contendo dois ou mais carbonos. A rede de reação também exibiu oscilações em que as quantidades de certos produtos aumentavam e diminuíam ao longo do tempo, ecoando o comportamento dinâmico de sistemas químicos vivos.
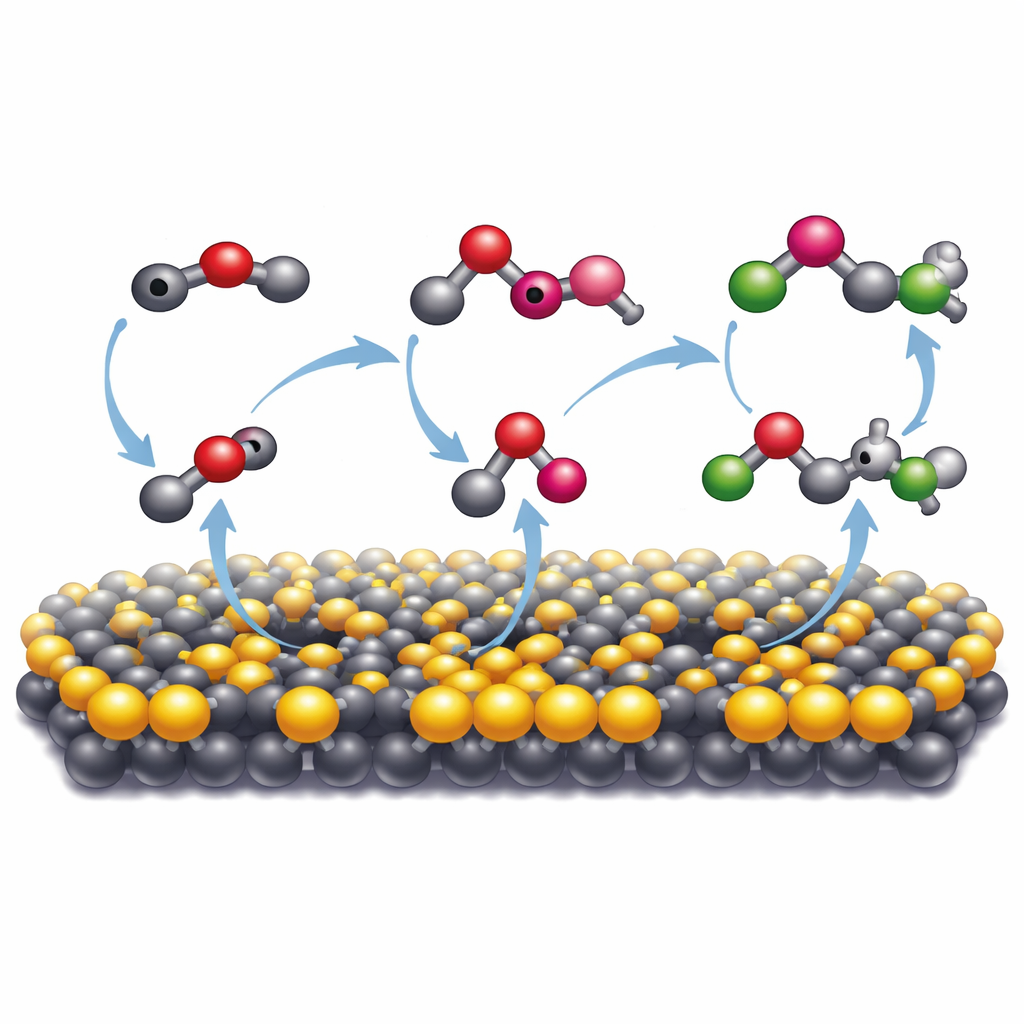
Como o mineral faz os átomos de carbono se unirem
Para entender por que esse mineral em particular foi tão eficaz, os pesquisadores o compararam com uma forma mais comum de sulfeto de molibdênio que tem uma estrutura atômica diferente. Apenas a forma metálica e distorcida—com muitas lacunas de enxofre—promoveu a formação extensa de organics maiores. Técnicas espectroscópicas revelaram que, nessa superfície, monóxido de carbono derivado do dióxido de carbono se liga fortemente e é reduzido adicionalmente a fragmentos altamente reativos, ou radicais. Esses radicais são estabilizados apenas o suficiente na superfície mineral para colidirem entre si e formarem novas ligações carbono–carbono. Medições de spin de elétrons confirmaram a presença desses radicais, e a adição de um químico armadilha de radicais suprimiu fortemente os produtos de múltiplos carbonos. Simulações computacionais corroboraram esse quadro, mostrando que as vacâncias de enxofre e a estrutura eletrônica alterada da fase 1T′ facilitam a doação de elétrons pela superfície e aproximam fragmentos de carbono para que possam se combinar.
Da química das pedras ao primeiro metabolismo
Conjugando os achados, sugere-se que certos minerais de sulfeto metálico na Terra primitiva poderiam ter sustentado uma química de carbono complexa e auto-organizadora muito antes da existência de enzimas. Em cenários de respiradouros hidrotermais, onde fluidos quentes e ricos em hidrogênio encontram dióxido de carbono e rochas portadoras de metais, um mineral como o sulfeto de molibdênio 1T′ poderia ter continuamente convertido carbono inorgânico em uma teia de vias orgânicas interconectadas semelhantes aos ciclos metabólicos modernos. Para um leitor não especialista, a mensagem-chave é que a química central da vida pode não ter precisado da vida para começar: sob condições adequadas, rochas simples, água e gás podem construir espontaneamente muitas das mesmas moléculas e circuitos reacionais que as células vivas ainda usam hoje.
Citação: Chen, P., Liu, X., He, D. et al. Metallic molybdenum sulfide catalyses protometabolic carbon dioxide reaction networks under extreme conditions. Nat Commun 17, 2395 (2026). https://doi.org/10.1038/s41467-026-69255-w
Palavras-chave: origem da vida, química prebiótica, respiradouros hidrotermais, fixação de carbono, sulfeto de molibdênio