Clear Sky Science · pt
Modelos de deep learning interpretáveis e generativos elucidam motivos intrinsecamente desordenados que promovem separação de fase
Por que pequenos segmentos de proteína importam
Dentro de cada uma de nossas células, moléculas vitais frequentemente se agrupam em glóbulos semelhantes a gotículas chamados condensados biomoleculares. Essas gotículas ajudam a organizar a química sem as paredes de uma membrana, moldando como genes são ativados, como sinais são transmitidos e como as células respondem ao estresse. Muitas dessas gotículas são formadas por trechos flexíveis de proteínas conhecidos como regiões intrinsecamente desordenadas. Ainda assim, os biólogos têm dificuldade em identificar os pequenos trechos de sequência que realmente fazem essas gotículas se formar. Este estudo apresenta uma estrutura de deep learning, PhaSeMotif, que pode tanto localizar esses segmentos-chave quanto projetar novos, oferecendo aos pesquisadores uma nova e poderosa ferramenta para sondar e reprogramar gotículas celulares.
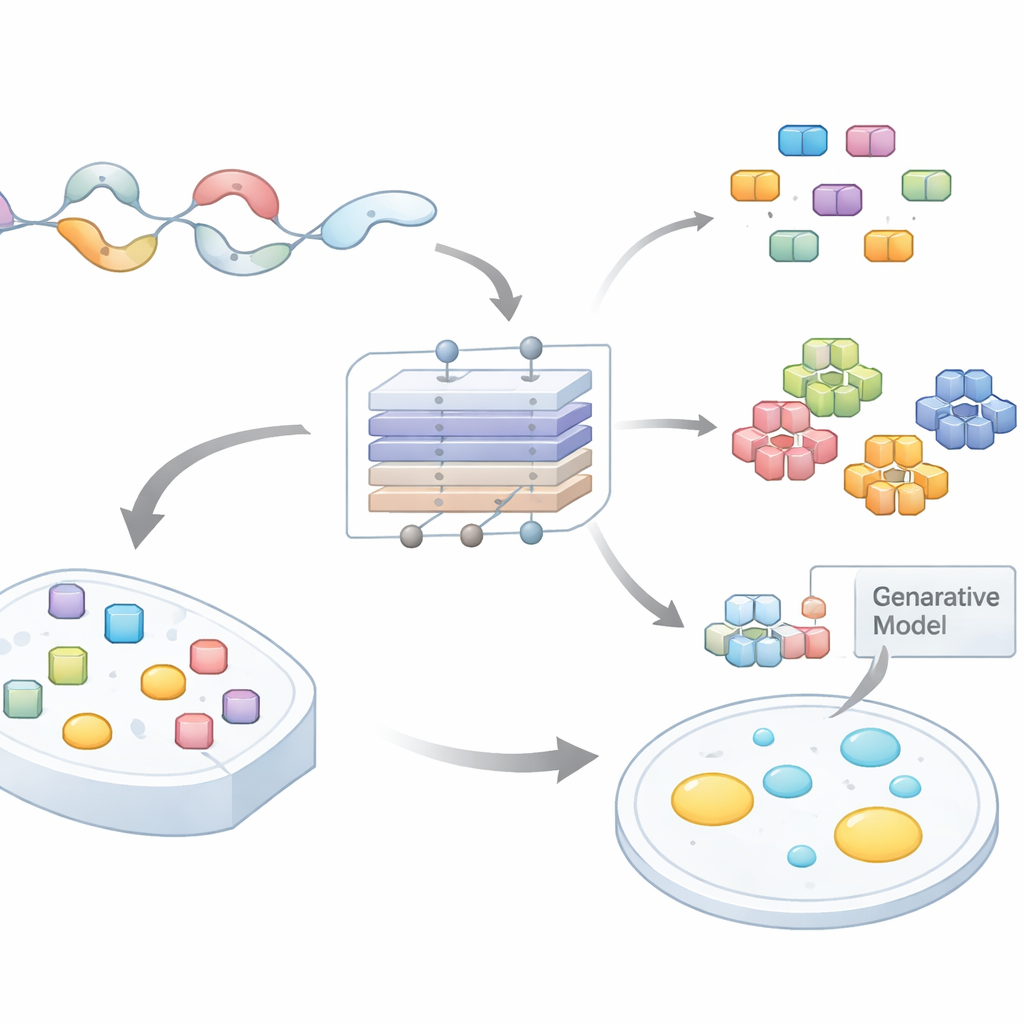
De caudas proteicas bagunçadas a ideias testáveis
Muitas proteínas contêm longas caudas flexíveis que não se dobram em formas fixas. Essas regiões desordenadas são enriquecidas em certos aminoácidos e frequentemente abrigam padrões repetidos ou pequenos motivos. Um número crescente de estudos mostra que tais motivos dirigem a condensação ao permitir muitas interações fracas simultâneas. No entanto, escanear proteomas inteiros para descobrir quais pequenos trechos importam, e por quê, tem sido um grande gargalo. Ferramentas computacionais existentes normalmente avaliam proteínas inteiras ou grandes regiões, oferecendo pouca orientação sobre onde mutar ou o que testar em laboratório. Os autores propuseram construir um modelo que prevê não apenas se uma região desordenada pode formar gotículas, mas também quais subsequências exatas estão fazendo o trabalho pesado.
Um mapa de deep learning dos motivos que promovem gotículas
A equipe compilou grandes conjuntos de dados de regiões desordenadas em várias espécies e as rotulou segundo a probabilidade de as proteínas hospedeiras sofrerem separação de fase. Eles então treinaram uma rede neural baseada em atenção, PhaSeMotif, que recebe uma sequência de aminoácidos de qualquer comprimento e produz uma pontuação de formação de gotículas. Crucialmente, a rede usa uma combinação de camadas convolucionais e mecanismos de atenção para avaliar quanto cada janela curta da sequência contribui para essa pontuação. Ao traçar o caminho de volta através do modelo (usando técnicas semelhantes à backpropagation guiada), os autores extraíram trechos de alta importância — pequenos motivos frequentemente com menos de 20 resíduos — que o modelo considerou essenciais para a formação de gotículas.
Colocando previsões à prova em células vivas
Para verificar se esses motivos realmente importavam, os pesquisadores recorreram a um sistema ativado por luz em células humanas. Eles fundiram regiões desordenadas preditas como formadoras de gotículas a um módulo de oligomerização sensível à luz e a uma etiqueta fluorescente. Sob luz azul, esses constructos condensaram-se rapidamente em pontuações brilhantes, relatando a separação de fase em tempo real. A equipe então removeu cirurgicamente motivos individuais substituindo-os por conectores neutros e flexíveis de igual comprimento. Em 82% das 17 sequências alteradas testadas, a formação de gotículas foi drasticamente enfraquecida ou desapareceu por completo, enquanto mutações de controle fora dos segmentos identificados pelo PhaSeMotif frequentemente tiveram pouco efeito. Importante, muitos desses motivos-chave coincidiam com locais onde mutações associadas a doenças são conhecidas por perturbar a condensação, ressaltando sua relevância biológica.
Revelando um vocabulário de tipos de motivos
Com mais de 17.000 motivos em mãos, os autores perguntaram-se se havia “sabores” comuns desses segmentos que promovem gotículas. Eles analisaram composição e padronização de aminoácidos e então agruparam os motivos em nove clusters. Alguns clusters eram ricos em resíduos aromáticos e glicina, consistente com interações π–π e catiônico–π aderentes. Outros continham manchas separadas de cargas positivas e negativas, favorecendo atração eletrostática e partição seletiva em condensados particulares. Clusters adicionais eram dominados por prolina e glicina, que sustentam flexibilidade, ou por longas sequências de glutamina que podem formar redes densas de ligações de hidrogênio. Diferentes compartimentos celulares e tipos de condensados exibiram misturas características dessas classes de motivos, sugerindo que a composição dos motivos ajuda a determinar onde e com quais parceiros uma proteína irá condensar.
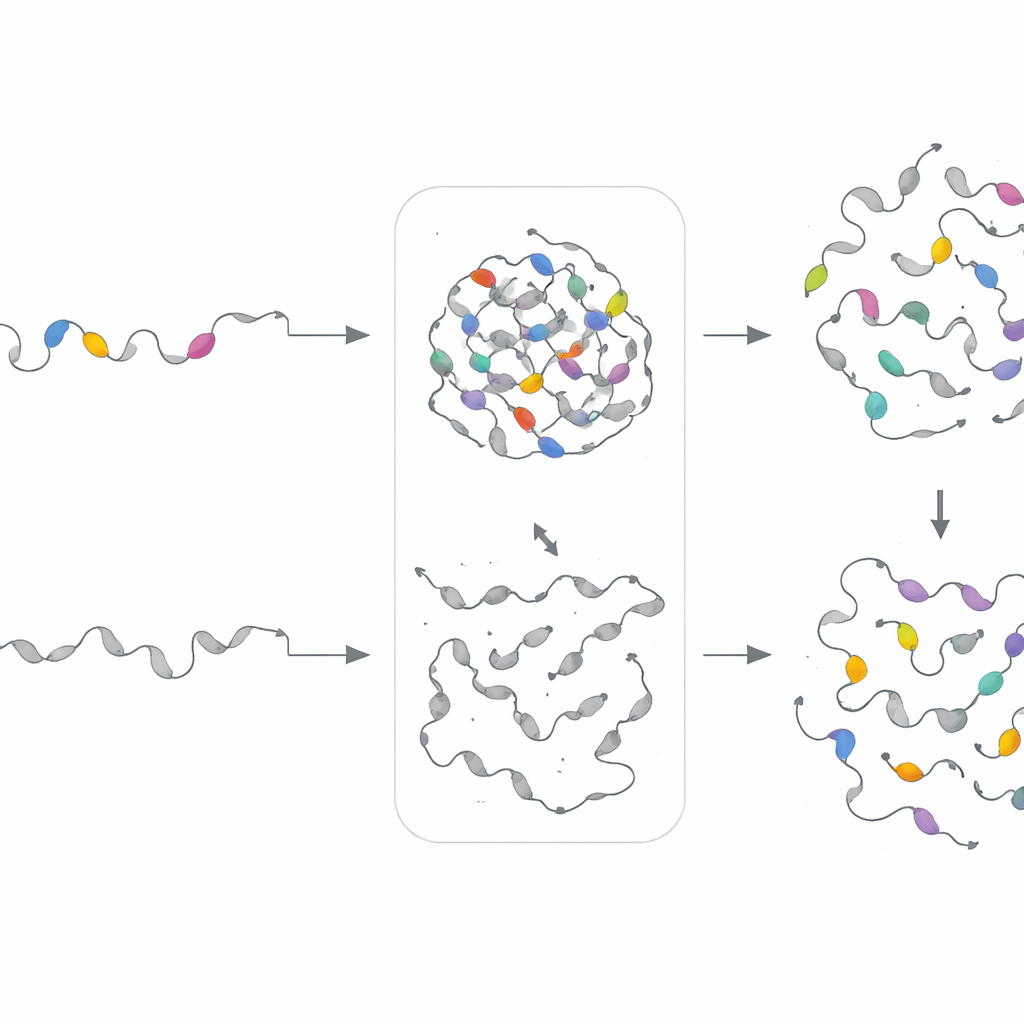
Projetando novos motivos para provar as regras
Para testar se “receitas” de motivos — em vez de sequências exatas — governam o comportamento das gotículas, a equipe construiu modelos generativos separados para cada cluster de motivos. Esses autoencoders variacionais aprenderam os padrões estatísticos de um dado cluster e então produziram novas sequências artificiais que compartilhavam as mesmas assinaturas composicionais, mas com ordem diferente. Os pesquisadores trocaram experimentalmente esses motivos sintéticos em proteínas cujos segmentos originais haviam sido deletados. Notavelmente, em 18 de 21 casos, os motivos projetados restauraram a separação de fase nas células, às vezes até ajustando a velocidade ou a densidade da formação de gotículas. Isso mostra que o PhaSeMotif captura regras de projeto subjacentes que podem ser reutilizadas para construir ou reparar regiões formadoras de gotículas.
O que isso significa para a biologia e a doença
Ao ligar deep learning interpretável com design generativo e testes celulares diretos, este trabalho transforma a noção vaga de “regiões desordenadas formadoras de gotículas” em um conjunto concreto de motivos curtos e compostáveis. Para não especialistas, a conclusão é que os cientistas agora podem ler e escrever os pequenos segmentos de proteína que controlam como gotículas celulares se montam, se misturam e falham. Isso abre a porta para descoberta mais rápida de mutações causadoras de doenças nesses segmentos, estudos mecanicistas mais claros sobre como os condensados organizam a fisiologia celular e, eventualmente, o projeto racional de proteínas que direcionem gotículas para aplicações terapêuticas ou de biologia sintética.
Citação: Yang, H., You, K., Ma, L. et al. Interpretable and generative deep learning models explicate phase separating intrinsically disordered motifs. Nat Commun 17, 2571 (2026). https://doi.org/10.1038/s41467-026-69252-z
Palavras-chave: condensados biomoleculares, proteínas intrinsecamente desordenadas, separação de fase, deep learning, motivos de proteínas