Clear Sky Science · pt
Hepatócitos reprogramados funcionalmente por células de câncer colorretal com alta expressão de KIAA1199 favorecem o acúmulo de neutrófilos Egr1+ pró‑metastáticos
Quando o câncer de cólon mira o fígado
A maioria das pessoas imagina a disseminação do câncer como células desonestas que simplesmente se destacam e vão flutuar para novos órgãos. Este estudo revela uma história mais inquietante: tumores colorretais podem silenciosamente reprogramar o fígado muito antes da chegada de quaisquer células cancerosas, preparando um “solo” acolhedor onde tumores futuros podem se estabelecer com facilidade. Compreender essa fase oculta de preparação pode abrir caminho para tratamentos que impeçam as metástases hepáticas — a principal causa de morte no câncer colorretal — antes que comecem.
Uma preparação furtiva antes da chegada dos tumores
O câncer colorretal frequentemente metastatiza para o fígado, mas apenas alguns tumores fazem isso de forma agressiva. Os autores concentraram‑se em uma molécula chamada KIAA1199, abundante em cânceres colorretais de alto risco. Em modelos animais e amostras de pacientes, tumores com alta expressão de KIAA1199 não apenas cresciam mais rápido; eles também preparavam o fígado para se tornar um “nicho pré‑metastático”, um microambiente particularmente favorável às células cancerosas que chegam. Mesmo quando tumores hepáticos foram semeados experimentalmente de uma fonte separada, animais portadores de tumores colorretais com alta KIAA1199 desenvolveram muito mais metástases hepáticas e tiveram sobrevida reduzida. Isso mostrou que sinais vindos do tumor primário, e não apenas células cancerosas migrantes, estavam remodelando o fígado com antecedência.
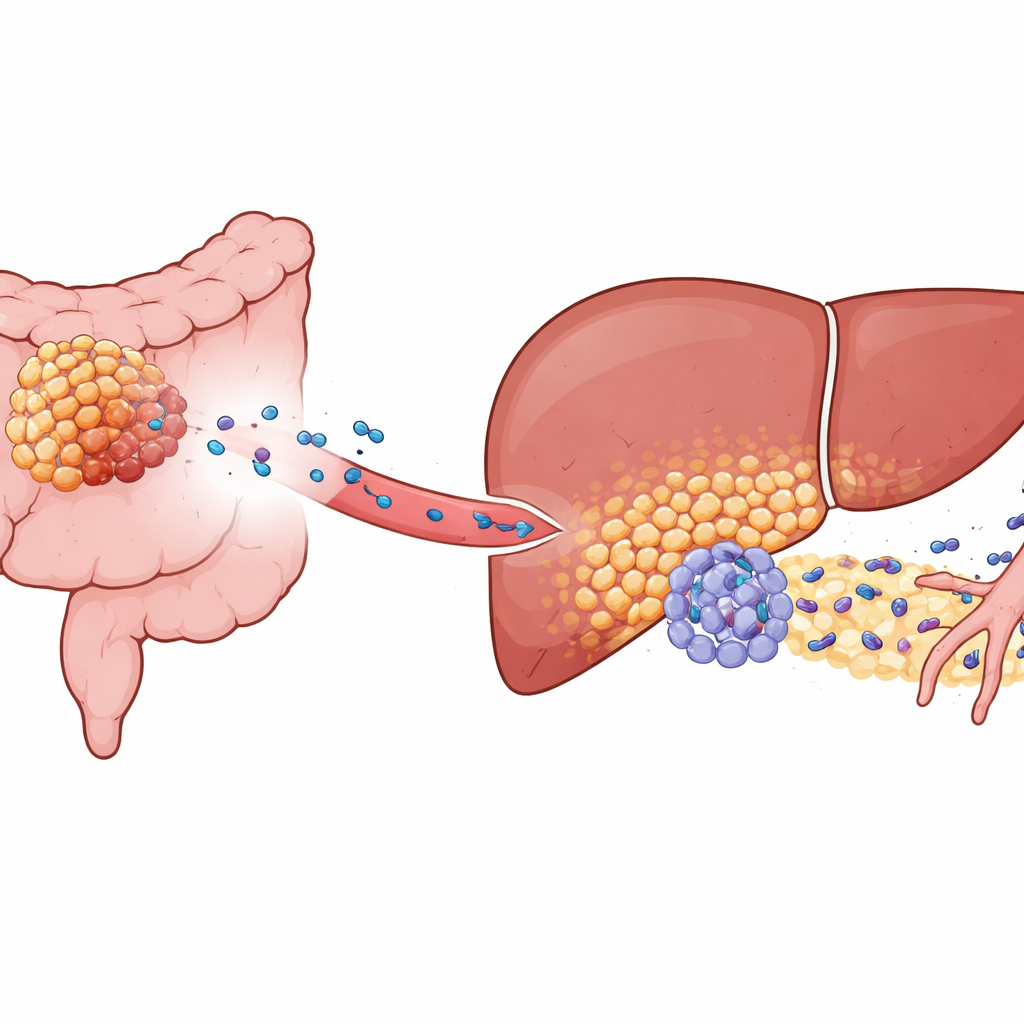
Células hepáticas reprogramadas em auxiliares tumorais
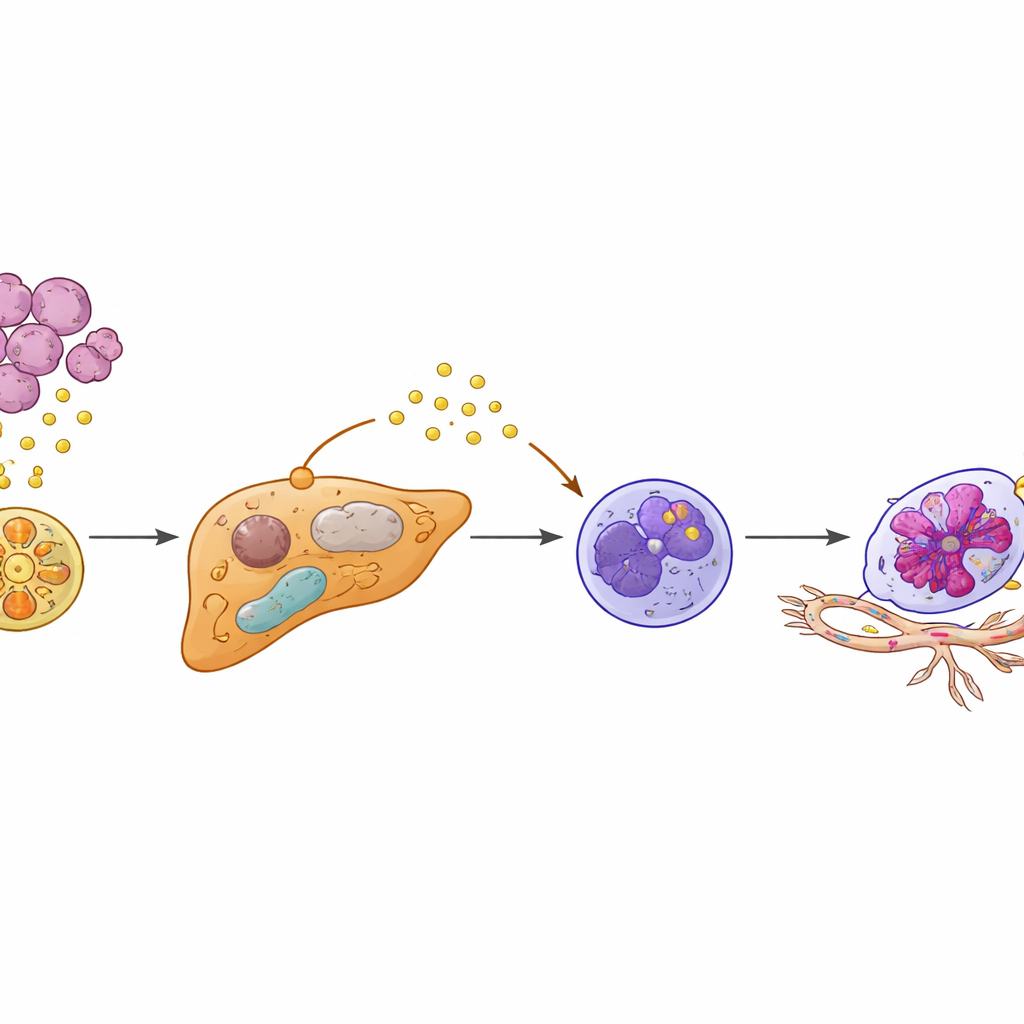
Ao aprofundar, os pesquisadores usaram sequenciamento de célula única e mapeamento espacial para examinar o tecido hepático em alta resolução. Descobriram um subgrupo distinto de hepatócitos — normalmente as células responsáveis pelas funções do fígado — que haviam sido “reprogramados funcionalmente”. Essas células surgiam apenas na presença de tumores com alta expressão de KIAA1199. Em vez de gerenciar o metabolismo de forma discreta, os hepatócitos alterados mudaram para um estilo metabólico mais parecido com o observado em contextos malignos e reduziram a expressão de um regulador protetor chamado PPARγ, que normalmente ajuda a conter inflamação e respostas ao estresse. Com PPARγ suprimido, esses hepatócitos começaram a produzir altos níveis de uma proteína chamada SAA2, que liberaram ao redor, particularmente na interface onde o tecido hepático encontra células tumorais invasoras.
Convertendo defensores comuns em neutrófilos pró‑metastáticos
Neutrófilos — glóbulos brancos conhecidos por combater infecções — também se comportaram de forma estranha neste fígado preparado. Os autores identificaram um subconjunto especial com assinatura “Egr1+”, nomeado por um fator de transcrição que remodela a função dessas células. Em vez de chegarem da corrente sanguínea já alterados, os neutrófilos parecem ser reeducados localmente pelos hepatócitos reprogramados. A SAA2 liberada pelos hepatócitos ligava‑se a um receptor chamado FPR2 em neutrófilos próximos, ativando um circuito de sinalização PI3K‑AKT que estabilizava a atividade de Egr1. O resultado foi um neutrófilo de vida útil prolongada e altamente ativo que secretava grandes quantidades de VEGFA, um potente indutor de formação de novos vasos sanguíneos. Esses neutrófilos Egr1+ se agrupavam na interface tumor–fígado, exatamente onde novos e frágeis vasos estavam brotando.
Construindo vasos sanguíneos que recebem as células tumorais
O estudo mostra que esses neutrófilos reeducados não são meros espectadores — eles remodelam ativamente a vasculatura hepática. Em cultura celular, fatores liberados por neutrófilos Egr1+ fizeram células endoteliais proliferarem, migrarem e formar estruturas tubulares análogas a novos vasos. Em camundongos, a adição de neutrófilos Egr1+ aumentou as metástases hepáticas e acelerou a mortalidade. Bloquear etapas-chave da cadeia — seja o sinal SAA2–FPR2 aos neutrófilos ou a via PI3K‑AKT a jusante — interrompeu a sobrevivência dos neutrófilos e a produção de VEGFA, reduzindo o crescimento vascular e a disseminação metastática. Do mesmo modo, restaurar a atividade de PPARγ nos hepatócitos com o antidiabético rosiglitazona diminuiu os níveis de SAA2, contiveu o surgimento de neutrófilos Egr1+ e reduziu drasticamente a metástase hepática em modelos pré‑clínicos.
Do mecanismo à predição e prevenção
Como KIAA1199 no tumor e SAA2 no fígado ocupam posições altas nessa cascata, os autores testaram se essas proteínas poderiam ajudar a identificar pacientes com alto risco de metástase hepática. Em várias coortes de pacientes, pessoas com níveis sanguíneos elevados de ambos os marcadores tiveram muito mais probabilidade de desenvolver metástases hepáticas e de fazê‑lo mais cedo. Uma pontuação combinada simples KIAA1199–SAA2 superou cada marcador isolado na predição de risco e foi incorporada a um “nomograma” clínico que estima a probabilidade individual de disseminação hepática nos próximos dois anos. Em conjunto, os achados desenham um quadro claro: cânceres colorretais com alta expressão de KIAA1199 enviam sinais em vesículas que reprogramam hepatócitos, os quais, por sua vez, convertem neutrófilos próximos em cúmplices de longa vida que constroem vasos. Ao mirar esse eixo KIAA1199–PPARγ/SAA2–Egr1 — com drogas metabólicas, agentes que modulam o sistema imune ou ambos — pode ser possível não apenas tratar metástases hepáticas existentes, mas preveni‑las antes que se estabeleçam.
Citação: Li, L., Zhao, L., Cao, K. et al. Hepatocytes functionally reprogrammed by KIAA1199-high colorectal cancer cells favour the accumulation of pro-metastatic Egr1+ neutrophils. Nat Commun 17, 2462 (2026). https://doi.org/10.1038/s41467-026-69250-1
Palavras-chave: metástase hepática do câncer colorretal, nichos pré‑metastáticos, neutrófilos, reprogramação de hepatócitos, microambiente tumoral