Clear Sky Science · pt
Reduzir a metilação da lisina 4 da histona 3.3 na eminência ganglionar medial e no hipotálamo reproduz fenótipos de transtornos do neurodesenvolvimento
Como pequenas etiquetas químicas moldam cérebro e corpo
Por que algumas alterações genéticas causam tanto dificuldades de aprendizagem quanto crescimento incomum, como ser muito pequeno na infância mas obeso na idade adulta? Este estudo examina pequenas etiquetas químicas nas proteínas que embalam o DNA no cérebro e mostra como perturbá-las em apenas duas regiões-chave pode se propagar em convulsões, comportamento semelhante à ansiedade, problemas de memória e mudanças dramáticas no tamanho corporal em camundongos.
Interruptores nos dimmers do genoma
Dentro de toda célula cerebral, o DNA está enrolado em torno de proteínas em forma de carretel chamadas histonas. Marcas químicas colocadas nessas histonas funcionam como dimmers, aumentando ou diminuindo grupos de genes. Uma dessas marcas, adicionada em um local chamado H3K4, está fortemente ligada à ativação de genes. Estudos genéticos humanos revelaram que pessoas nascidas com defeitos em enzimas que adicionam ou removem essa marca frequentemente têm transtornos do neurodesenvolvimento que combinam deficiência intelectual, epilepsia e crescimento corporal anormal. No entanto, não estava claro quais células cerebrais são mais sensíveis a essa perturbação e como seu mau funcionamento poderia ligar excitabilidade cerebral e metabolismo do corpo inteiro.
Alvejando dois centros cerebrais críticos
Os pesquisadores criaram camundongos em que uma versão mutante de uma proteína histona (H3.3K4M) foi ativada apenas em células originadas de duas regiões cerebrais embrionárias: a eminência ganglionar medial, que produz muitas das células inibitórias “freio” do cérebro, e o hipotálamo em desenvolvimento, que ajuda a regular apetite, hormônios e balanço energético. Essa mutação bloqueia especificamente a metilação de H3K4 sem eliminar as histonas em si. Testes confirmaram que a proteína mutante estava amplamente presente nas áreas alvo e que as marcas normais de H3K4 foram fortemente reduzidas ali, enquanto os níveis globais de histonas permaneceram estáveis. Esse desenho imita muitas condições humanas em que apenas uma cópia de um gene relacionado a H3K4 é defeituosa, em vez de estar completamente ausente.
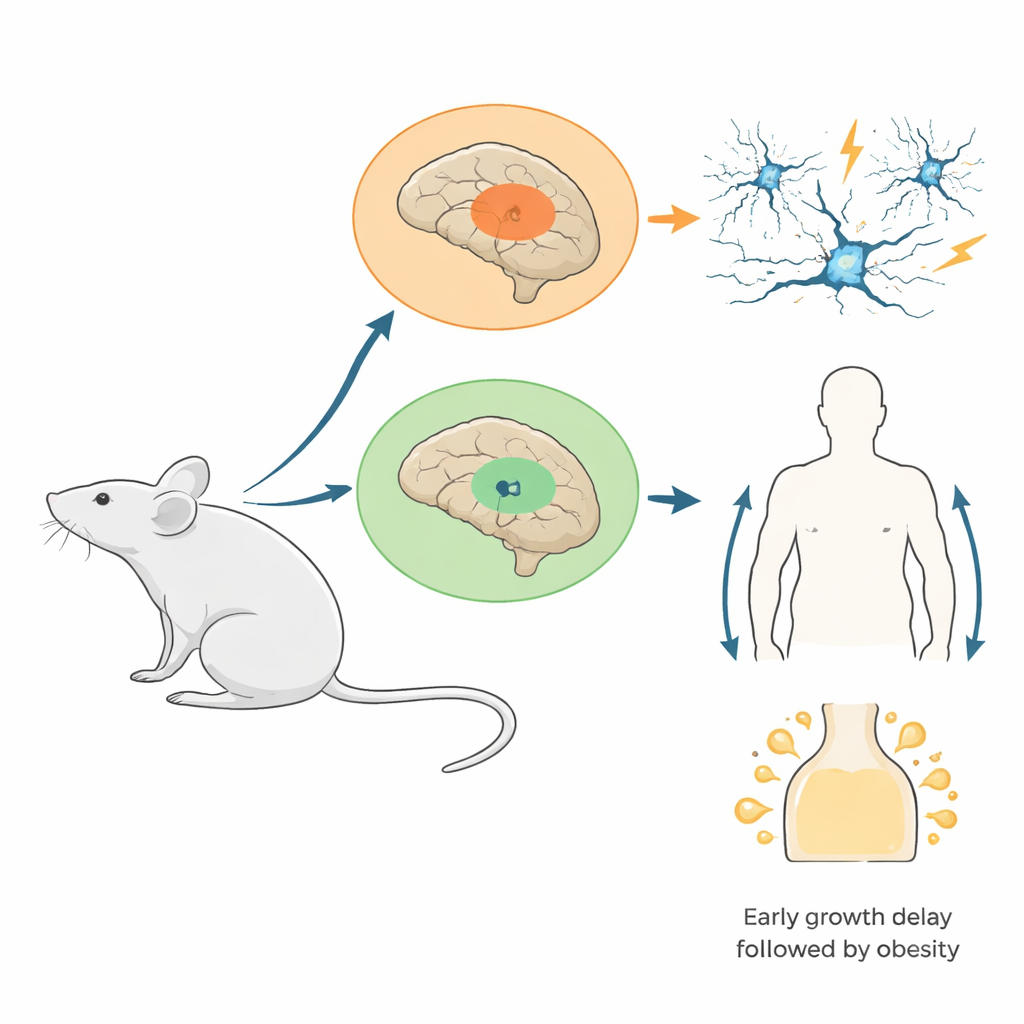
De células "freio" ausentes a circuitos com propensão a convulsões
À medida que esses camundongos cresciam, as consequências para os circuitos cerebrais ficaram claras. Jovens mutantes tinham menos interneurônios inibitórios no córtex e no hipocampo, especialmente um tipo de disparo rápido que normalmente mantém os ritmos neurais bem cronometrados. Registros detalhados mostraram que os interneurônios remanescentes estavam presentes, mas mais variáveis em suas propriedades elétricas, sugerindo que sua maturação foi perturbada. Quando o hipocampo foi estimulado em fatias cerebrais, as habituais oscilações de alta frequência “gama” — ritmos elétricos ligados ao processamento de informação — estavam mais fracas e mais lentas, e surgiram eventos anormais em rajadas. Em animais vivos, muitos mutantes, particularmente fêmeas, desenvolveram convulsões espontâneas e foram muito mais sensíveis a convulsões induzidas por drogas. No início do desenvolvimento, a equipe traçou essa perda celular principalmente à má migração dos interneurônios para o córtex, não ao aumento da morte celular ou à redução da divisão celular.
Reconfigurando a atividade gênica em células ligadas a convulsões
Para conectar essas mudanças físicas ao controle gênico, a equipe usou sequenciamento de núcleo único que lê tanto a atividade gênica quanto a acessibilidade do DNA em células individuais. Na eminência ganglionar medial embrionária, a maioria dos genes que mudaram nos mutantes foi silenciada, incluindo reguladores-chave que orientam as células para destinos inibitórios específicos. Em interneurônios adultos, o equilíbrio entre subtipos se alterou, e grupos de genes envolvidos na formação de conexões e no controle de correntes de potássio — os fluxos que ajudam a definir a velocidade de disparo — foram desregulados. A análise de redes destacou uma disrupção coordenada de genes de canais de potássio que já se sabe influenciam epilepsia e ritmos cerebrais, fornecendo um elo molecular direto entre a perda de uma marca de histona, a identidade alterada dos interneurônios e a suscetibilidade a convulsões.
Desequilíbrio hipotálamo e uma curva de crescimento em duas fases
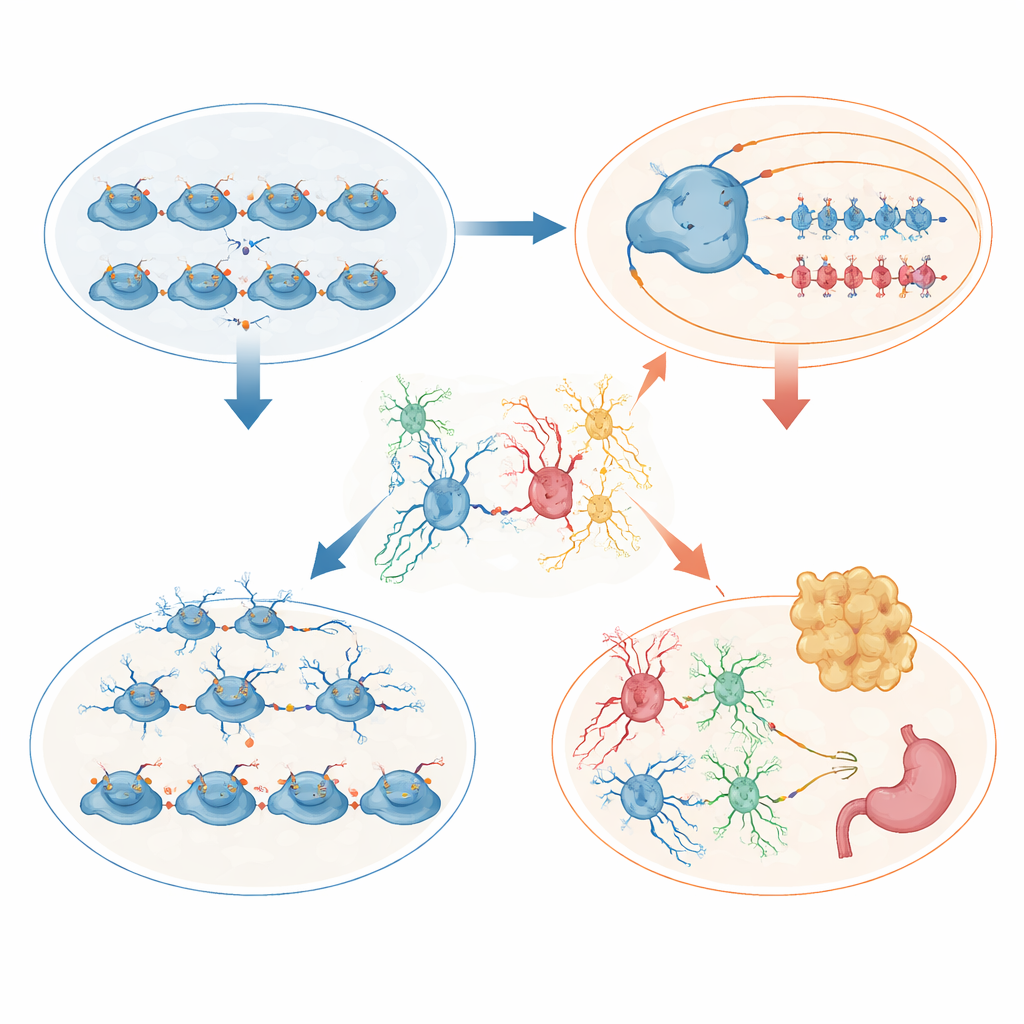
O hipotálamo contou uma história complementar centrada no crescimento corporal. Quando filhotes, os camundongos mutantes eram menores e uma fração substancial morreu cedo. Os sobreviventes, porém, mais tarde comeram mais, acumularam gordura e desenvolveram níveis elevados do hormônio leptina, sinalizando obesidade e provável resistência à leptina. A análise de célula única do hipotálamo embrionário revelou mais células progenitoras em divisão, mas menos células destinadas a núcleos-chave relacionados à alimentação, especialmente regiões que normalmente detectam o estado nutricional e regulam o hormônio do crescimento. No hipotálamo adulto, a mistura celular foi remodelada: astrócitos aumentaram acentuadamente, oligodendrócitos diminuíram, e células especializadas de barreira chamadas tanycitos e glia vizinha perderam sua arrumação ordenada na interface do cérebro com hormônios e nutrientes circulantes. Essas mudanças estruturais e na expressão gênica provavelmente distorcem como o cérebro percebe reservas de energia e controla o apetite.
Reverberações comportamentais de transtornos do neurodesenvolvimento humanos
O comportamento dos camundongos ecoou sintomas vistos em muitas condições do neurodesenvolvimento. Eles exibiram comportamento semelhante à ansiedade mais acentuado, marcha alterada, movimento espontâneo reduzido em casa e desempenho ruim em tarefas que testam memória, reconhecimento de objetos e filtragem de sons que assustam. Alguns testes revelaram ações mais impulsivas. Em várias medidas, fêmeas tendiam a ser mais severamente afetadas do que machos, sugerindo que sistemas hormonais sexuais e regulação gênica específicos por sexo podem interagir com marcas de histona para moldar a vulnerabilidade.
O que isso significa para a saúde humana
Em conjunto, os achados mostram que enfraquecer um conjunto de marcas de histona em apenas dois centros cerebrais embrionários é suficiente para reproduzir uma ampla constelação de problemas: menos “freios” inibitórios, redes cerebrais instáveis, convulsões, circuitos de alimentação perturbados e crescimento corporal anômalo. Para leigos, a mensagem chave é que marcas epigenéticas como a metilação de H3K4 não são adereços vagos, mas dials de controle precisos que ajudam as células cerebrais em desenvolvimento a se tornarem o tipo certo, no lugar certo, no momento certo. Quando esses dials são mal ajustados, como em muitas síndromes genéticas raras, o resultado pode ser uma combinação estreitamente ligada de sintomas cognitivos, comportamentais e metabólicos. Entender essas raízes compartilhadas pode, em última instância, orientar terapias que corrijam não apenas um sintoma, como convulsões ou obesidade, mas o sistema interconectado que lhes dá origem.
Citação: Li, J., Tanzillo, A.F., Pizzirusso, G. et al. Reducing methylation of histone 3.3 lysine 4 in the medial ganglionic eminence and hypothalamus recapitulates neurodevelopmental disorder phenotypes. Nat Commun 17, 2984 (2026). https://doi.org/10.1038/s41467-026-69248-9
Palavras-chave: epigenética, interneurônios, hipotálamo, convulsões, obesidade