Clear Sky Science · pt
Separar a separação de fases da fibrilização preserva a atividade de condensados biomoleculares
Por que isso importa para a saúde do cérebro
Muitas doenças cerebrais, incluindo o Alzheimer, envolvem proteínas que, com o tempo, se aglomeram em emaranhados rígidos e fibrosos. Essas mesmas proteínas também podem formar estruturas mais macias, em forma de gotícula, dentro das células que ajudam a organizar a química celular — algo como pequenas estações de trabalho líquidas. Este estudo faz uma pergunta crucial: podemos impedir que essas gotículas maléficas se endureçam em fibras sem destruir sua função útil do dia a dia? Os autores mostram que um metabólito celular comum, o aminoácido L-arginina, pode fazer exatamente isso para uma proteína-chave relacionada ao Alzheimer chamada Tau.
Do estado livre à formação de pequenas gotículas
Dentro das células, certas proteínas nem sempre permanecem bem misturadas no fluido interno. Em vez disso, elas podem se reunir em gotículas, chamadas condensados biomoleculares, que se comportam como géis muito macios ou líquidos espessos. A equipe concentrou-se na Tau, uma proteína que normalmente ajuda a construir e estabilizar microtúbulos — filamentos ocos que atuam como estradas dentro dos neurônios. A Tau também é famosa por formar fibrilas amiloides, as fibras rígidas encontradas nos emaranhados que marcam muitas doenças neurodegenerativas. Para estudar como as gotículas de Tau evoluem ao longo do tempo, os pesquisadores projetaram uma versão da proteína, denominada SynTag-Tau, que forma condensados ativos que envelhecem em fibrilas amiloides em uma escala de tempo experimentalmente conveniente, sem aditivos agressivos.
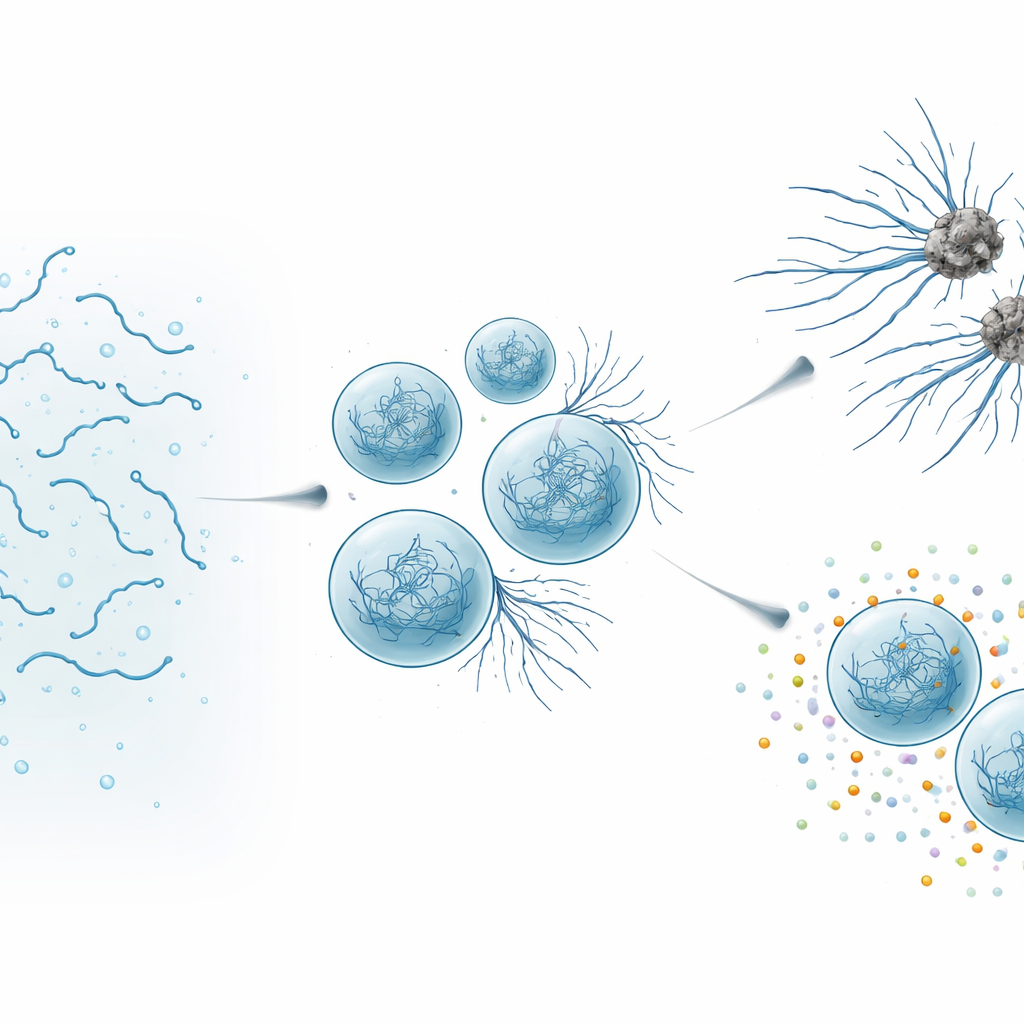
Quando gotículas úteis se tornam prejudiciais
Usando microscopia de alta resolução e medições biofísicas, os autores acompanharam as mudanças nas gotículas de SynTag-Tau ao longo de horas. Gotículas recentes se comportavam como líquidos: fundiam-se facilmente, suas moléculas moviam-se rapidamente e não havia sinal de estrutura ordenada. Com o tempo, as gotículas desaceleraram e enrijeceram, e fibras finas começaram a brotar de suas superfícies para a solução ao redor. Métodos ópticos sensíveis mostraram que essas fibras continham a arquitetura “cross–beta” fortemente empacotada típica do amiloide. Importante, a interface — a fronteira entre a gotícula densa e o fluido circundante — atuou como um ponto quente onde os fibrilos surgiram primeiro. À medida que as gotículas envelheceram e produziram mais fibras, a função normal da Tau foi prejudicada: os condensados tornaram-se piores em atrair tubulina, o bloco de construção dos microtúbulos, e eventualmente perderam totalmente a capacidade de suportar a montagem de microtúbulos.
Pequenas moléculas que inclinam o equilíbrio
Os pesquisadores então perguntaram se metabólitos simples poderiam retardar ou prevenir essa transição de líquido para fibra deixando as gotículas intactas. Ao rastrear várias pequenas moléculas naturais, eles descobriram que os aminoácidos positivamente carregados L-arginina e L-lisina retardaram fortemente ou bloquearam a formação de fibrilas amiloides a partir das gotículas de SynTag-Tau, sem interromper a formação de gotículas em concentrações realistas, na faixa de mili molar baixa. Em contraste, aminoácidos negativamente carregados como glutamato e aspartato aceleraram a formação de fibrilas, e químicos gerais que desorganizam proteínas ou não ajudaram ou perturbaram as próprias gotículas. Um análogo fluorescente da L-arginina revelou que essa molécula prefere se localizar dentro dos condensados de Tau em vez de fora, sugerindo que ela age onde é mais necessária.
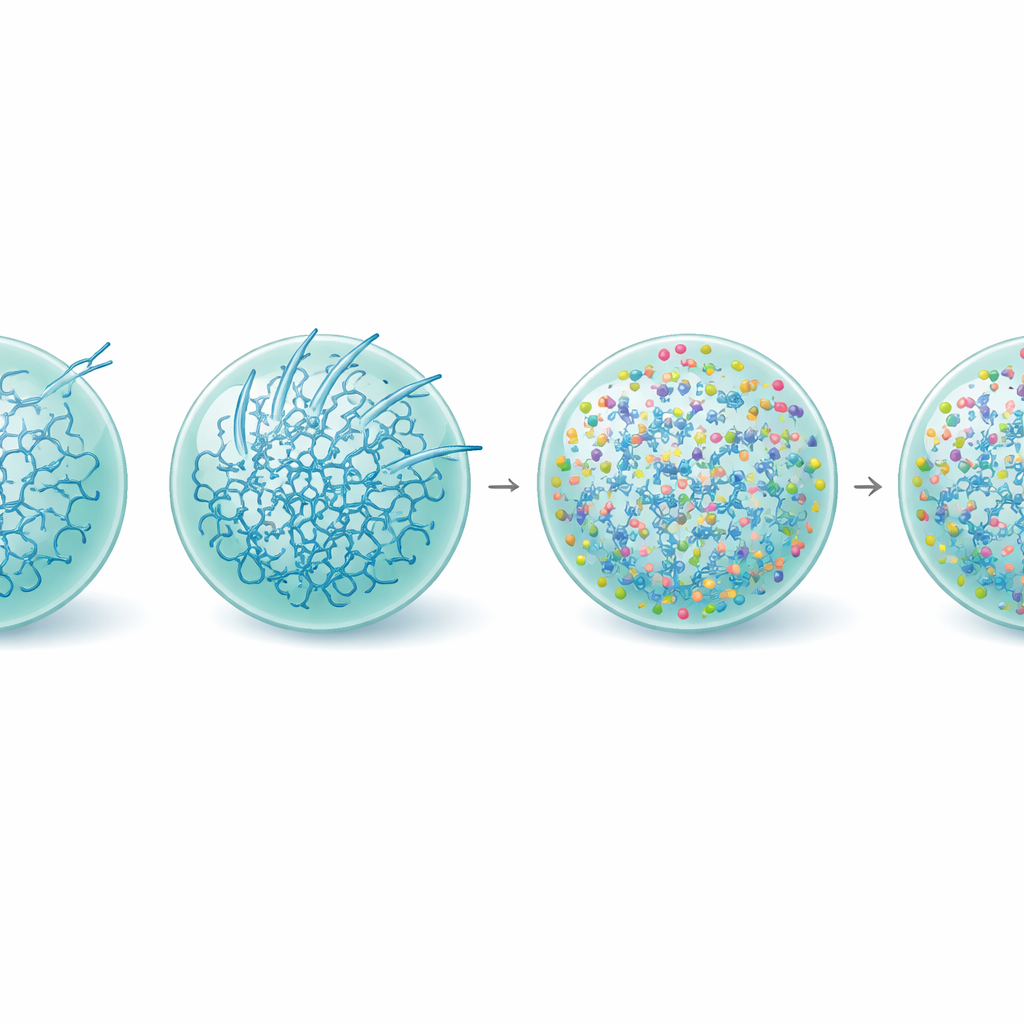
Endurecendo a gotícula, preservando a função
Aprofundando, a equipe examinou como a L-arginina remodela a vida interna das gotículas de Tau. Medições da estrutura proteica mostraram que, na presença de L-arginina, a fração de moléculas de Tau adotando formas rígidas ricas em beta, associadas ao amiloide, foi reduzida, mesmo em gotículas mais velhas. Nanorreologia baseada em vídeo — rastreando o movimento de pequenas partículas dentro dos condensados — revelou que a L-arginina na verdade tornou as gotículas de Tau mais viscoelásticas, o que significa que sua rede interna se tornou mais forte e mais interconectada, mantendo-se ainda com comportamento fluido. Esse fortalecimento parece manter o sistema em um estado metastável funcional e eleva a barreira energética para a formação de fibrilas, particularmente na superfície da gotícula. Em concordância com isso, condensados tratados com L-arginina continuaram a recrutar tubulina de maneira uniforme e suportaram o crescimento de microtúbulos muito depois de gotículas não tratadas terem se tornado inativas.
O que isso significa para terapias futuras
O trabalho demonstra que as forças que impulsionam a formação de gotículas proteicas e aquelas que impulsionam a formação de fibras prejudiciais são relacionadas, mas separáveis. Ao ajustar a química interna dos condensados com um metabólito como a L-arginina, é possível preservar o estado benéfico e semelhante a líquido enquanto se retarda ou evita a transição para fibras amiloides associadas à doença. Embora este estudo utilize um sistema Tau especialmente projetado in vitro, ele oferece uma prova de princípio: pequenas moléculas que reforcem seletivamente a estabilidade dos condensados podem, um dia, ajudar a proteger as células do acúmulo gradual de agregados proteicos tóxicos sem bloquear os papéis organizadores normais dos condensados biomoleculares.
Citação: Mahendran, T.S., Singh, A., Srinivasan, S. et al. Decoupling phase separation and fibrillization preserves activity of biomolecular condensates. Nat Commun 17, 2841 (2026). https://doi.org/10.1038/s41467-026-69244-z
Palavras-chave: Proteína Tau, condensados biomoleculares, fibrilas amiloides, L-arginina, neurodegeneração