Clear Sky Science · pt
Variantes de FOXJ3 associadas à epilepsia ligam um programa transcricional da via PTEN-mTOR à especificação neuronal e à laminação cortical
Quando a fiação cerebral sai ligeiramente do curso
A epilepsia frequentemente começa na infância, mas em muitos pacientes jovens os médicos não identificam nada óbvio nas imagens cerebrais. Este estudo investiga uma causa oculta: pequenas alterações em um gene chamado FOXJ3 que, silenciosamente, remodelam como a camada externa do cérebro, o córtex, é construída. Ao acompanhar a ação desse gene em famílias com epilepsia focal e em cérebros de camundongos em desenvolvimento, os pesquisadores mostram como erros precoces na geração, no deslocamento e na laminação das células podem eventualmente dar origem a convulsões.
Uma malformação sutil por trás de convulsões resistentes
Muitas crianças com epilepsia focal resistente a medicamentos possuem uma condição chamada displasia cortical focal (DCF), na qual áreas do córtex ficam malformadas. Essas regiões contêm neurônios deslocados e anormalmente grandes e são uma razão comum pela qual os remédios falham em controlar as crises. Ainda assim, a causa molecular da DCF frequentemente é desconhecida, e a ressonância magnética padrão pode não detectar defeitos pequenos ou superficiais. Os autores começaram por uma família em que vários membros tinham epilepsia focal e evidência de DCF. Uma análise genômica cuidadosa apontou para variações raras em FOXJ3, um gene ainda não associado à epilepsia. Casos adicionais em grandes bancos de dados genéticos revelaram mais indivíduos com variantes incomuns de FOXJ3 e convulsões focais, sugerindo que esse gene pode ser um ator recorrente nesses transtornos.
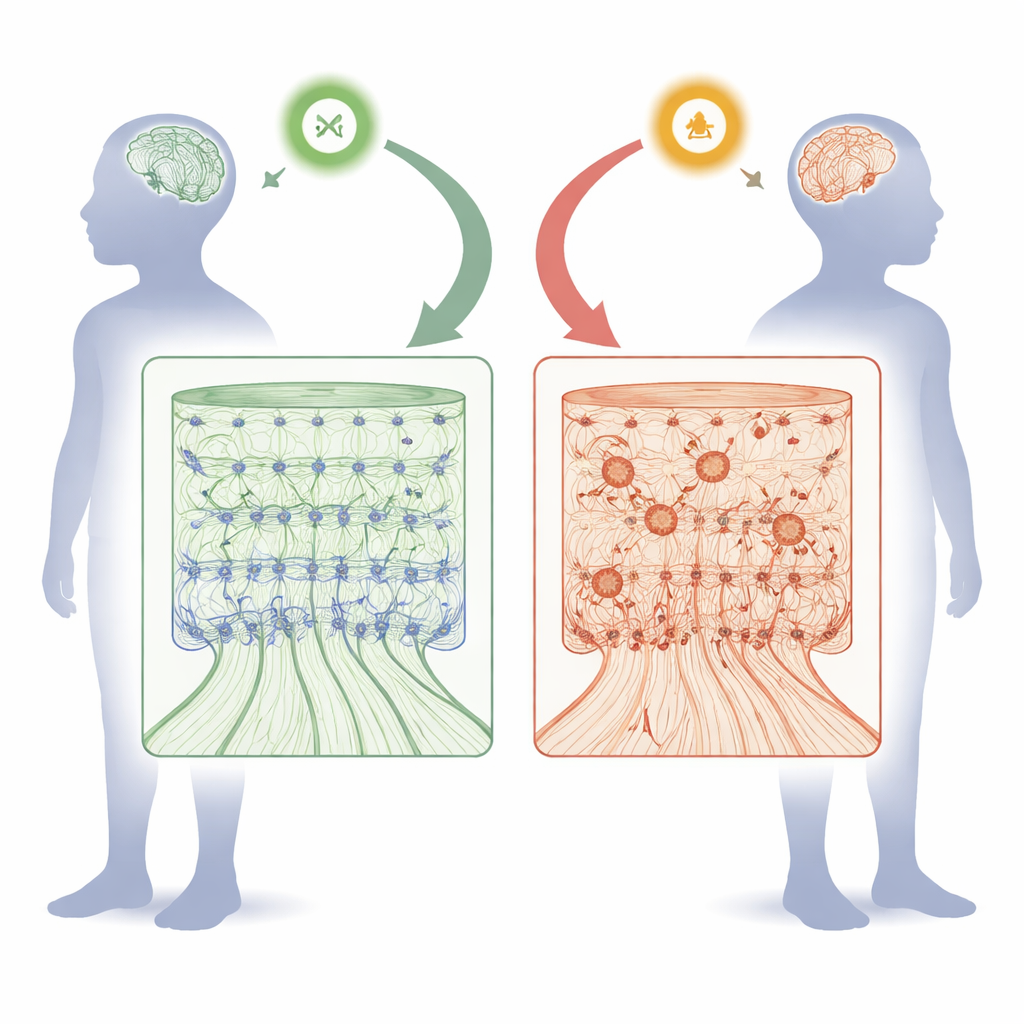
Como o FOXJ3 ajuda a moldar a superfície pensante do cérebro
Durante o desenvolvimento fetal, o córtex é montado como um edifício de muitos andares. Células progenitoras semelhantes a células-tronco que revestem a superfície interna do cérebro se dividem e depois enviam neurônios recém-nascidos para fora ao longo de “andaimes” radiais para formar seis camadas ordenadas. A equipe descobriu que FOXJ3 está ativo tanto nesses progenitores quanto em neurônios jovens, mas sua atividade nos progenitores diminui naturalmente após um ponto específico na metade da gestação. Usando ferramentas de silenciamento gênico em embriões de camundongo, os pesquisadores reduziram os níveis de Foxj3 em diferentes estágios e observaram o que acontecia. A perda precoce de Foxj3 fez com que os neurônios recém-formados migrassem mais lentamente e se estabelecessem nas camadas erradas. Células que deveriam se tornar neurônios de camadas profundas passaram a adotar identidades típicas de camadas superiores, e neurônios de projeção calosa, que conectam os dois hemisférios, foram produzidos em excesso. Já em estágios mais tardios do desenvolvimento, reduzir Foxj3 teve efeitos muito mais leves, mostrando que seu papel é altamente sensível ao tempo.
Mantendo o equilíbrio entre divisão celular e crescimento
Para entender por que FOXJ3 tem tanta influência, os pesquisadores combinaram várias abordagens em larga escala. Eles mapearam onde FOXJ3 se liga ao DNA e quais genes estão ativos em milhares de células corticais individuais. Isso apontou fortemente para genes que regulam o ciclo celular e o crescimento cerebral, em especial PTEN, um importante freio numa via de crescimento conhecida como mTOR. Em células progenitoras, a ligação de FOXJ3 aumentava a atividade de PTEN, o que por sua vez ajudava as células a saírem do ciclo de divisão, se transformarem em neurônios e migrarem para fora de maneira ordenada. Quando Foxj3 foi reduzido, mais progenitores permaneceram em estado de divisão, menos saíram do ciclo no tempo certo, e a migração estagnou em zonas intermediárias. Crucialmente, restaurar os níveis de PTEN em cérebros deficientes em Foxj3 reverteu em grande parte os problemas de migração, laminação e destino celular, enquanto aumentar outro regulador de crescimento, TSC1, não teve o mesmo efeito. Isso coloca PTEN no centro do controle que FOXJ3 exerce sobre a construção cortical.
De vias desreguladas a neurônios aumentados
A equipe, em seguida, investigou como variantes de FOXJ3 semelhantes às de pacientes se comportam. Uma versão associada à doença não conseguiu elevar os níveis de PTEN e permitiu que a via mTOR ficasse hiperativa, como visto pelo aumento da fosforilação de uma proteína-chave relacionada ao crescimento. Em camundongos adolescentes projetados para expressar essa forma mutante no córtex em desenvolvimento, os neurônios mais tarde apresentaram-se visivelmente inchados, com corpos e perímetros celulares maiores, imitando as células dismórficas observadas na DCF humana. Ainda assim, a proteína mutante ainda alcançava o núcleo corretamente, indicando que o problema está na regulação gênica defeituosa, não na má localização. Juntos, esses achados ligam mutações em FOXJ3 a uma cascata de eventos — menos PTEN, mais sinalização mTOR, saída tardia do ciclo celular, migração desordenada e neurônios hipertrofiados — que podem preparar o terreno para redes epilépticas.
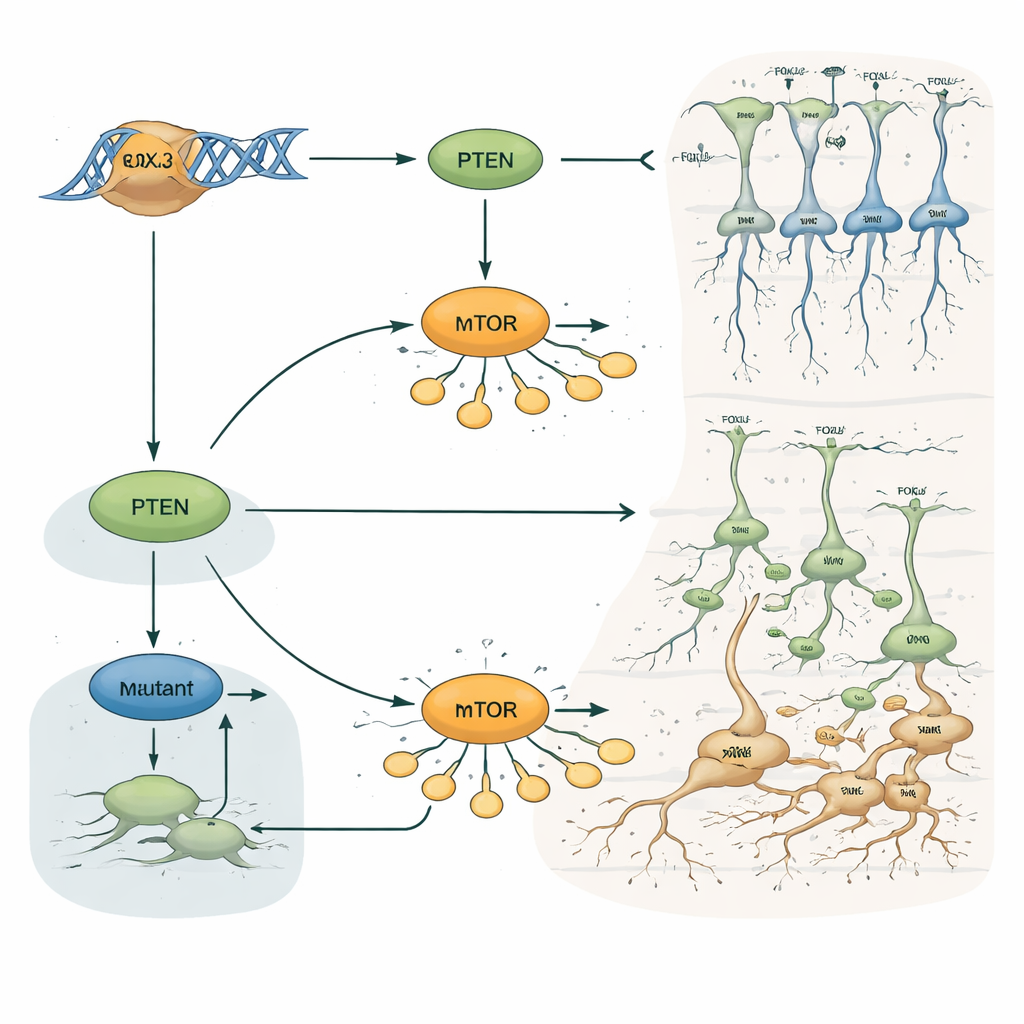
Por que isso importa para epilepsia e lesões cerebrais ocultas
Para um público não especialista, a mensagem principal é que um único fator de transcrição, FOXJ3, ajuda a decidir quando e onde os neurônios corticais nascem, como se deslocam e em qual camada acabam. Ao agir através da via de crescimento PTEN–mTOR, FOXJ3 mantém a construção cerebral no cronograma. Alterações raras nesse gene podem desequilibrar esse processo, causando pequenos fragmentos de córtex com conexão e laminação incorretas, mesmo quando as ressonâncias magnéticas parecem normais. Este trabalho não só propõe FOXJ3 como uma nova causa genética de displasia cortical focal e epilepsia, como também ilustra como mudanças sutis no desenvolvimento cerebral precoce podem repercutir décadas depois como convulsões de difícil tratamento.
Citação: Cheng, HY., Liu, C., Nien, CW. et al. Epilepsy-associated FOXJ3 variants link a transcriptional program of the PTEN-mTOR pathway to neuronal specification and cortical lamination. Nat Commun 17, 1815 (2026). https://doi.org/10.1038/s41467-026-69241-2
Palavras-chave: displasia cortical focal, gene FOXJ3, via PTEN mTOR, desenvolvimento cortical, epilepsia focal