Clear Sky Science · pt
Armazenamento de sódio aprimorado em carbono duro via eletrólito de co-intercalação de solvente permitindo células pouch de nível Ah em baixas temperaturas
Por que baterias à prova de frio importam
De carros elétricos em climas nevados a sensores no Ártico profundo, muitos dispositivos modernos precisam de baterias que continuem funcionando no frio. As baterias de lítio e de sódio atuais frequentemente perdem potência ou falham completamente em temperaturas muito baixas porque sua química interna desacelera. Este estudo explora uma nova forma de construir baterias de íons de sódio — usando um líquido especialmente formulado dentro da bateria — para que elas possam armazenar e fornecer energia de maneira confiável mesmo a temperaturas de até −50 °C.
O desafio das baterias que congelam
As baterias armazenam energia deslocando átomos carregados, chamados íons, entre dois eletrodos sólidos através de um eletrólito líquido. Em baterias de íons de sódio, os íons de sódio precisam atravessar uma fina película superficial e entrar em um eletrodo negativo à base de carbono conhecido como carbono duro. Em baixas temperaturas, duas coisas dão errado: os íons movem‑se mais lentamente pelo líquido e têm dificuldade em perder as moléculas de solvente que os cercam antes de entrar no carbono duro. Ao mesmo tempo, a película protetora — chamada de interfase sólida do eletrólito — tende a ficar mais espessa e mais resistiva no frio. Tudo isso torna mais difícil o movimento dos íons de sódio, de modo que a bateria entrega bem menos energia quando ela é mais necessária.
Uma nova mistura líquida para facilitar a viagem dos íons
Os pesquisadores enfrentaram esse problema redesenhando o eletrólito para que os íons de sódio não precisem mais desprender completamente sua camada de solvente antes de entrar no carbono duro. Eles misturaram dois solventes à base de éter: dietilenoglicol dimetil éter (G2), que se liga firmemente aos íons de sódio e favorece o movimento rápido dos íons, e 2-metiloxolano (MO), um líquido menos polar que permanece fluido em temperaturas muito baixas. No eletrólito resultante de “co-intercalação”, os íons de sódio coordenam-se principalmente com o G2, enquanto o MO atua em grande parte como um solvente livre, não ligante, que ajuda a manter a mistura líquida até −50 °C. Simulações por computador e medições espectroscópicas mostraram que essa mistura forma uma estrutura estável em que os íons de sódio e o G2 viajam juntos como um pequeno aglomerado.
Perguntando os íons a entrar no carbono sem se despir
Em vez de forçar os íons de sódio a perderem sua camada de solvente na superfície do eletrodo, o novo eletrólito permite que os aglomerados sódio–G2 deslizem diretamente através da película superficial e entrem nos espaços em camadas do carbono duro. Esse processo, chamado co-intercalação de solvente, contorna a lenta etapa de “despir” que normalmente limita o desempenho no frio. Testes microscópicos e espectroscópicos revelaram que a película formada com este eletrólito é mais fina e mais rica em compostos inorgânicos do que em sistemas convencionais. Essa combinação protege o eletrodo ao mesmo tempo em que permite a rápida passagem dos íons. Medições de difusão iônica e resistência elétrica confirmaram que os íons movem‑se mais rápido dentro do carbono e através da interface, especialmente em baixas temperaturas.
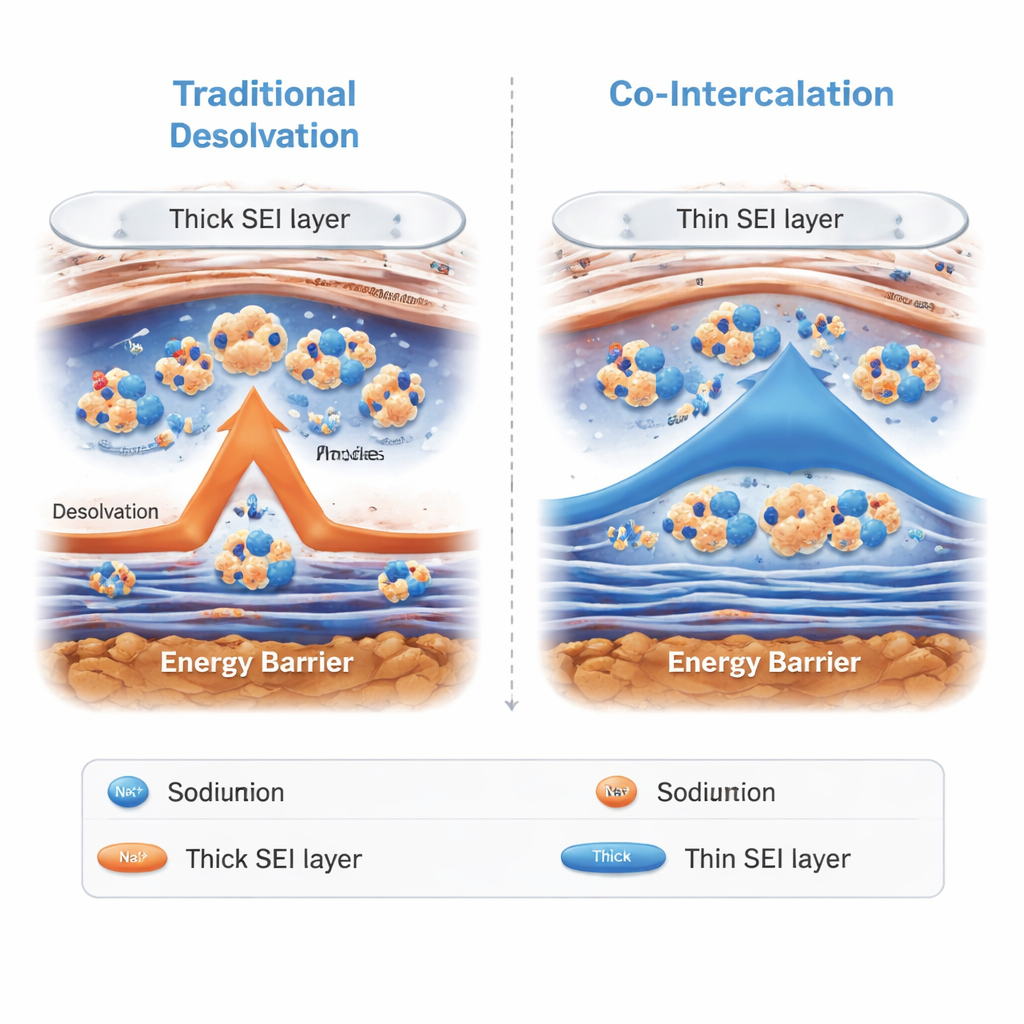
Desempenho forte mesmo a −50 °C
Quando a equipe testou células do tipo coin usando carbono duro e o novo eletrólito, verificaram que as baterias mantiveram alta capacidade e eficiência desde a temperatura ambiente até −50 °C. A −50 °C, o eletrodo de carbono duro ainda apresentava cerca de 80% de sua eficiência de carga inicial e manteve mais de 90% da capacidade após 200 ciclos de carga e descarga. Indo além das células pequenas, os pesquisadores construíram células pouch — baterias planas semelhantes às usadas em eletrônicos de consumo — com capacidade de cerca de 1,2 ampere-hora. Essas baterias completas de íons de sódio atingiram uma densidade de energia específica de 163 watt-hora por quilograma à temperatura ambiente e 107 watt-hora por quilograma a −50 °C, enquanto continuavam a alimentar lâmpadas LED por mais de 10 horas em uma câmara a −50 °C.
O que isso significa para baterias em futuros climas frios
Para não especialistas, a mensagem principal é que os autores encontraram uma forma de permitir que os íons de sódio mantenham seu revestimento de solvente útil ao entrar no eletrodo de carbono da bateria. Ao formular um eletrólito que permanece líquido no frio e forma uma película superficial fina e favorável aos íons, eles eliminaram um grande gargalo no desempenho em baixas temperaturas. Essa abordagem pode ajudar a tornar as baterias de íons de sódio — uma alternativa mais barata às de íons de lítio — mais práticas para uso em climas de inverno, regiões de alta altitude e outros ambientes severos onde armazenamento de energia confiável e acessível é urgentemente necessário.
Citação: Li, M., Liu, Z., Zhao, Y. et al. Enhanced sodium storage in hard carbon via solvent co-intercalation electrolyte enabling Ah-level pouch cells at low temperatures. Nat Commun 17, 1478 (2026). https://doi.org/10.1038/s41467-026-69237-y
Palavras-chave: baterias de íons de sódio, baterias para baixas temperaturas, projeto de eletrólito, armazenamento de energia