Clear Sky Science · pt
Base molecular da galactosilação do colágeno pela GLT25D1
Como pequenas etiquetas de açúcar ajudam a construir tecidos resistentes
O colágeno é a proteína mais comum do corpo, formando a estrutura da pele, ossos, vasos sanguíneos e muitos outros tecidos. Mas o colágeno não atua sozinho: ele precisa ser decorado com pequenas moléculas de açúcar em pontos precisos para adquirir a resistência e flexibilidade adequadas. Este estudo revela, em detalhe atômico, como uma enzima-chave, a GLT25D1, anexa um açúcar específico ao colágeno e como falhas nesse processo podem levar a vasos frágeis, problemas musculares e possivelmente até câncer.
Um olhar mais atento à transformação oculta do colágeno
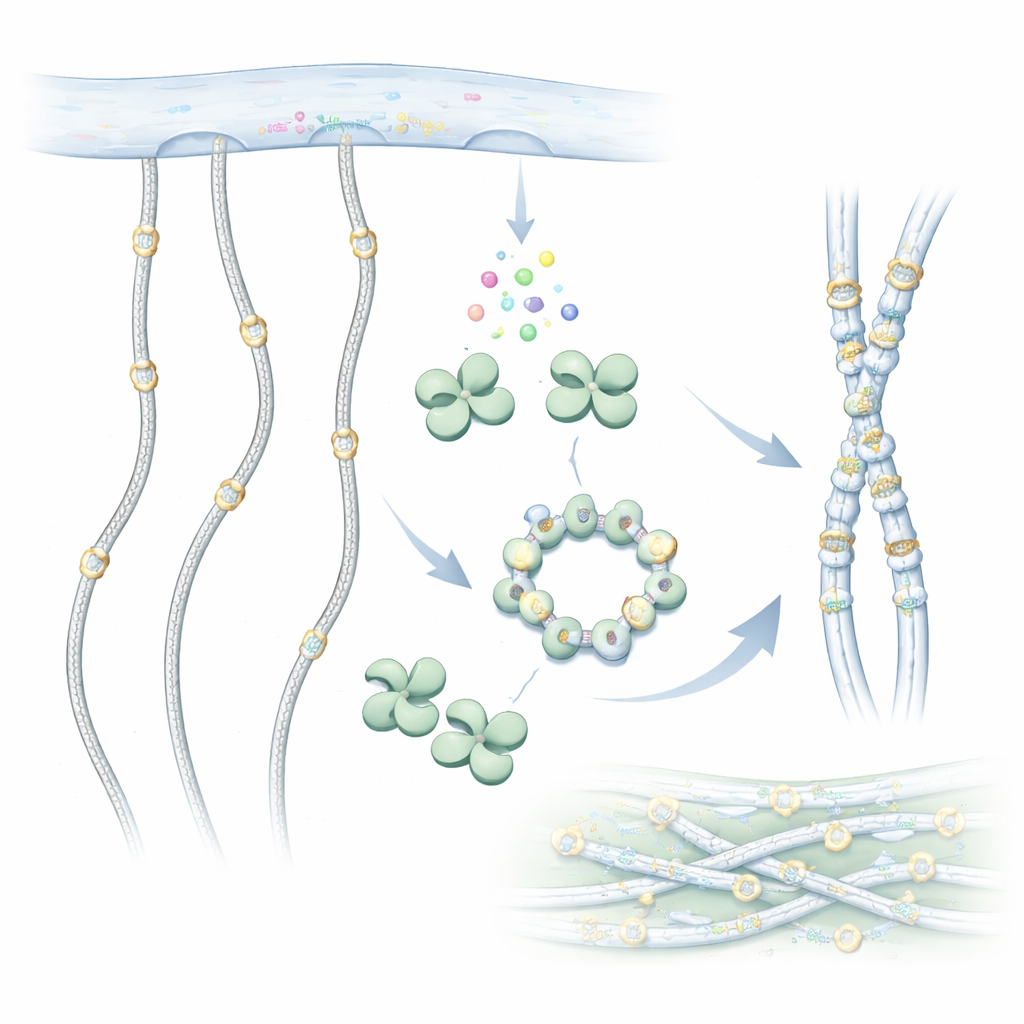
As moléculas de colágeno são cadeias longas e semelhantes a cordas que se organizam em fibras resistentes fora das células. Antes de saírem da célula, no entanto, elas são quimicamente editadas. Uma edição importante é a adição de grupos de açúcar a blocos de construção especiais chamados hidroxilisinas ao longo da cadeia de colágeno. A GLT25D1 realiza o primeiro passo nessa marcação por açúcar, transferindo uma galactose de uma molécula doadora para a hidroxilisina. Essa decoração por açúcar é conservada desde animais simples até humanos e ajuda o colágeno a se dobrar corretamente, interagir com células e resistir ao desgaste.
Revelando a forma de um decorador do colágeno
Para entender como a GLT25D1 funciona, os pesquisadores usaram microscopia crioeletrônica para imagear a enzima humana em resolução quase atômica. Eles descobriram que cada molécula de GLT25D1 possui dois lóbulos semelhantes, ambos relacionados a um dobramento enzimático comum observado em proteínas transferidoras de açúcares. Esses lóbulos emparelham-se para formar dímeros alongados, e três dímeros podem se montar adicionalmente em um hexâmero com formato de anel. Nesses arranjos, os verdadeiros operários — os centros catalíticos — ficam bem distantes entre si, um arranjo que pode permitir que vários sítios de adição de açúcar atuem ao longo de uma cadeia de colágeno esticada ao mesmo tempo.
As partes funcionais: onde a transferência de açúcar realmente acontece
A equipe resolveu estruturas da GLT25D1 ligada tanto ao seu doador de açúcar quanto a um peptídeo curto semelhante ao colágeno contendo hidroxilisina. Esse complexo ternário mostrou que apenas o segundo lobo, chamado domínio C‑terminal, executa efetivamente a química. Ali, a molécula doadora se acomoda em um bolso estabilizado por um íon metálico, enquanto o peptídeo se posiciona em um sulco estreito que impõe um padrão local específico: uma hidroxilisina seguida imediatamente por uma pequena glicina. Um único resíduo de ácido aspártico atua como base química, ativando o grupo hidroxila da hidroxilisina para que ele possa atacar o açúcar e completar a transferência. Alterações em qualquer um desses aminoácidos-chave reduzem drasticamente ou abolam a atividade, confirmando seus papéis essenciais.
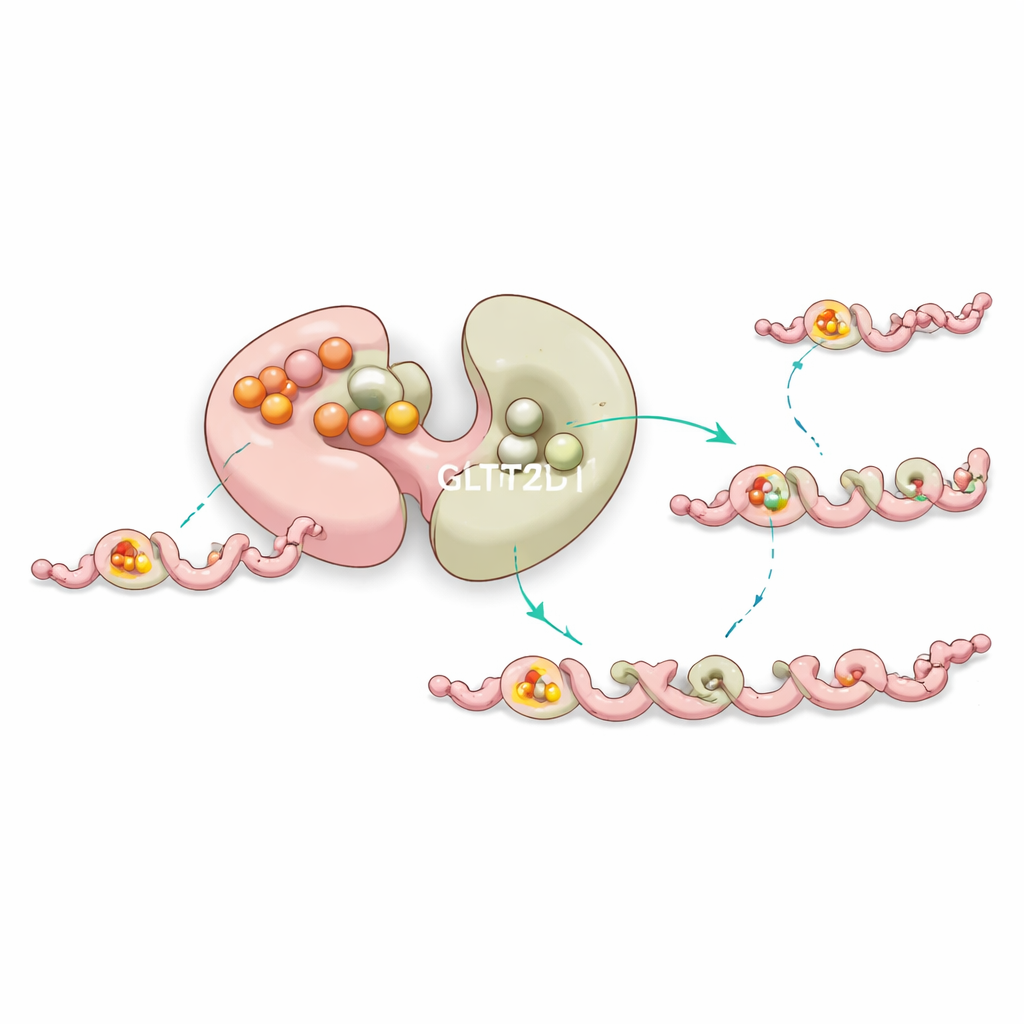
Um estabilizador incorporado e controle à distância
Curiosamente, o primeiro lobo da GLT25D1 liga um doador de açúcar muito firmemente, mas não realiza a transferência. Em vez disso, experimentos e simulações por computador sugerem que esse sítio “silencioso” ajuda a estabilizar a enzima e ajusta sutilmente o comportamento do lobo ativo por meio de comunicação de longo alcance dentro da proteína. Mutações próximas a esse bolso não catalítico frequentemente desestabilizam a enzima ou alteram sua eficiência, sugerindo que a natureza usa esse sítio de ligação extra como uma forma de controle de qualidade interno para manter a modificação do colágeno funcionando sem problemas.
Quando o decorador falha: conexões com doenças
Ao mapear mutações derivadas de pacientes em seu modelo estrutural, os autores puderam explicar como erros na GLT25D1 levam a doenças humanas. Algumas mutações removem completamente o lobo catalítico, outras desestabilizam o núcleo da proteína e outras atacam diretamente os sítios de ligação ao açúcar ou ao colágeno. Essas falhas reduzem ou eliminam a adição de açúcar ao colágeno e têm sido associadas a doenças dos pequenos vasos cerebrais, problemas cognitivos e defeitos musculares e esqueléticos. Mutações associadas ao câncer também se agrupam em regiões cruciais, sugerindo que a decoração alterada do colágeno pode influenciar o crescimento e a disseminação tumoral.
Por que isso importa para a saúde e tratamentos futuros
Ao apresentar um roteiro tridimensional detalhado da GLT25D1 em ação, este trabalho explica como etiquetas de açúcar precisas são adicionadas ao colágeno e por que essa etapa é tão importante para a integridade dos tecidos. Para não especialistas, a mensagem principal é que pequenas mudanças químicas no colágeno podem ter efeitos desproporcionais sobre vasos sanguíneos, ossos e possivelmente no risco de câncer. O mapa estrutural da GLT25D1 agora oferece um guia para diagnosticar variantes prejudiciais e para projetar terapias — seja com pequenas moléculas que estabilizem enzimas defeituosas ou estratégias baseadas em genes — que um dia possam corrigir os defeitos na marcação por açúcar do colágeno em sua origem.
Citação: Sun, H., Zhang, M., Shi, Y. et al. Molecular basis of collagen galactosylation by GLT25D1. Nat Commun 17, 2426 (2026). https://doi.org/10.1038/s41467-026-69234-1
Palavras-chave: glicosilação do colágeno, GLT25D1, matriz extracelular, doença vascular, estrutura por crio‑ME