Clear Sky Science · pt
Deficiência de esclerostina sensibiliza adipócitos brancos a sinais termogênicos que induzem o surgimento de tecido bege em camundongos
Por que aquecer sua gordura pode resfriar doenças
A maioria de nós pensa em osso e tecido adiposo como mundos separados: um nos dá estrutura, o outro armazena energia. Este estudo em camundongos revela que osso e gordura mantêm uma conversa química constante, e que uma proteína produzida por células ósseas pode decidir se nossa gordura “branca” apenas armazena calorias ou se se transforma em gordura “bege” mais ativa, que queima calorias. Entender esse diálogo oculto pode abrir novas vias para combater obesidade, diabetes e perda óssea ao mesmo tempo.
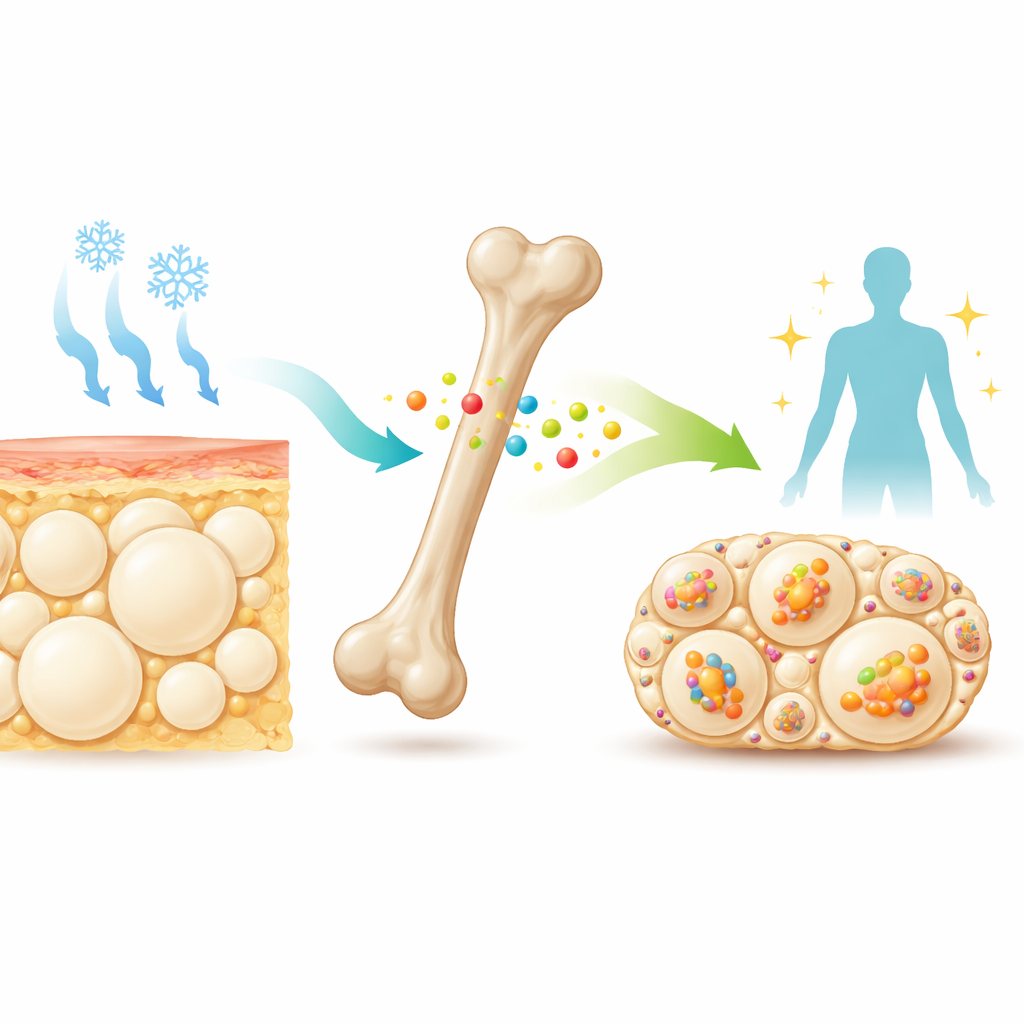
Um mensageiro silencioso do osso
No interior dos ossos, células especializadas liberam uma pequena proteína chamada esclerostina na corrente sanguínea. Médicos já direcionam a esclerostina com medicamentos para fortalecer o osso em pacientes com risco de fraturas. Trabalhos anteriores mostraram que camundongos sem esclerostina não são apenas mais fortes, mas também mais magros e mais sensíveis à insulina. Sua gordura subcutânea, especialmente ao redor dos quadris (gordura inguinal branca), contém pequenas células adiposas com várias compartimentações que lembram gordura bege, capaz de queimar combustível para produzir calor. Essas pistas levaram os pesquisadores a perguntar se a esclerostina normalmente atua como um freio à capacidade do corpo de converter gordura branca em bege quando exposto ao frio ou a fármacos que imitam sinais nervosos para a gordura.
Sinais de frio, sinais do osso e ignição da gordura
A equipe expôs camundongos normais e camundongos sem o gene da esclerostina (Sost-/-) a um fármaco que ativa um receptor específico nas células adiposas (receptor β3-adrenérgico) ou a frio leve. Em animais normais, esses sinais termogênicos aumentaram a produção de esclerostina no osso e elevaram seu nível no sangue. Esse aumento foi associado à perda de osso trabecular, mas apenas a mudanças modestas na gordura subcutânea. Em contraste, camundongos deficientes em esclerostina exibiram uma resposta muito mais intensa: sua gordura inguinal captou mais glicose, liberou mais ácidos graxos, diminuiu de tamanho e encheu-se de células semelhantes à gordura bege, repletas de mitocôndrias, as usinas celulares. Genes termogênicos-chave foram ativados mais fortemente nesses animais, especialmente na gordura subcutânea, enquanto a clássica gordura marrom permaneceu em grande parte inalterada.
Ajustando a queima de gordura por meio de um interruptor compartilhado
Para entender como a esclerostina exerce esse controle, os pesquisadores concentraram-se na β-catenina, uma proteína envolvida na via de sinalização Wnt que a esclerostina normalmente suprime no osso. Na gordura, ativar a β-catenina após o nascimento direcionou as células brancas a um estado semelhante ao bege e aumentou sua resposta aos sinais β3-adrenérgicos, mas esse efeito desapareceu quando os camundongos foram mantidos em temperatura neutra termicamente, onde o corpo não precisa de calor extra. Por outro lado, deletar a β-catenina especificamente nas células adiposas de camundongos deficientes em esclerostina eliminou sua gordura bege, restaurou células brancas maiores e reverteu as melhorias em insulina e níveis de ácidos graxos. Esses experimentos sugerem que, quando a esclerostina está baixa, a β-catenina nas células adiposas se torna uma alavanca interna importante que torna a gordura branca mais responsiva aos sinais termogênicos.
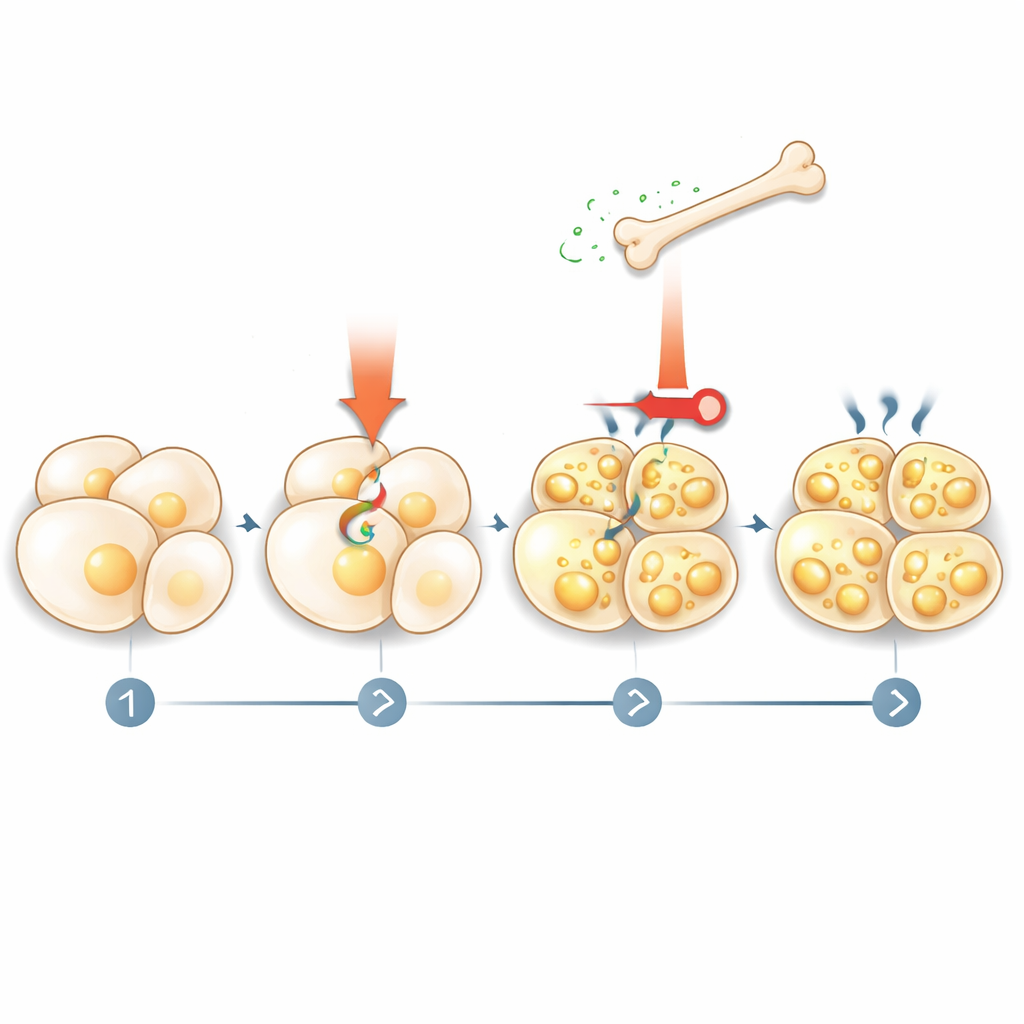
Como a gordura responde ao osso
A história não terminou com o osso dizendo à gordura o que fazer. A equipe descobriu que a estimulação termogênica ativa a quebra de gordura (lipólise), liberando ácidos graxos na circulação. Esses ácidos graxos, por sua vez, atuam nas células ósseas por meio de um receptor nuclear chamado PPARγ, aumentando a produção de esclerostina. Quando os pesquisadores bloquearam a lipólise nas células adiposas ou removeram o PPARγ das células ósseas, fármacos que imitam o frio não conseguiram mais elevar os níveis de esclerostina. Isso revela um circuito de retroalimentação: sinais termogênicos fazem a gordura liberar combustível, esse combustível instrui o osso a secretar mais esclerostina, e a esclerostina então retroalimenta para conter mais ativação e o surgimento de tecido bege.
Associando medicamentos para osso e gordura em prol da saúde metabólica
Por fim, os pesquisadores testaram se interromper esse circuito poderia ajudar em um contexto semelhante a doença. Camundongos obesos em dieta rica em gordura receberam uma baixa dose de mirabegron (um fármaco β3-adrenérgico já usado para problemas da bexiga), um anticorpo que neutraliza a esclerostina (romosozumabe, aprovado para osteoporose) ou ambos. Embora cada fármaco isoladamente tenha efeitos modestos, a combinação reduziu a massa de gordura em depósitos-chave, deslocou a gordura para células menores e mais ativas, diminuiu insulina, triglicerídeos e colesterol, e preservou a resistência óssea. A manutenção em ambiente aquecido, que reduz a necessidade de calor do corpo, apagou em grande parte os benefícios metabólicos da perda de esclerostina, ressaltando que essa via é mais relevante quando sinais termogênicos estão presentes.
O que isso significa para futuros tratamentos
Em termos simples, este trabalho mostra que o osso não é apenas um andaime passivo, mas um regulador ativo de quanto combustível as células adiposas gastam. A esclerostina funciona como um botão de volume que mantém a atividade da gordura termogênica, e portanto o uso de combustível, sob controle. Diminuir esse botão — por genética ou por fármacos — torna certos depósitos de gordura branca mais propensos a mudar para um modo produtor de calor quando o corpo é estimulado pelo frio ou por medicamentos específicos. Como a mesma intervenção pode fortalecer os ossos e melhorar a saúde metabólica em camundongos, combinações cuidadosamente desenhadas de terapias direcionadas ao osso e à gordura podem um dia ajudar a tratar obesidade, diabetes e osteoporose juntos, em vez de uma doença por vez.
Citação: Choquette, G.M., Kim, S.P., Wilkinson, K.J. et al. Sclerostin deficiency sensitizes white adipocytes to thermogenic signals that induce beiging in mice. Nat Commun 17, 2394 (2026). https://doi.org/10.1038/s41467-026-69227-0
Palavras-chave: esclerostina, gordura bege, comunicação osso–gordura, termogênese, doença metabólica