Clear Sky Science · pt
Síntese local de PI(4,5)P2 por isoformas associadas a septina de PIPKIγ controla a associação do centralspindlin com o corpúsculo médio durante a citocinese
Como as Células Concluem a Separação em Duas
A citocinese — o aperto final que divide uma célula em duas — é fácil de tomar como certa, mas quando falha pode contribuir para o desenvolvimento do câncer e de outras doenças. Este estudo revela como um conjunto específico de moléculas atua como capatazes de obra na estreita ponte que conecta duas células recém-formadas, garantindo que a separação seja concluída de maneira limpa em vez de retroceder ou parar.
A Ponte Final entre as Células Filhas
Após a duplicação do material genético e a separação dos cromossomos, a célula precisa se dividir fisicamente. Um anel contrátil de filamentos proteicos se contrai ao redor do centro da célula, formando uma ranhura profunda chamada sulco de clivagem. À medida que esse sulco se fecha para dentro, as duas células filhas permanecem ligadas por uma ponte intercelular fina que contém um núcleo denso, o corpúsculo médio. O corpúsculo médio é uma estrutura pequena, porém complexa, composta por microtúbulos agrupados, proteínas de andaime e lipídios sinalizadores; ele atua tanto como um vínculo quanto como um centro de controle que coordena os passos finais da divisão e o corte definitivo entre as células. 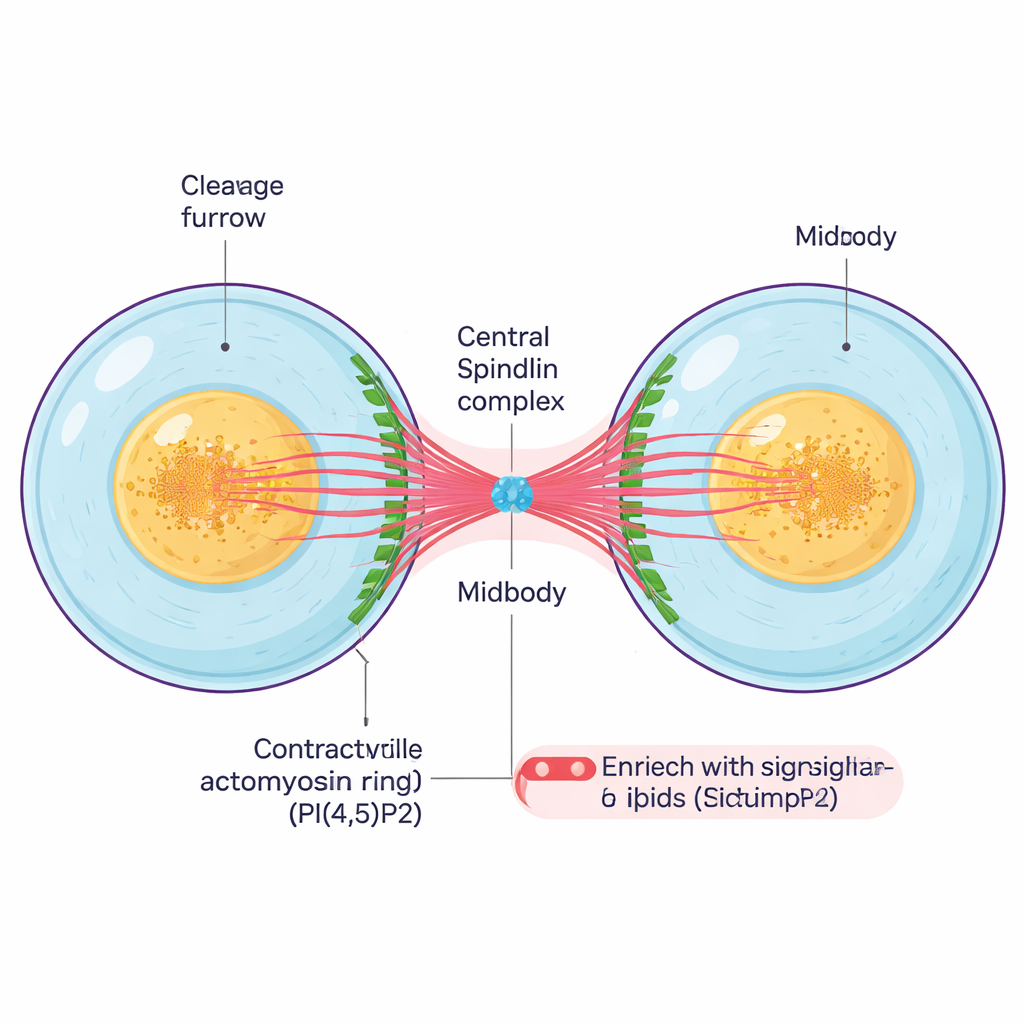
Um Sinal Lipídico que Deve Estar no Lugar Certo
Um ator-chave nesse processo é uma molécula lipídica sinalizadora na membrana celular chamada PI(4,5)P2. Esse lipídio ajuda a ancorar muitas proteínas que constroem e contraem o anel contrátil e estabilizam a ponte. O enigma era como as células controlam onde e quando o PI(4,5)P2 aparece, dado que ele pode se difundir na membrana. Os autores focaram em enzimas chamadas quinases PIP tipo I, que sintetizam PI(4,5)P2, e em particular em um gene, PIPKIγ, que existe em várias formas alternativas de splicing. Ao reduzir seletivamente cada quinase em células humanas e observar os efeitos com microscopia avançada, eles descobriram que o PIPKIγ tem um papel especial no final da citocinese, quando a ponte e o corpúsculo médio estão se formando, mesmo sem alterar fortemente os níveis globais de PI(4,5)P2 na superfície celular.
Andaimes de Septina Recrutam uma Enzima Especializada
A equipe descobriu que duas versões de splicing do PIPKIγ, chamadas i3 e i5, atuam como ferramentas de precisão que são levadas ao local correto por proteínas estruturais conhecidas como septinas. As septinas formam filamentos e anéis que ajudam a moldar a ponte e a organizar outros componentes. Experimentos bioquímicos de pull-down e imagens celulares mostraram que PIPKIγ-i3 e PIPKIγ-i5 se ligam fisicamente a complexos de septina e decoram filamentos de septina, enquanto outras variantes de PIPKIγ não o fazem. Quando os pesquisadores mutaram dois aminoácidos específicos nesses trechos de splicing, as enzimas perderam a capacidade de se ligar às septinas. Em células em divisão, o PIPKIγ-i3/i5 normal migra de um padrão difuso na membrana para se concentrar no sulco de clivagem e então contornar a ponte intercelular e o corpúsculo médio em sincronia com as septinas e outra proteína de andaime, a anilina. Remover apenas as variantes i3 e i5 espalhou a anilina e as septinas ao longo da ponte, afastando-as do corpúsculo médio, e muitas células falharam na citocinese, terminando com múltiplos núcleos.
A Produção Local de Lipídios Trava a Máquinaria de Divisão
Para testar se esses efeitos dependiam da produção local de PI(4,5)P2, os autores mensuraram o PI(4,5)P2 ao redor do corpúsculo médio e manipularam enzimas que adicionam ou removem esse lipídio. Depleção de PIPKIγ-i3/i5 reduziu o PI(4,5)P2 no corpúsculo médio, enquanto bloquear uma enzima degradadora de PI(4,5)P2 teve o efeito oposto. Importante, restaurar uma forma de splicing cataliticamente ativa e capaz de se ligar às septinas resgatou o agrupamento adequado de anilina e septinas na ponte, mas mutantes sem atividade quinase ou incapazes de se ligar às septinas não o fizeram. Usando imagens ao vivo e uma técnica de microscopia de expansão que infla fisicamente a amostra para revelar detalhes finos, a equipe mostrou que, sem PIPKIγ-i3/i5, as septinas deixam de se mover para os microtúbulos da ponte, a ponte fica mais curta e menos agrupada, e um complexo crucial chamado centralspindlin deixa de permanecer firmemente associado ao corpúsculo médio. 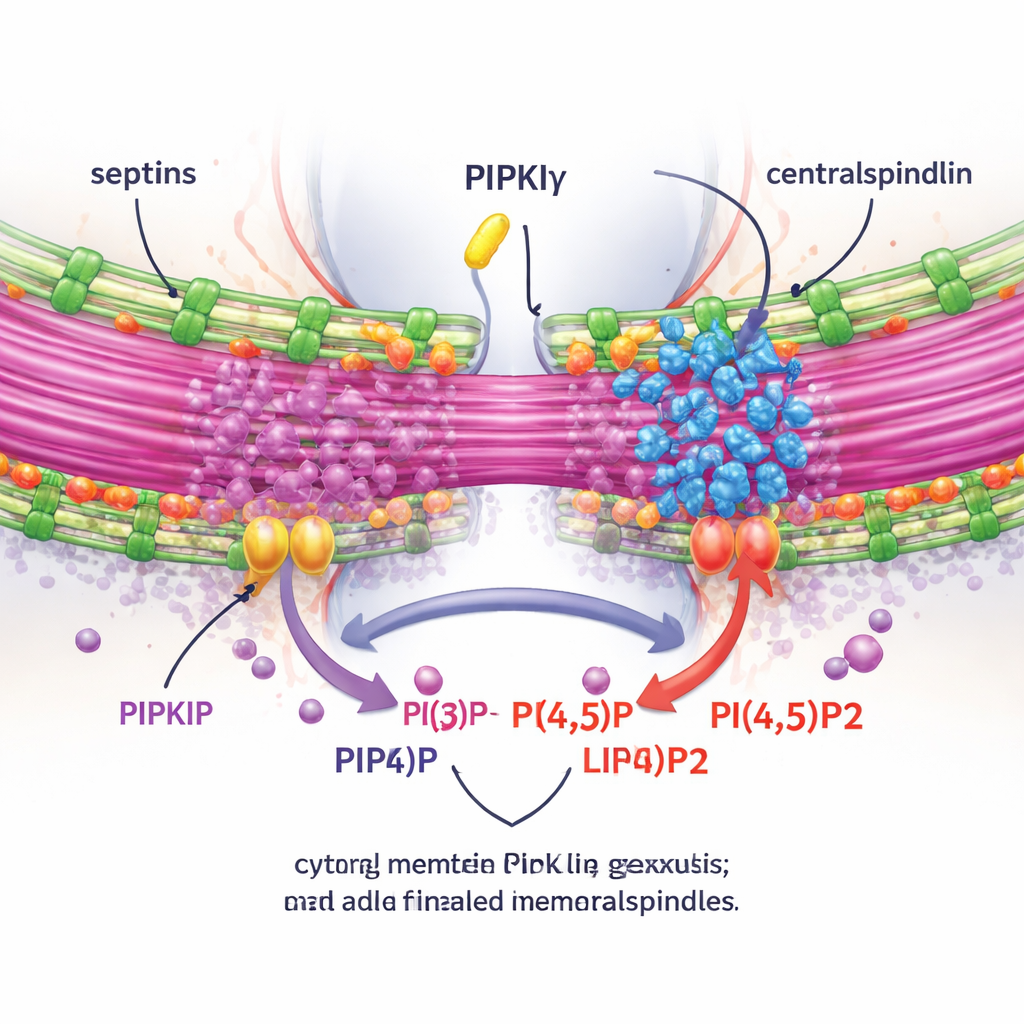
Montando um Ponto de Controle para um Corte Limpo
O centralspindlin ajuda a ligar os microtúbulos do corpúsculo médio à membrana circundante e regula pequenos interruptores moleculares que controlam a forma celular. O estudo mostra que o centralspindlin se associa tanto às septinas quanto ao PIPKIγ, e que a perda de qualquer um desses parceiros enfraquece de modo semelhante sua presença no corpúsculo médio. Os autores propõem que as septinas recrutam PIPKIγ-i3/i5 para o sulco invaginado, onde essas enzimas criam um mosaico concentrado de PI(4,5)P2. Esse reservatório lipídico local, por sua vez, estabiliza a anilina, o centralspindlin e as septinas nas proximidades do corpúsculo médio, promove o agrupamento e a estabilização dos microtúbulos da ponte e permite que a ponte intercelular amadureça até ocorrer o corte final de abscisão. Se esse sistema for perturbado, o PI(4,5)P2 aparece nos lugares errados, as proteínas de andaime se dispersam, os microtúbulos ficam mal agrupados e a citocinese frequentemente falha.
Por Que Isso Importa além da Biologia Celular Básica
Ao identificar como variantes específicas de splicing de PIPKIγ e as septinas cooperam para gerar um sinal lipídico local no corpúsculo médio, este trabalho explica como as células conferem precisão espacial a uma molécula sinalizadora altamente móvel. Essa precisão é crucial para a conclusão segura da divisão celular, ajudando a prevenir a má segregação de cromossomos e números celulares anormais que podem favorecer o desenvolvimento tumoral. As mesmas estruturas do corpúsculo médio também influenciam o destino e a proliferação celular após a divisão, de modo que entender como elas são montadas abre novas vias para explorar como erros nesses andaimes nanoscópicos podem contribuir para o câncer e possivelmente para a manipulação de células-tronco.
Citação: Russo, G., Hümpfer, N., Jaensch, N. et al. Local PI(4,5)P2 synthesis by septin-associated PIPKIγ isoforms controls centralspindlin association with the midbody during cytokinesis. Nat Commun 17, 1482 (2026). https://doi.org/10.1038/s41467-026-69224-3
Palavras-chave: divisão celular, citocinese, lipídios sinalizadores, septinas, biologia do câncer