Clear Sky Science · pt
Inibidor pan‑RAF exarafenibe mira BRAF classe II/III em NSCLC e revela resistência ARAF‑KSR1 e estratégias de combinação
Por que esta pesquisa importa para pacientes com câncer de pulmão
Muita gente já ouviu falar de medicamentos oncológicos direcionados que atacam alterações genéticas específicas. Mas para muitos pacientes com câncer de pulmão, especialmente aqueles cujos tumores carregam mutações menos comuns no gene BRAF, os medicamentos atuais simplesmente não funcionam. Este estudo apresenta um novo fármaco experimental, o exarafenibe, projetado para atingir um conjunto mais amplo de tumores impulsionados por BRAF, e explica como as células cancerosas tentam escapar dele—revelando tratamentos combinados que podem manter esses tumores sob controle por mais tempo.
Uma maioria oculta de mutações negligenciadas
Os pesquisadores começaram fazendo uma pergunta básica: quão comuns são os diferentes tipos de mutações em BRAF em cânceres avançados, e especialmente no câncer de pulmão não pequenas células (NSCLC)? Usando um banco de dados muito grande de biópsias líquidas com mais de 160.000 pacientes, eles analisaram fragmentos de DNA tumoral circulante no sangue. Encontraram que, no câncer de pulmão, mutações em BRAF ocorrem em aproximadamente 4–5% dos pacientes, o que ainda se traduz em muitas milhares de pessoas no mundo. Crucialmente, cerca de dois terços desses tumores pulmonares carregavam as chamadas mutações BRAF da Classe II e Classe III—tipos que os medicamentos aprovados atualmente não atingem de forma eficaz. Pacientes com uma dessas classes, especialmente a Classe II, tendiam a viver menos tempo do que aqueles com a mutação mais familiar da Classe I, provavelmente porque pacientes com Classe I têm acesso a terapias alvo estabelecidas enquanto os de Classe II/III recebem majoritariamente quimioterapia padrão ou imunoterapia.
Um fármaco de próxima geração que mira toda a via
BRAF faz parte de um revezamento de proteínas (a via MAPK) que transmite sinais de crescimento da superfície celular até o núcleo. Muitos dos medicamentos BRAF existentes foram projetados para bloquear apenas uma forma mutante e podem até estimular inadvertidamente proteínas relacionadas em células normais. O exarafenibe foi desenvolvido de forma diferente: é um inibidor “pan‑RAF” criado para calar vários membros da família RAF (ARAF, BRAF e CRAF) em formas monoméricas e dimerizadas, preservando a maioria das outras enzimas celulares. Em testes bioquímicos contra centenas de quinases humanas, o exarafenibe bloqueou fortemente as três proteínas RAF e apresentou poucos efeitos fora do alvo, sugerindo um perfil de segurança mais limpo do que compostos pan‑RAF anteriores.
Efeitos potentes em modelos de tumores difíceis de tratar
A equipe testou o exarafenibe em uma bateria de linhas celulares e modelos em camundongos que carregam diferentes mutações em BRAF e RAS, incluindo tumores derivados de pacientes. Em culturas celulares, o exarafenibe reduziu o crescimento e interrompeu a sinalização MAPK não apenas em células cancerígenas clássicas com BRAF V600E, mas também naquelas com mutações das Classes II e III e em muitas células com mutação em RAS que hoje carecem de boas opções dirigidas. Em camundongos portadores de tumores pulmonares com essas alterações, o exarafenibe encolheu ou retardou os tumores de forma dependente da dose e mostrou relações claras entre níveis do fármaco, supressão da via e resposta tumoral. Dados clínicos iniciais de dois pacientes com câncer de pulmão avançado mutado em BRAF—um com uma fusão rara de BRAF e outro com uma mutação pontual de Classe II—mostraram respostas parciais e alívio sintomático relevante, apoiando a relevância do trabalho pré‑clínico.
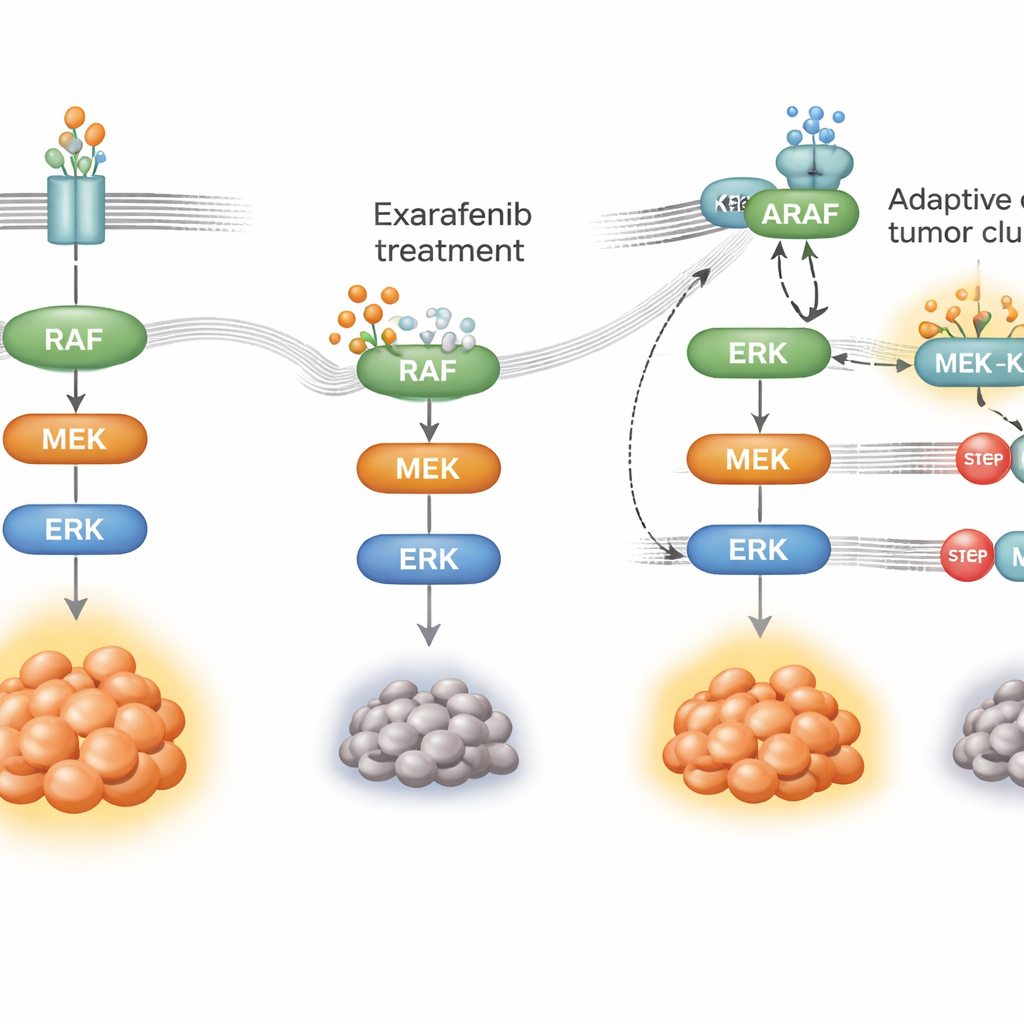
Como o câncer aprende a contornar o fármaco
Nenhuma terapia direcionada funciona para sempre; as células cancerosas se adaptam. Para ver como tumores poderiam resistir ao exarafenibe, os pesquisadores expuseram células de câncer de pulmão com mutação em BRAF ao fármaco por meses até que surgissem populações resistentes. Essas células ainda dependiam da mesma via de crescimento, mas a reconfiguraram. Em vez de dependerem principalmente do BRAF mutante, aumentaram a atividade de um interruptor a montante chamado RAS e passaram a usar outro membro da família, ARAF, em conjunto com uma proteína scaffolding chamada KSR1. Sob pressão do fármaco, ARAF e KSR1 formaram complexos estáveis que ajudaram a manter o revezamento MAPK ativo mesmo com exarafenibe ligado. Quando os cientistas silenciaram seletivamente ARAF ou KSR1, ou reduziram a atividade de RAS, as células resistentes voltaram a ficar sensíveis ao exarafenibe e os sinais de sobrevivência ruíram.
Estratégias de combinação para se antecipar à resistência
Munidos desse mapa mecanístico, a equipe procurou fármacos parceiros que pudessem bloquear a via em pontos de estrangulamento compartilhados pelas rotas original e de desvio. Descobriram que associar exarafenibe com drogas que inibem MEK ou ERK—etapas-chave a jusante no revezamento MAPK—produziu forte sinergia em muitos modelos celulares e em camundongos, incluindo tumores intrinsecamente menos sensíveis ou que haviam adquirido resistência. Essas combinações mantiveram a via bloqueada por mais tempo, desencadearam mais morte celular e, em animais, muitas vezes funcionaram tão bem quanto ou melhor do que doses mais altas de exarafenibe sozinho, sem toxicidade adicional óbvia. Agentes que miram RAS diretamente também potencializaram os efeitos do exarafenibe em modelos onde RAS claramente dirigia a resistência, sugerindo outra tática clinicamente promissora.
O que isso significa para os pacientes
Para pessoas com NSCLC que carregam mutações BRAF das Classes II ou III—ou fusões complexas de BRAF e co‑mutações em RAS—não existem atualmente terapias alvo aprovadas, e os desfechos ficam atrás dos pacientes com alterações mais comuns. Este estudo fornece um forte argumento científico de que o exarafenibe pode ajudar a preencher essa lacuna ao silenciar amplamente a sinalização dirigida por RAF. Também explica como os tumores podem se adaptar por meio do desvio ARAF‑KSR1 e mostra que atingir a via em vários níveis, especialmente combinando inibidores de RAF e MEK ou acrescentando inibidores de RAS, pode proporcionar controle tumoral mais profundo e duradouro. Juntas, essas descobertas traçam um caminho para ensaios clínicos destinados a levar terapias-alvo combinadas e personalizadas a um grande e anteriormente desassistido grupo de pacientes com câncer de pulmão.
Citação: Manabe, T., Bergo, H.C., Li, Q. et al. Pan-RAF inhibitor exarafenib targets BRAF class II/III NSCLC and reveals ARAF-KSR1 resistance and combination strategies. Nat Commun 17, 2484 (2026). https://doi.org/10.1038/s41467-026-69216-3
Palavras-chave: Câncer de pulmão com mutação em BRAF, inibidor pan‑RAF, sinalização MAPK, resistência a fármacos, combinações de terapias alvo