Clear Sky Science · pt
Engenharia de uma enzima citocromo P450 como peroxigenase para hidroxilação seletiva de esteroides
Fazendo medicamentos a partir de moléculas difíceis de ajustar
Medicamentos esteroidais — desde comprimidos anti-inflamatórios até terapias hormonais — estão entre os fármacos mais utilizados no mundo. Ainda assim, ajustar finamente essas moléculas, adicionando um único átomo de oxigênio exatamente no local certo, é notoriamente difícil com a química tradicional. Este estudo mostra como cientistas redesenharam uma enzima natural para que ela possa “lapidar” com precisão moléculas de esteroides usando peróxido de hidrogênio simples, potencialmente criando rotas mais limpas e baratas para fármacos importantes.
Por que os esteroides são tão difíceis de customizar
Esteroides são construídos a partir de um empilhamento compacto de anéis de carbono, com muitas ligações carbono–hidrogênio quase idênticas. Métodos químicos convencionais têm dificuldade em mirar apenas uma dessas ligações sem afetar outras, frequentemente exigindo reagentes agressivos, altas temperaturas e múltiplas etapas de proteção que geram resíduos. Ainda assim, pequenas alterações — como adicionar um único grupo hidroxila (um –OH) em uma posição específica — podem alterar dramaticamente o comportamento de um esteroide no organismo. Enzimas da família citocromo P450 são as especialistas naturais para esse tipo de ativação precisa de ligações C–H, mas em sua forma natural elas normalmente precisam de cofatores caros e maquinaria para manejar oxigênio, o que limita seu uso direto na manufatura.
Descobrindo um ponto de partida enzimático promissor
Usando mineração genômica, os pesquisadores identificaram uma P450 autossuficiente, chamada P450stri, de uma bactéria do solo. Diferente de uma enzima clássica de trabalho chamada P450BM3, que prefere ácidos graxos pequenos, a P450stri aceita naturalmente moléculas esteroidais volumosas como a testosterona. Em suas condições nativas, alimentada pelo cofator celular NADH, a P450stri adiciona grupos hidroxila em três posições da testosterona, produzindo uma mistura de produtos. Essa habilidade intrínseca de reconhecer esteroides tornou a P450stri um “andaime” atraente para a engenharia de um catalisador mais seletivo e compatível com processos industriais.
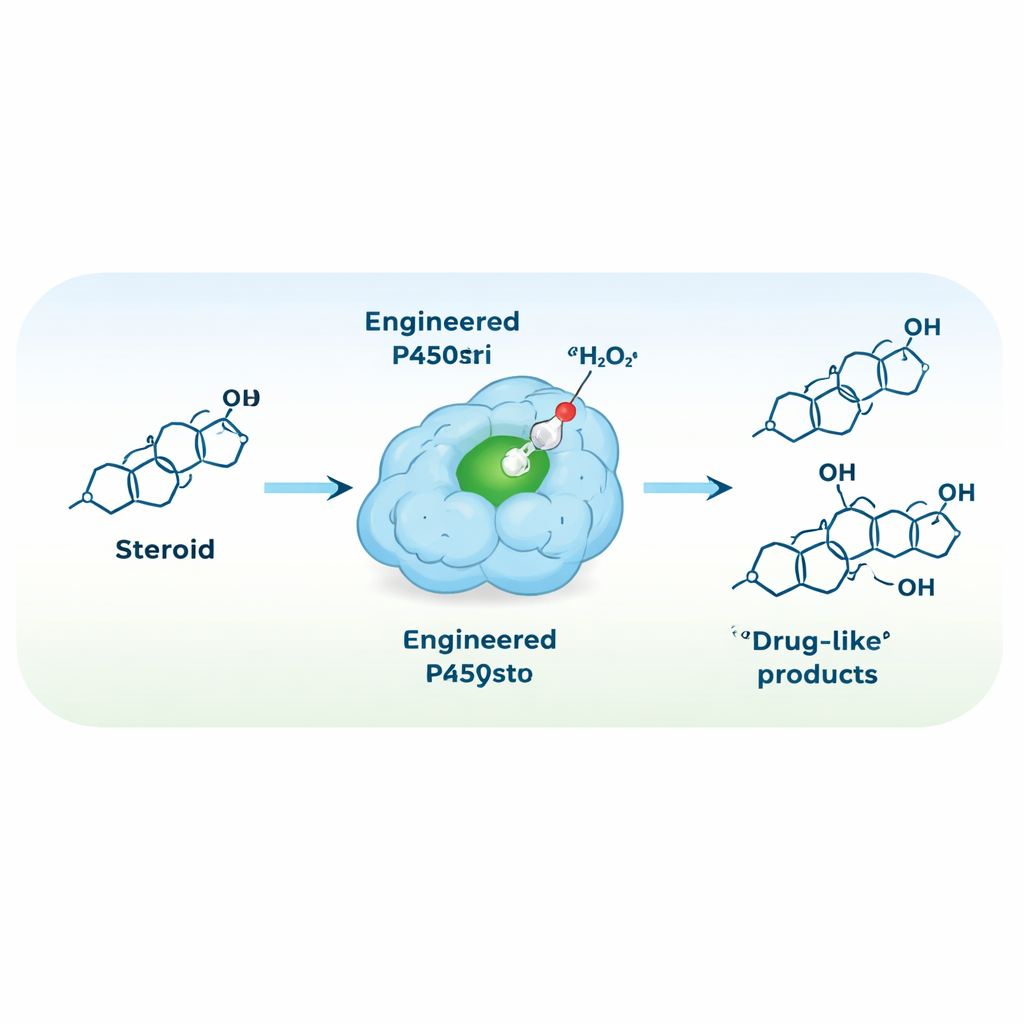
Reconfigurando a enzima para funcionar com peróxido de hidrogênio
Para simplificar o preparo da reação, a equipe procurou transformar a P450stri em uma peroxigenase — uma enzima que usa diretamente peróxido de hidrogênio como agente oxidante, eliminando a necessidade de cofatores caros e proteínas auxiliares. Uma única mutação estratégica, substituindo uma fenilalanina volumosa logo acima do centro heme por uma alanina menor, gerou uma variante chamada M1. Essa mudança abriu espaço ao redor do centro de ferro reativo e, surpreendentemente, tornou a enzima tanto mais tolerante a níveis elevados de peróxido de hidrogênio quanto muito mais seletiva. No novo modo dirigido por peróxido, M1 converteu a testosterona principalmente em um único produto, hidroxilado na posição 15β, com cerca de 94% de seletividade — ante 35% na enzima original.
Um modelo “Frasco Redondo” para um design enzimático mais inteligente
Para melhorar ainda mais o desempenho, os autores introduziram um conceito de projeto que chamam de modelo “Frasco Redondo”. Eles tratam o sítio ativo onde a química ocorre como a base arredondada e os túneis de acesso estreitos como o pescoço e a tampa. A base determina qual posição do esteroide será modificada, enquanto o pescoço controla a facilidade com que o esteroide e o peróxido de hidrogênio alcançam o centro reativo. Guiados por simulações computacionais e software de mapeamento de túneis, ajustaram sistematicamente um pequeno conjunto de aminoácidos que revestem esses túneis, afinando seu tamanho e hidrofobicidade. Essa estratégia bidimensional gerou uma variante de destaque, M4, que manteve alta seletividade 15β enquanto aumentou consideravelmente a velocidade da reação e tolerou concentrações de peróxido de hidrogênio de até algumas centenas de miliM.
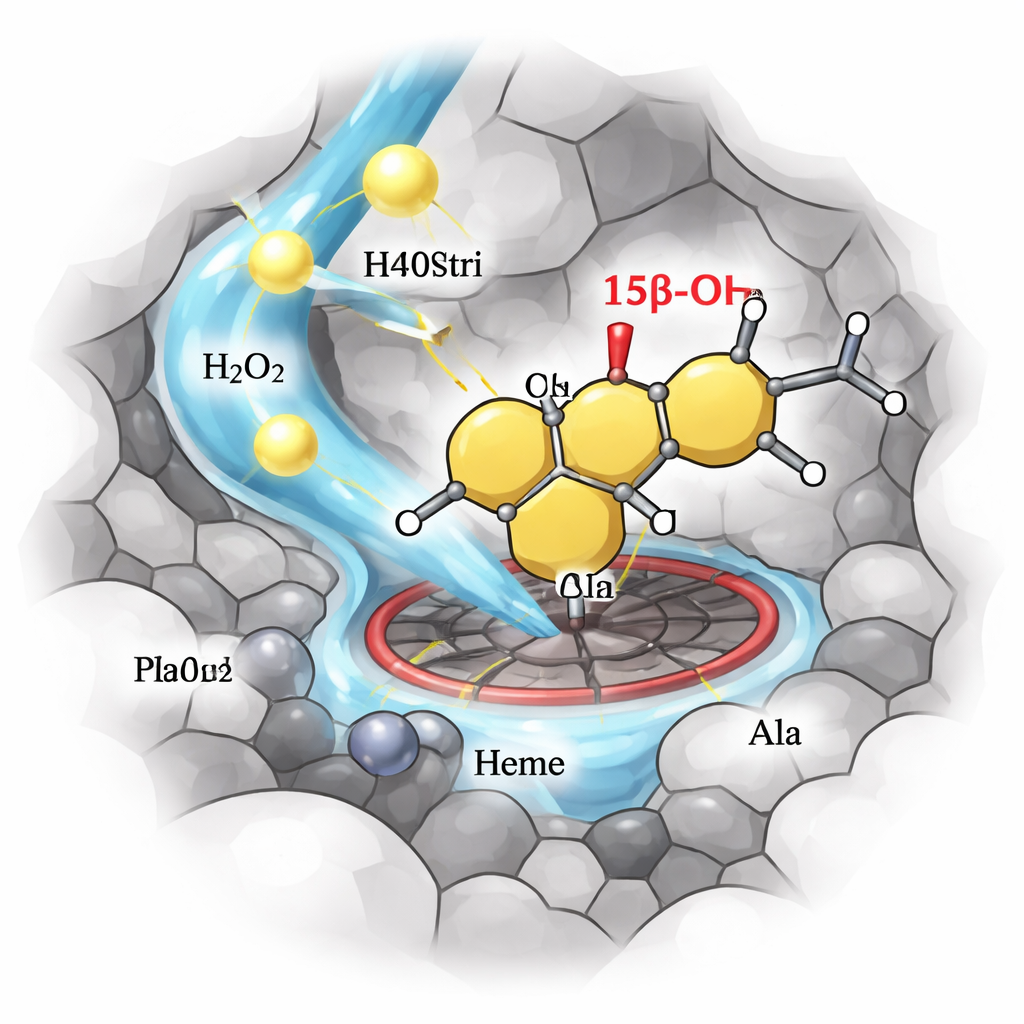
Do banco de laboratório a upgrades de esteroides em escala
A enzima M4 engenheirada foi então testada em reações em escala maior com testosterona e um esteroide relacionado usado em contextos de melhora de desempenho. Em misturas aquosas simples à temperatura ambiente, impulsionada apenas por peróxido de hidrogênio, a M4 converteu mais de 90% do material inicial e entregou produtos isolados hidroxilados em 15β em rendimentos em torno de 75–80%. Essas condições são muito mais brandas e limpas do que as rotas químicas típicas. Por fim, a equipe mostrou que ao transplantar as mutações-chave para várias P450s relacionadas no mesmo “ramo” evolutivo, puderam convertê-las de modo confiável em peroxigenases igualmente seletivas e eficientes, destacando a generalidade de suas regras de projeto.
O que isso significa para futuros medicamentos
Para um não-especialista, o ponto principal é que os pesquisadores ensinaram uma enzima natural a agir como uma “microfábrica” altamente precisa, alimentada por peróxido, para modificar fármacos esteroidais. Ao combinar um modelo conceitual simples com mutações direcionadas, criaram uma enzima capaz de adicionar um grupo OH no local exato, sob condições suaves e escaláveis, e então transferiram essa estratégia para proteínas relacionadas. Essa abordagem pode agilizar a produção de esteroides existentes, abrir rotas para novos candidatos a fármacos e servir de roteiro para a engenharia de outras enzimas que ativam de forma limpa ligações C–H resistentes em moléculas complexas.
Citação: Tang, T., Wang, R. & Chen, Y. Engineering a cytochrome P450 enzyme as a peroxygenase for selective hydroxylation of steroids. Nat Commun 17, 1996 (2026). https://doi.org/10.1038/s41467-026-69211-8
Palavras-chave: biocatálise de esteroides, engenharia de citocromo P450, peroxigenase, catálise com peróxido de hidrogênio, hidroxilação seletiva