Clear Sky Science · pt
Biologia estrutural em célula única com cristalografia eletrônica intracelular
Vendo a Forma da Vida, Uma Célula de Cada Vez
As proteínas são as pequenas máquinas que mantêm cada célula viva, mas para entender de fato como funcionam, os cientistas precisam ver suas formas tridimensionais em detalhes finos. Tradicionalmente, isso significou purificar quantidades enormes de proteína e cultivar grandes cristais frágeis fora da célula—frequentemente um processo lento e sujeito a falhas. Este estudo apresenta uma nova forma de ler a estrutura de proteínas diretamente a partir de um único cristal dentro de uma única célula, usando elétrons em vez de raios X. Isso aponta para um futuro em que a biologia estrutural de alta resolução pode ser feita em laboratórios comuns e até mesmo ao nível de células individuais.
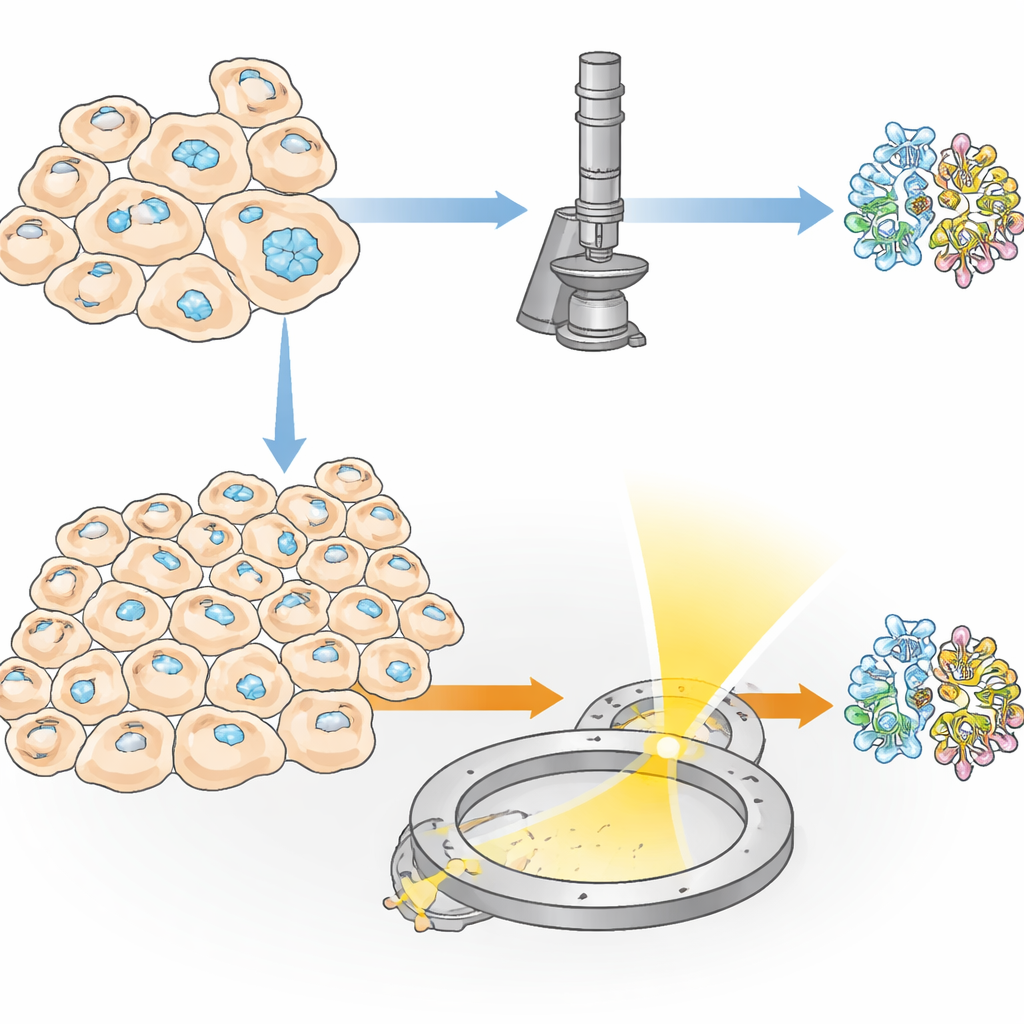
Cristais Ocultos Dentro de Células Vivas
Algumas proteínas naturalmente se agregam em pequenos cristais dentro de células vivas, servindo a propósitos como armazenamento, proteção ou ajudando as células a responder ao estresse. Pesquisadores também podem induzir células a produzir tais cristais ao engenheirar a produção de grandes quantidades de uma proteína escolhida. Essa cristalização “in‑cell” tem duas grandes vantagens: a proteína nunca sai de um ambiente semelhante ao natural, e características delicadas—como adições de açúcar ou pequenas moléculas ligadas—podem ser preservadas de maneiras que frequentemente falham na cristalização em tubos de ensaio. No entanto, um obstáculo importante permaneceu: em muitos experimentos, apenas uma fração muito pequena das células realmente forma cristais, de modo que métodos tradicionais de raios X precisam de dezenas de milhares de cristais e, portanto, de um número enorme de células.
Uma Nova Rota: Elétrons em Vez de Raios X
Os autores introduzem um método que chamam de IncelluloED, que combina cristalização in‑cell com difração eletrônica tridimensional. Elétrons interagem muito mais fortemente com a matéria do que raios X, o que significa que dados úteis podem ser coletados a partir de cristais que são tanto menores quanto em número muito menor. A equipe escolheu uma proteína fúngica chamada HEX‑1, que normalmente forma cristais hexagonais que ajudam a tampar poros minúsculos entre células fúngicas sob estresse. Produzindo essa proteína dentro de células de inseto, eles criaram cristais microscópicos regulares que serviram como caso‑teste para o novo fluxo de trabalho.
Transformando Um Cristal em um Mapa Detalhado
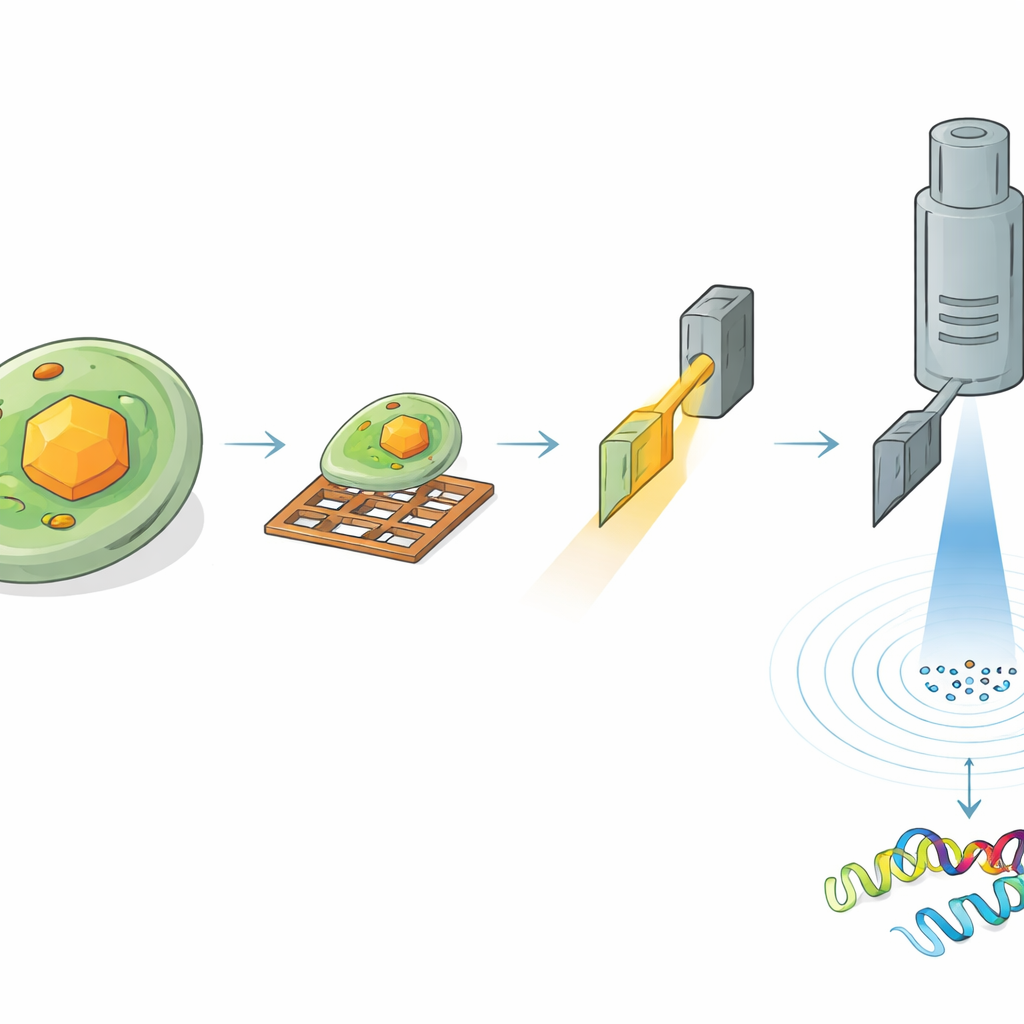
Para ler a estrutura do HEX‑1 dentro de uma célula, os pesquisadores precisaram localizar e cuidadosamente afinar a região certa da amostra. Primeiro, congelaram as células contendo cristais em grades metálicas minúsculas e revestiram a superfície com uma fina camada de platina. Usando microscopia óptica criogênica, varreram grandes áreas da grade para localizar células contendo cristais e mediram as posições tridimensionais dos cristais sob a superfície. Em seguida, moveram a mesma amostra para um instrumento especializado que combina um microscópio eletrônico de varredura com um feixe de íons focalizado. Guiados pelas imagens ópticas anteriores, fresaram o material circundante para esculpir uma fatia ultrafina, ou lamela, atravessando um cristal escolhido, com apenas algumas centenas de nanômetros de espessura—ideal para a passagem de elétrons.
Elétrons Revelam Detalhe Atômico a Partir de Volumes Microscópicos
As lamelas preparadas foram então transferidas para um microscópio eletrônico de alto desempenho operando em temperaturas criogênicas. À medida que a fatia de cristal era girada lentamente no microscópio, um feixe de elétrons finamente controlado passava através dela, criando uma série de padrões de difração—arranjos delicados de pontos que codificam as posições dos átomos. A partir de um volume de cristal de aproximadamente 1,6 micrômetros cúbicos, a equipe reconstruiu a estrutura 3D completa do HEX‑1 a 1,9 ångström de resolução, nítida o bastante para modelar a maioria das cadeias laterais da proteína. Volumes ainda menores, de cerca de 0,8 micrômetros cúbicos, produziram uma estrutura praticamente idêntica com resolução apenas um pouco inferior. Importante, os modelos resultantes se ajustaram de perto aos obtidos usando uma abordagem convencional de raios X serial que requereu mais de 60.000 cristais e um volume total de cristal aproximadamente sete milhões de vezes maior.
Como Isso Muda o Jogo da Biologia Estrutural
Comparações lado a lado mostraram que a estrutura determinada a partir de um único cristal in‑cell por difração eletrônica é essencialmente a mesma daquela obtida pela média de dezenas de milhares de cristais com raios X. Quaisquer diferenças foram pequenas e majoritariamente confinadas a loopings flexíveis, onde se espera movimento natural. Os pesquisadores também demonstraram que as doses de elétrons usadas foram baixas o suficiente para evitar danos por radiação graves, e que todo cristal processado gerou dados de alta qualidade. Embora a preparação das lamelas finas ainda exija habilidade e tempo, os instrumentos necessários—microscópios ópticos criogênicos, sistemas de feixe de íons focalizado e microscópios eletrônicos criogênicos—já são comuns em muitos centros de pesquisa.
De Muitas Células a um Laboratório Estrutural de Célula Única
Este trabalho mostra que agora é possível determinar a estrutura de uma proteína em nível atômico a partir de apenas um cristal dentro de uma célula, sem nunca purificar a proteína. IncelluloED pode ser especialmente poderoso quando apenas poucas células formam cristais, ou quando proteínas são difíceis de isolar sem perder parceiros importantes ou grupos químicos. À medida que o fluxo de trabalho se tornar mais automatizado e for estendido a outras proteínas, ele pode permitir que pesquisadores explorem como as estruturas variam de célula para célula, estudem mudanças relacionadas a doenças em seu contexto nativo e até apoiem a descoberta de medicamentos diretamente em células vivas. Em efeito, o estudo aproxima muito a visão de um “laboratório estrutural de célula única” da realidade.
Citação: Bílá, Š., Pinkas, D., Khakurel, K. et al. Single-cell structural biology with intracellular electron crystallography. Nat Commun 17, 2109 (2026). https://doi.org/10.1038/s41467-026-69205-6
Palavras-chave: difração eletrônica, cristalografia in cellulo, biologia estrutural em célula única, estrutura de proteína, crio‑EM