Clear Sky Science · pt
14-3-3ζ interage com o domínio de ligação ao DNA de FOXO3a e dissocia o DNA por competição via ancoragem de duplo motivo
Como células cancerosas desativam seu próprio interruptor de autodestruição
Nossas células possuem sistemas de segurança embutidos que podem desencadear sua própria morte quando ficam muito danificadas ou perigosas. Um desses sistemas é controlado por uma proteína chamada FOXO3a, que ativa genes que fazem células descontroladas cometerem suicídio. Muitos cânceres, porém, encontram maneiras de silenciar o FOXO3a e continuar crescendo. Este estudo investiga os detalhes moleculares de como outra proteína, 14-3-3ζ, ajuda células cancerosas a desprender o FOXO3a do DNA e desativar esse interruptor de autodestruição.
A proteína guardiã que empurra de volta contra o câncer
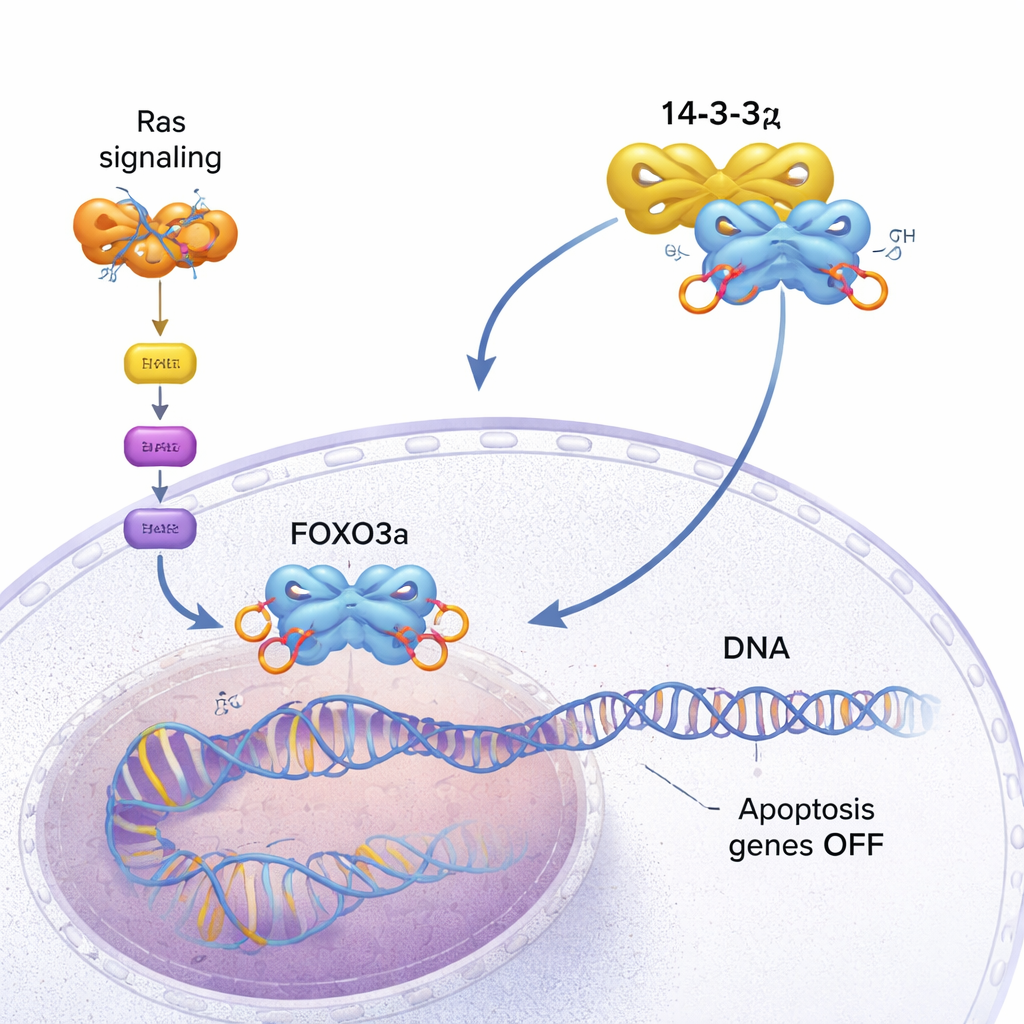
FOXO3a age como um inspetor de segurança da célula. Ela se liga a locais específicos no DNA e ativa genes que freiam o crescimento ou desencadeiam a morte celular programada (apoptose) quando algo dá errado. Em células saudáveis, isso ajuda a evitar a formação de tumores. Em muitos cânceres, entretanto, uma via de promoção do crescimento dirigida por proteínas Ras mutantes fica permanentemente ativada. Essa via ativa uma quinase chamada AKT, que marca quimicamente o FOXO3a em vários sítios com grupos fosfato. Essas marcas criam pontos de ancoragem para a 14-3-3ζ, uma proteína “adaptadora” dimérica que reconhece motivos fosforilados em muitos alvos. Quando a 14-3-3ζ se prende ao FOXO3a, os freios internos da célula começam a falhar.
Por que a simples força de ligação não explicava o efeito
Trabalhos anteriores em uma proteína relacionada, FOXO4, sugeriram que proteínas 14-3-3 removem fatores FOXO do DNA simplesmente porque se ligam com maior afinidade. Mas o FOXO3a prefere seus alvos de DNA naturais mais fortemente do que o modelo anterior supunha. Neste estudo, os pesquisadores produziram uma versão do FOXO3a que inclui o domínio de ligação ao DNA e dois sítios-chave de fosforilação. Eles mediram quão fortemente essa proteína se liga ao DNA ou à 14-3-3ζ e descobriram que as diferenças na força de ligação eram modestíssimas: a 14-3-3ζ era apenas cerca de duas vezes uma parceira mais forte que o DNA. Ainda assim, em experimentos de mistura que acompanham como as moléculas viajam através de uma coluna de cromatografia, a 14-3-3ζ foi capaz de induzir quase a liberação completa do DNA do FOXO3a, como se fosse aproximadamente 100 vezes mais competitiva do que o esperado. Essa discrepância sugeriu que um mecanismo extra estava em ação.
Uma fixação em três pontos que afasta o DNA
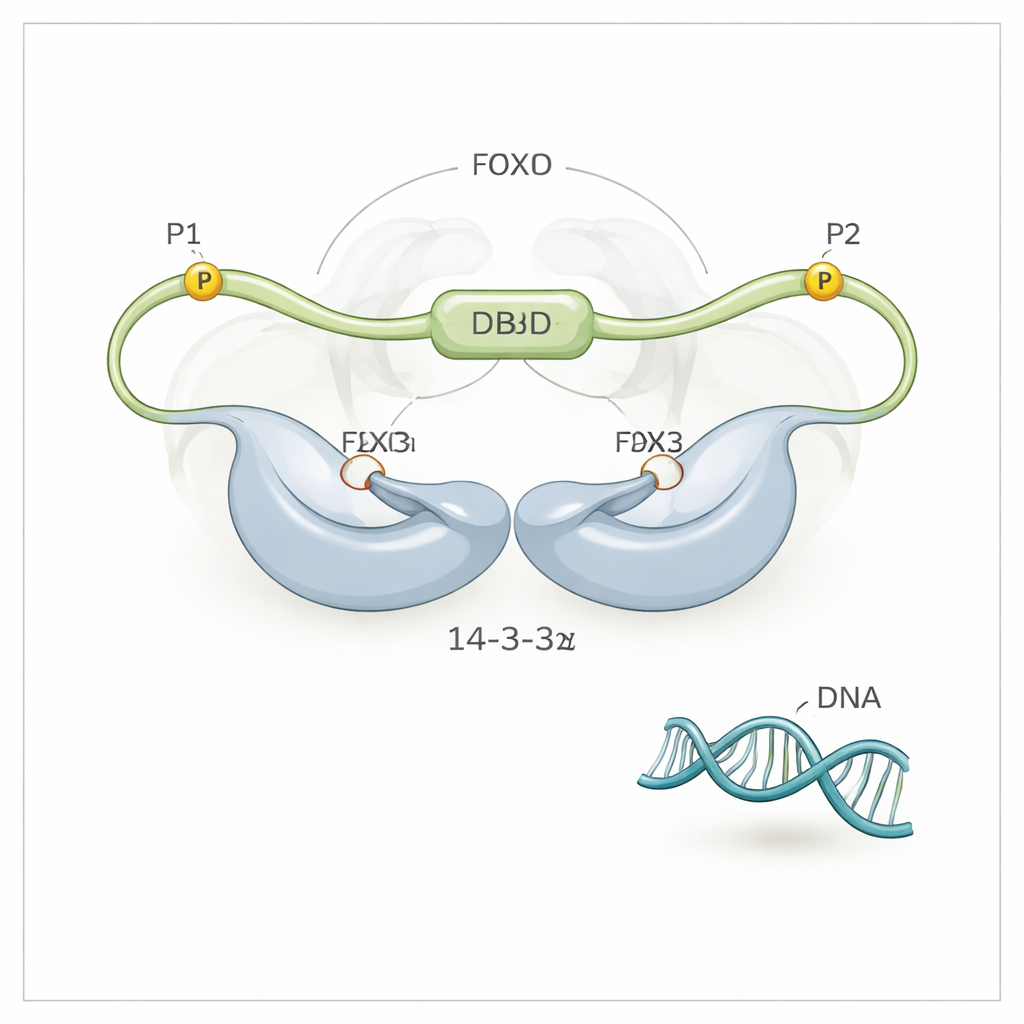
Usando espectroscopia de RMN de alta resolução, a equipe descobriu que a 14-3-3ζ faz mais do que apenas agarrar o FOXO3a em seus dois motivos fosforilados (chamados P1 e P2). Ela também estabelece contato direto, embora mais fraco, com o próprio domínio de ligação ao DNA (DBD) do FOXO3a — a superfície que normalmente abraça o DNA. A proteína 14-3-3ζ forma um dímero simétrico com dois sulcos. Cada sulco prende um dos motivos fosforilados do FOXO3a, ancorando o FOXO3a na 14-3-3ζ em dois pontos. Como um desses motivos (P2) fica muito próximo, na cadeia, do domínio de ligação ao DNA, essa “ancoragem de duplo motivo” posiciona efetivamente a 14-3-3ζ bem ao lado do DBD, aumentando muito a probabilidade de que o DBD colida e se ligue à superfície da 14-3-3ζ em vez de ao DNA. Os pesquisadores puderam até ver que o DBD oscila entre os dois lados do dímero 14-3-3ζ, passando a maior parte do tempo protegido do DNA.
Quais marcas de fosfato importam mais
Para separar os papéis dos dois sítios fosforilados, a equipe engenheirou variantes de FOXO3a nas quais apenas um sítio podia ser fosforilado por vez. Quando apenas o sítio P2, próximo ao DBD, estava ativo, a 14-3-3ζ podia desalojar parcialmente o DNA, mas não completamente. Quando apenas o sítio mais distante P1 estava ativo, a 14-3-3ζ podia se ligar ao FOXO3a, mas mal afetava sua conexão com o DNA. A liberação completa do DNA exigia que ambos os sítios atuassem em conjunto: P1 fornece um ponto de ancoragem inicial de alta afinidade para a 14-3-3ζ, e P2 posiciona o dímero suficientemente perto do DBD para tornar a concentração local de 14-3-3ζ efetivamente enorme naquele ponto. Essa ancoragem em múltiplas etapas amplifica uma preferência de ligação modesta em uma poderosa capacidade de expulsar o DNA.
Do cabo de guerra molecular a novas ideias para fármacos
Para um não especialista, a conclusão principal é que células cancerosas exploram um truque geométrico molecular inteligente, não apenas força bruta de ligação, para silenciar uma importante proteína supressora de tumor. A 14-3-3ζ usa duas pequenas marcas de ancoragem no FOXO3a como pontos de apoio, então estende-se para cobrir a superfície de apreensão do DNA do domínio central do FOXO3a, impedindo-o de ativar genes de morte celular. Como as famílias FOXO e 14-3-3 são amplamente utilizadas em muitos tecidos, essa estratégia de ancoragem dupla provavelmente é comum em outros cânceres também. Interromper tanto os pontos de ancoragem dependentes de fosfato quanto o contato mais fraco com a face de ligação ao DNA do FOXO3a poderia restaurar sua capacidade de ativar programas de autodestruição em células tumorais, oferecendo ângulos promissores para o desenho de novos fármacos anticâncer.
Citação: Enomoto, S., Kuwayama, T., Nakatsuka, S. et al. 14-3-3ζ interacts with DNA-binding domain of FOXO3a and competitively dissociates DNA by dual-motif tethering. Nat Commun 17, 1503 (2026). https://doi.org/10.1038/s41467-026-69203-8
Palavras-chave: FOXO3a, proteínas 14-3-3, apoptose, sinalização Ras–AKT, terapias contra o câncer