Clear Sky Science · pt
Mecanismos moleculares dos complexos de flotilina na organização de microdomínios de membrana
Salas ocultas na superfície da célula
Cada célula do seu corpo é envolvida por uma membrana fina que à primeira vista parece simples, mas na verdade é dividida em inúmeros "bairros" minúsculos. Esses bairros ajudam a controlar como sinais são recebidos, como nutrientes entram e como resíduos saem. Este estudo revela como um par de proteínas há muito misteriosas, chamadas flotilinas, constroem pequenas salas protegidas no lado interno da membrana — estruturas que podem influenciar processos tão diversos quanto sinalização celular, transporte de carga e até a disseminação do câncer. 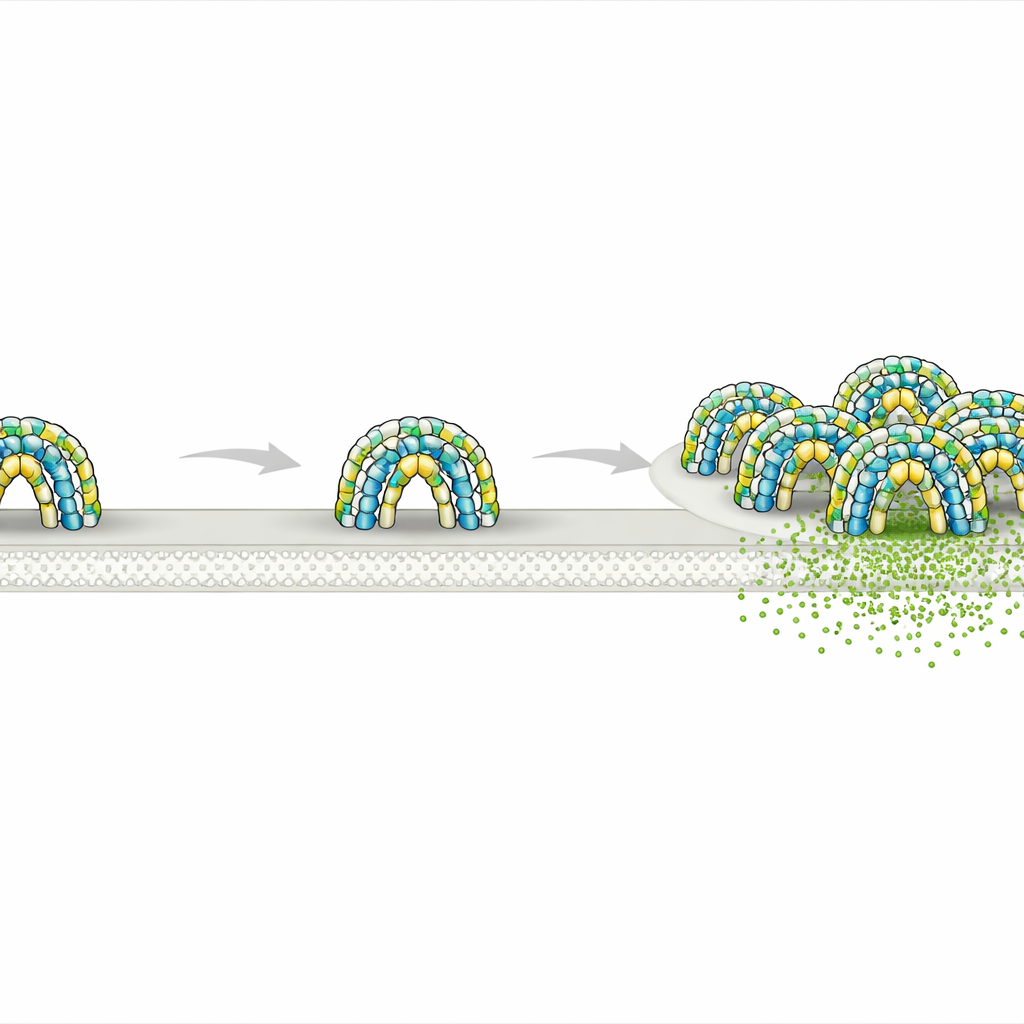
Um olhar mais atento aos minúsculos bairros de membrana
Os biólogos já sabiam há muito tempo que as membranas celulares não são uniformes. Em vez disso, lipídios e proteínas se agrupam em pequenas manchas que funcionam como estações de trabalho temporárias para tarefas específicas, como comunicação ou triagem de carga. Flotilina‑1 e flotilina‑2 são duas proteínas que parecem sempre marcar essas manchas, formando pequenos pontos brilhantes na superfície celular e participando da endocitose — o processo pelo qual as células internalizam material — bem como da sinalização e do tráfego de proteínas. No entanto, ninguém sabia qual a forma que as estruturas de flotilina realmente tomam, nem como elas demarcam seu próprio território na membrana.
Cúpulas que cercam círculos de membrana
Usando criomicroscopia eletrônica de alta resolução em proteínas humanas purificadas, os pesquisadores descobriram que flotilina‑1 e flotilina‑2 se organizam em um complexo notavelmente grande composto por 44 cópias de proteína, alternando entre os dois tipos. Juntas, formam uma cúpula rígida assentada na face interna da membrana. A base dessa cúpula é construída a partir de segmentos âncora na membrana ricos em aminoácidos hidrofóbicos e ligações lipídicas que penetram parcialmente na membrana. Acima disso, longos hastes helicoidais formam uma parede compacta em forma de barril, e um teto de segmentos proteicos entrelaçados tampa a estrutura. O anel de flotilina na base define uma mancha circular de membrana com cerca de 30 nanômetros de diâmetro — essencialmente cercando um pequeno disco de membrana e o espaço logo acima dele.
Cúpulas flexíveis observadas em células vivas
Para testar se essas cúpulas existem em células reais, a equipe engenheirou células T humanas para produzir flotilina‑1 e flotilina‑2 marcadas com fluorescência e as imageou por uma combinação de microscopia de luz e tomografia por criomicroscopia eletrônica. Eles observaram estruturas ocos em forma de cúpula presas à superfície interna da membrana plasmática, correspondendo de perto à forma determinada em amostras purificadas. Muitas cúpulas pareciam ligeiramente distorcidas ou parcialmente abertas, e algumas continham densidades extras no interior, provavelmente representando outras proteínas temporariamente presas sob o teto. Em algumas regiões, múltiplas cúpulas se agrupavam em membranas planas ou curvas, incluindo endossomos e pequenas vesículas extracelulares, sugerindo que cúpulas individuais podem se unir para formar plataformas de membrana maiores. 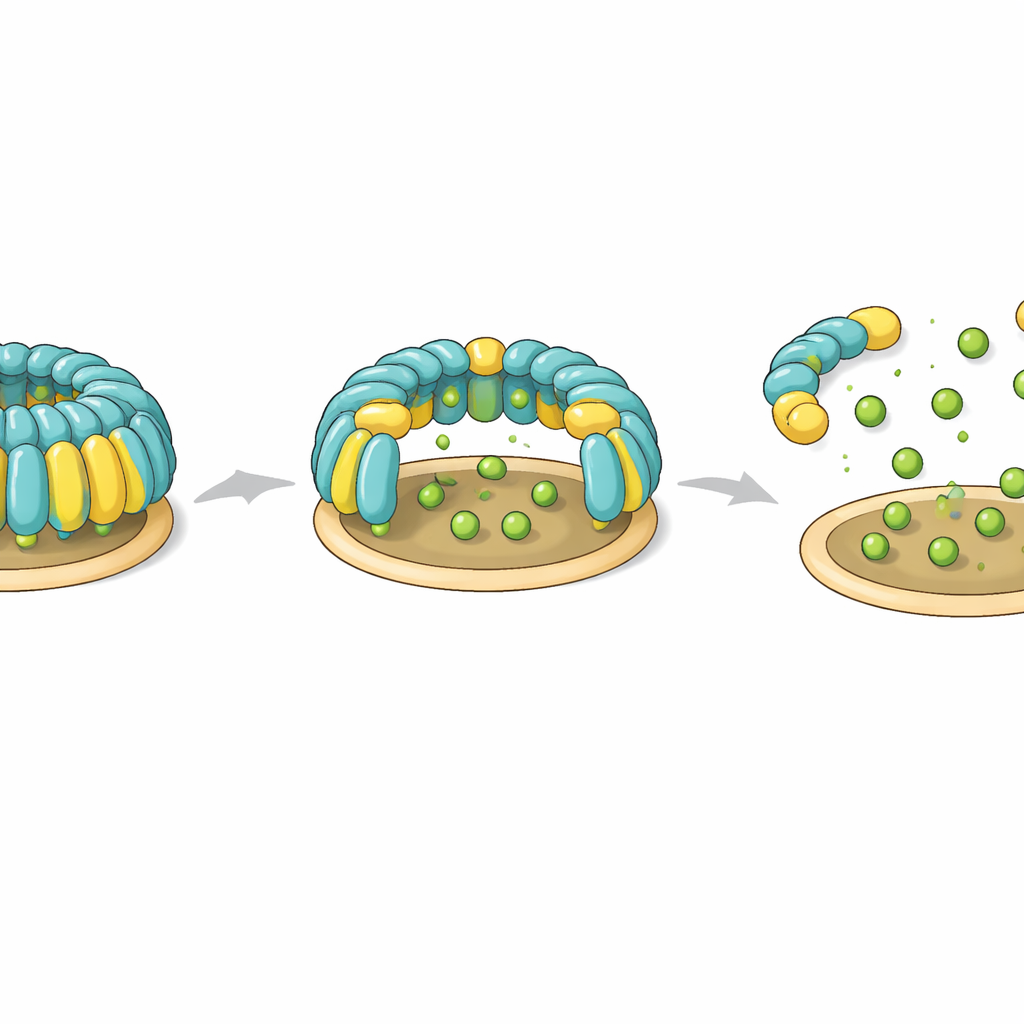
Um interruptor molecular para montar e desmontar cúpulas
O estudo também identifica um possível botão de controle que as células poderiam usar para montar ou desmontar as cúpulas de flotilina. Dois resíduos específicos de tirosina — um em cada proteína de flotilina — situam‑se em posições semelhantes a dobradiças, que conectam a base âncora na membrana à parede helicoidal. No complexo intacto, esses resíduos ajudam a formar um núcleo hidrofóbico justo que trava a orientação dos domínios. Quando os pesquisadores introduziram mutações que imitam a adição de uma carga negativa, como ocorreria quando enzimas fosforilam essas tirosinas, toda a cúpula deixou de se montar. Mutações sem carga não afetaram a montagem. Essas observações sugerem que a fosforilação nesses pontos de dobradiça poderia atuar como um interruptor reversível que desestabiliza a cúpula, abrindo‑a ou desmontando‑a durante processos como a endocitose dependente de flotilina.
Redefinindo como esses domínios moldam a membrana
As manchas de flotilina antes eram vistas principalmente como “rafts” lipídicos ricos em colesterol e gorduras relacionadas. Surpreendentemente, quando a equipe examinou grandes bolhas de membrana destacadas de células, as flotilinas preferiram as regiões mais fluidas, não‑raft, em vez das rígidas e densas em colesterol. A análise lipídica mostrou apenas um enriquecimento modesto de uma molécula em particular, a esfingosina, dentro dos complexos de flotilina, enquanto outros lipídios associados a rafts não estavam concentrados. Isso aponta para um princípio organizador diferente: em vez de serem passageiros em rafts lipídicos pré‑existentes, as cúpulas de flotilina atuam como contêineres estruturais que segregam lateralmente porções de membrana, capturando certas proteínas e lipídios dentro de sua área cercada.
Por que essa arquitetura minúscula importa
Em termos práticos, os complexos de flotilina se comportam como dosséis modulares que as células podem implantar na sua superfície interna para cercar pequenos terrenos circulares de membrana. Cada cúpula pode abrigar uma mistura específica de proteínas parceiras e lipídios e, ao se agrupar com outras, pode construir zonas funcionais maiores para sinalização, triagem de carga ou formação de vesículas. Como as cúpulas são flexíveis e parecem abrir e fechar, e porque sua montagem é sensível à fosforilação, as células podem remodelar dinamicamente essas estruturas em resposta a sinais. Assim, este trabalho reconceitua as flotilinas de indicadores vagos de “rafts” em elementos arquitetônicos concretos que ajudam a esculpir a membrana em micro‑estações de trabalho especializadas.
Citação: Lu, MA., Qian, Y., Ma, L. et al. Molecular mechanisms of flotillin complexes in organizing membrane microdomains. Nat Commun 17, 2541 (2026). https://doi.org/10.1038/s41467-026-69197-3
Palavras-chave: flotilina, microdomínios de membrana, criomicroscopia eletrônica, endocitose, rafts lipídicos