Clear Sky Science · pt
A sobrevivência de macrófagos residentes em tecido depende da função mitocondrial regulada por SerpinB2 em inflamação crônica
Por que as células imunes da gordura importam
A maioria das pessoas pensa na gordura corporal como um depósito passivo, mas ela é na verdade um tecido ativo repleto de células imunes que ajudam a controlar a inflamação e a glicemia. Este estudo revela como um grupo específico de células imunes de longa duração na gordura abdominal profunda atua como guardiã contra o diabetes tipo 2 — e como a inflamação crônica na obesidade as elimina silenciosamente ao danificar suas pequenas usinas de energia, as mitocôndrias.
Dois tipos de guardiões da gordura
O tecido adiposo visceral — gordura que envolve os órgãos internos — contém dois tipos principais de células imunes chamadas macrófagos. Um tipo é de curta duração e é constantemente renovado a partir do sangue; esses macrófagos “inflamatórios” tendem a alimentar o inchaço e a resistência à insulina. O outro tipo é de longa permanência, macrófagos residentes no tecido, que se formam cedo na vida e normalmente ajudam a manter o tecido calmo, a suportar o armazenamento saudável de gordura e a promover a sensibilidade à insulina em todo o organismo. Ao rastrear essas células em camundongos e comparar a atividade gênica, os pesquisadores mostraram que os macrófagos residentes são enriquecidos em genes anti‑inflamatórios e sensibilizadores de insulina, enquanto os macrófagos derivados de monócitos que chegam expressam genes que pioram o controle da glicose.
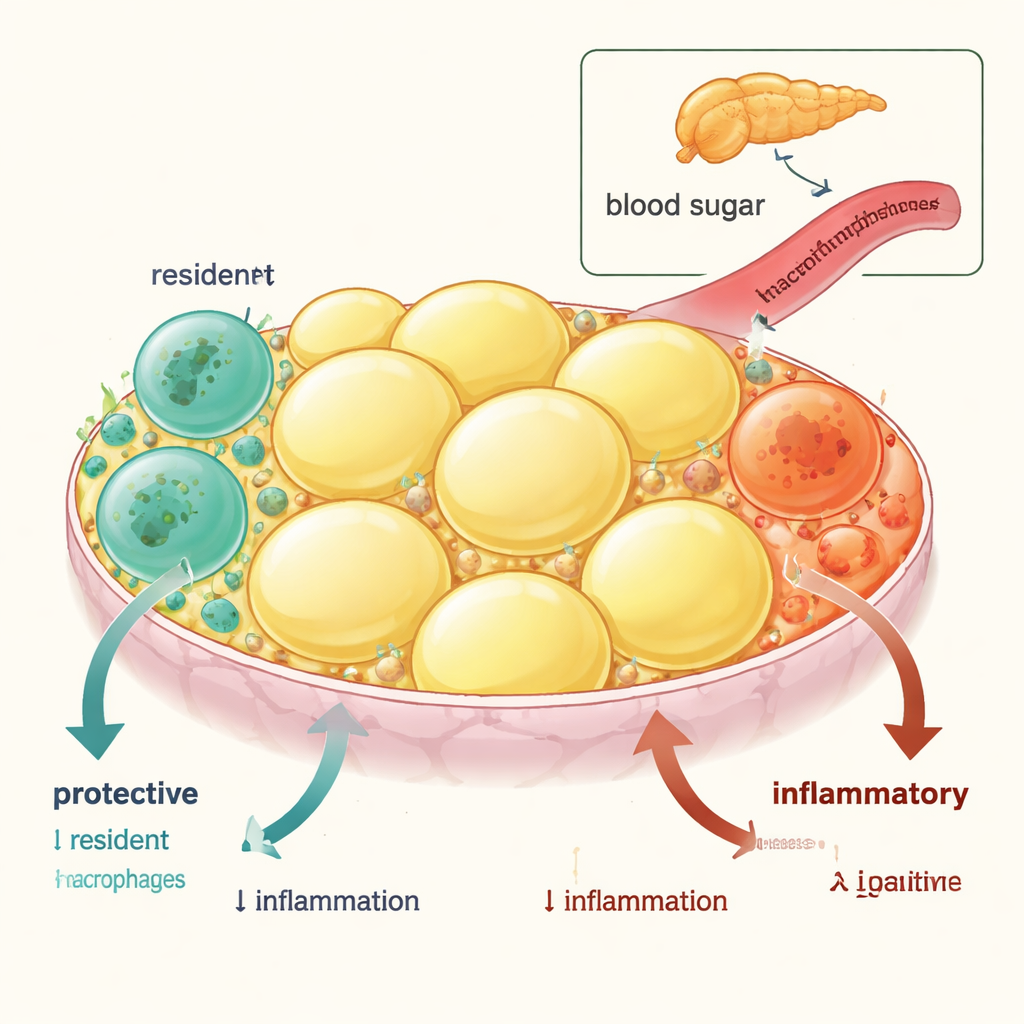
Quando a inflamação mata os bons
Na obesidade, esse equilíbrio protetor se altera. A equipe descobriu que tanto em camundongos obesos quanto em pessoas obesas ou diabéticas, o número de macrófagos residentes na gordura visceral cai, enquanto os macrófagos inflamatórios aumentam. Imagens cuidadosas e marcadores de morte celular revelaram o porquê: os macrófagos residentes passam por mais morte celular programada (apoptose), enquanto as células inflamatórias não. Notavelmente, quando camundongos obesos foram retirados da dieta rica em gordura, a população residente se recuperou lentamente por proliferação local, e a saúde metabólica melhorou — mostrando que essa perda é impulsionada pelo estado inflamatório e pode ser revertida.
Uma única proteína liga as mitocôndrias à sobrevivência
Uma pista-chave foi uma proteína chamada SerpinB2, mais conhecida por papéis na coagulação sanguínea. Os pesquisadores descobriram que SerpinB2 é produzida em níveis muito altos dentro dos macrófagos residentes, mas muito menos nos inflamatórios. Em humanos e camundongos obesos, os macrófagos residentes reduziram fortemente a expressão de SerpinB2, e um índice de massa corporal maior esteve associado a menos células positivas para SerpinB2. Experimentos em células sem SerpinB2 mostraram aumento do vazamento de citocromo c — uma proteína crucial — das mitocôndrias para o citoplasma, um gatilho clássico de apoptose. Esses macrófagos deficientes em SerpinB2 apresentaram menos defesas antioxidantes, mais espécies reativas de oxigênio mitocondriais (ROS) e maior consumo de oxigênio, todos sinais de mitocôndrias estressadas e sobrecarregadas que empurram as células em direção a comportamento inflamatório e morte.
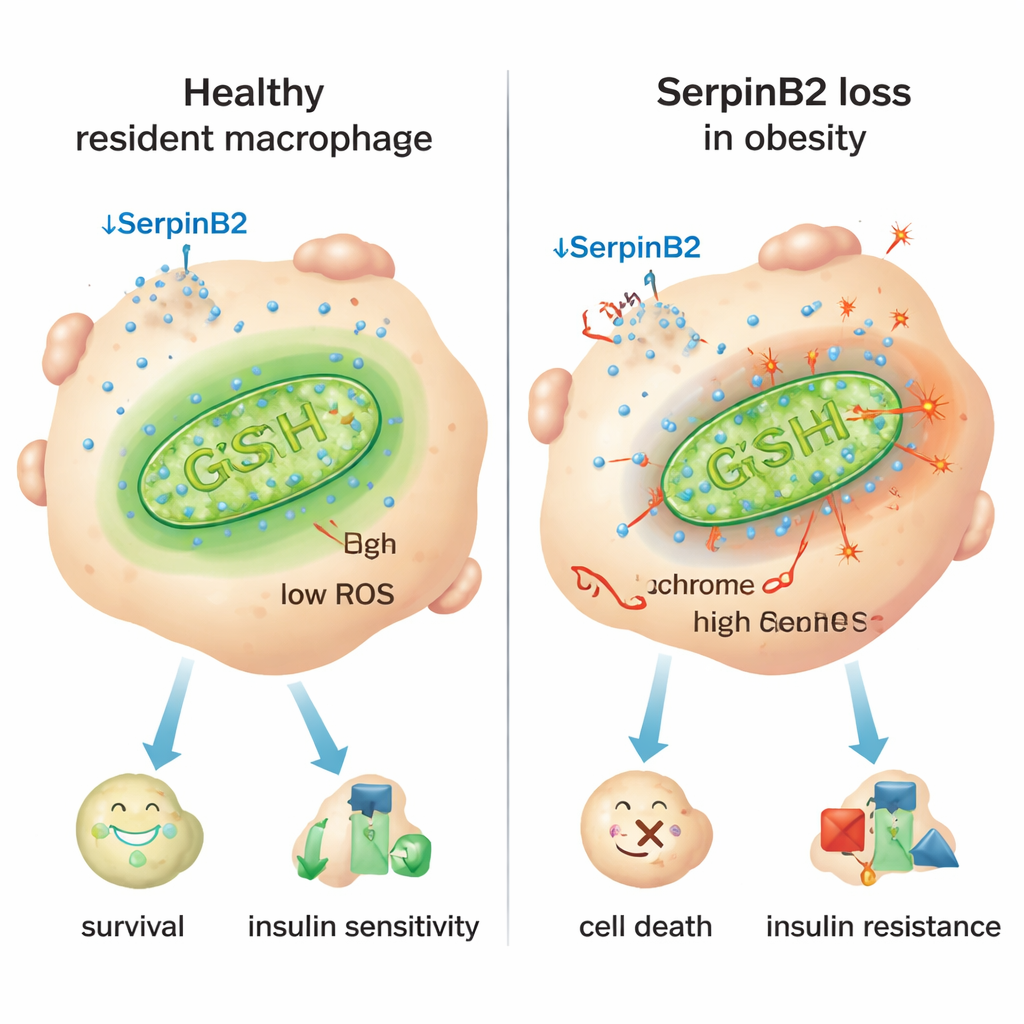
O interruptor inflamatório e uma possível solução
O estudo rastreou esse estresse mitocondrial até sinais inflamatórios crônicos na obesidade, especialmente o mensageiro imune interferon‑γ (IFN‑γ), que é produzido em excesso no tecido adiposo. IFN‑γ ativa um repressor transcricional chamado Ikaros que se liga à região de controle do gene SerpinB2 e a reprime. Em camundongos modificados para que suas células mieloides não respondessem a IFN‑γ, os macrófagos residentes preservaram SerpinB2, sobreviveram melhor, e os animais apresentaram glicemia mais baixa, melhor sensibilidade à insulina e adipócitos menores. Por outro lado, a deleção de SerpinB2 especificamente em macrófagos piorou a intolerância à glicose e a resistência à insulina, em parte porque o tecido adiposo ficou mais inflamado e expandido. O aumento dos níveis do antioxidante glutationa com o suplemento N‑acetilcisteína (NAC) restaurou a proteção mitocondrial, resgatou a sobrevivência dos macrófagos residentes, reduziu o tamanho dos adipócitos e melhorou medidas metabólicas mesmo na ausência de SerpinB2.
O que isso significa para a saúde metabólica
Para o leitor leigo, a mensagem central é que nem toda gordura ou células imunes residentes na gordura são prejudiciais. Um grupo especializado e de longa vida de macrófagos na gordura visceral nos protege da inflamação descontrolada e da glicemia alta ao manter suas mitocôndrias saudáveis por meio de defesas antioxidantes dirigidas por SerpinB2. Na obesidade, sinais inflamatórios crônicos desligam SerpinB2, as mitocôndrias ficam estressadas, essas células protetoras morrem e macrófagos mais danosos assumem, contribuindo para a resistência à insulina. O trabalho sugere que terapias destinadas a preservar os macrófagos residentes — bloqueando o freio IFN‑γ/Ikaros sobre SerpinB2 ou apoiando defesas antioxidantes à base de glutationa — podem ajudar a prevenir ou tratar doenças metabólicas ligadas à obesidade.
Citação: Vasamsetti, S.B., Sadaf, S., Uddin, M.A. et al. Tissue-resident macrophage survival depends on mitochondrial function regulated by SerpinB2 in chronic inflammation. Nat Commun 17, 1493 (2026). https://doi.org/10.1038/s41467-026-69196-4
Palavras-chave: gordura visceral, macrófagos, mitocôndrias, resistência à insulina, SerpinB2