Clear Sky Science · pt
Engenharia metabólica da biossíntese da doxorrubicina por meio da otimização de P450‑parceiros redox e análise estrutural de DoxA
Por que a origem de um medicamento contra o câncer importa
A doxorrubicina é um dos fármacos coringa da quimioterapia moderna, usada para tratar desde leucemias até tumores de mama. Contudo, apesar de décadas de uso, a forma como produzimos esse medicamento é surpreendentemente indireta: a indústria costuma fabricá‑lo a partir de um composto relacionado em vez de permitir que o microrganismo nativo conclua o processo. Este estudo revela por que a bactéria produtora tem dificuldade em completar as etapas químicas finais e mostra como reengenheirar sua maquinaria interna pode aumentar fortemente a produção de doxorrubicina totalmente formada, abrindo caminho para fornecimentos mais confiáveis e potencialmente mais baratos.
De bactérias do solo a um remédio que salva vidas
A doxorrubicina pertence às antraciclinas, uma família de moléculas naturais sintetizadas por bactérias do solo do gênero Streptomyces. Esses compostos compartilham um arcabouço de carbono rígido e plano que se intercala entre os pares de bases do DNA, além de uma unidade de açúcar que se acomoda nas fendas da dupla hélice. Em conjunto, essas características bloqueiam as máquinas que manipulam o DNA da célula e, em última instância, desencadeiam a morte celular — útil contra células cancerosas de rápido crescimento. O produtor clássico, Streptomyces peucetius, naturalmente produz principalmente um fármaco precursor chamado daunorrubicina, e apenas uma quantidade modesta da mais eficaz doxorrubicina, que difere por um único grupo contendo oxigênio a mais. Essa pequena alteração estrutural melhora dramaticamente a atividade, mas mostra‑se surpreendentemente difícil para o microrganismo alcançar de forma eficiente.
Encontrando a fiação elétrica certa dentro da célula
A enzima crucial que realiza as três últimas etapas de oxidação no esqueleto do fármaco chama‑se DoxA, membro da família dos citocromos P450. Como uma pequena fábrica química, a DoxA precisa de um fluxo contínuo de elétrons para ativar o oxigênio e incorporar novos átomos de oxigênio na molécula do fármaco. Dentro da bactéria, esses elétrons são fornecidos por uma cadeia de proteínas auxiliares conhecidas como parceiros redox. O genoma de S. peucetius contém vários candidatos, o que tornava incerto quais realmente emparelham com a DoxA. Ao comparar a atividade gênica e o metabolismo em uma cepa normal, um mutante rico em daunorrubicina e um mutante rico em doxorrubicina, os pesquisadores identificaram um ferredoxina (Fdx4) e uma ferredoxina redutase (FdR3) como os parceiros naturais. Reconstruir esse trio em reações em tubo de ensaio confirmou que a DoxA funciona melhor quando conectada a essa cadeia específica de transferência de elétrons, muito parecido com combinar o adaptador de energia certo com um dispositivo.
Aliviando a desaceleração autoinduzida da enzima
Mesmo com a fiação elétrica correta, a DoxA tende a travar na etapa final que converte daunorrubicina em doxorrubicina. Trabalhos anteriores sugeriram que o próprio produto pode entupir a enzima. A equipe investigou um gene vizinho, dnrV, cuja função era misteriosa. Testes bioquímicos mostraram que a proteína DnrV se liga firmemente a uma variedade de moléculas antraciclínicas, incluindo a doxorrubicina, sem alterá‑las quimicamente. Adicionar DnrV às reações com DoxA melhorou muito o fluxo químico, permitindo a conversão completa dos precursores ao fármaco final enquanto evitava reações colaterais deletérias. Em termos práticos, DnrV age como uma esponja interna que absorve a doxorrubicina recém‑formada, impedindo que ela bloqueie a enzima ou danifique o DNA dentro da célula produtora.
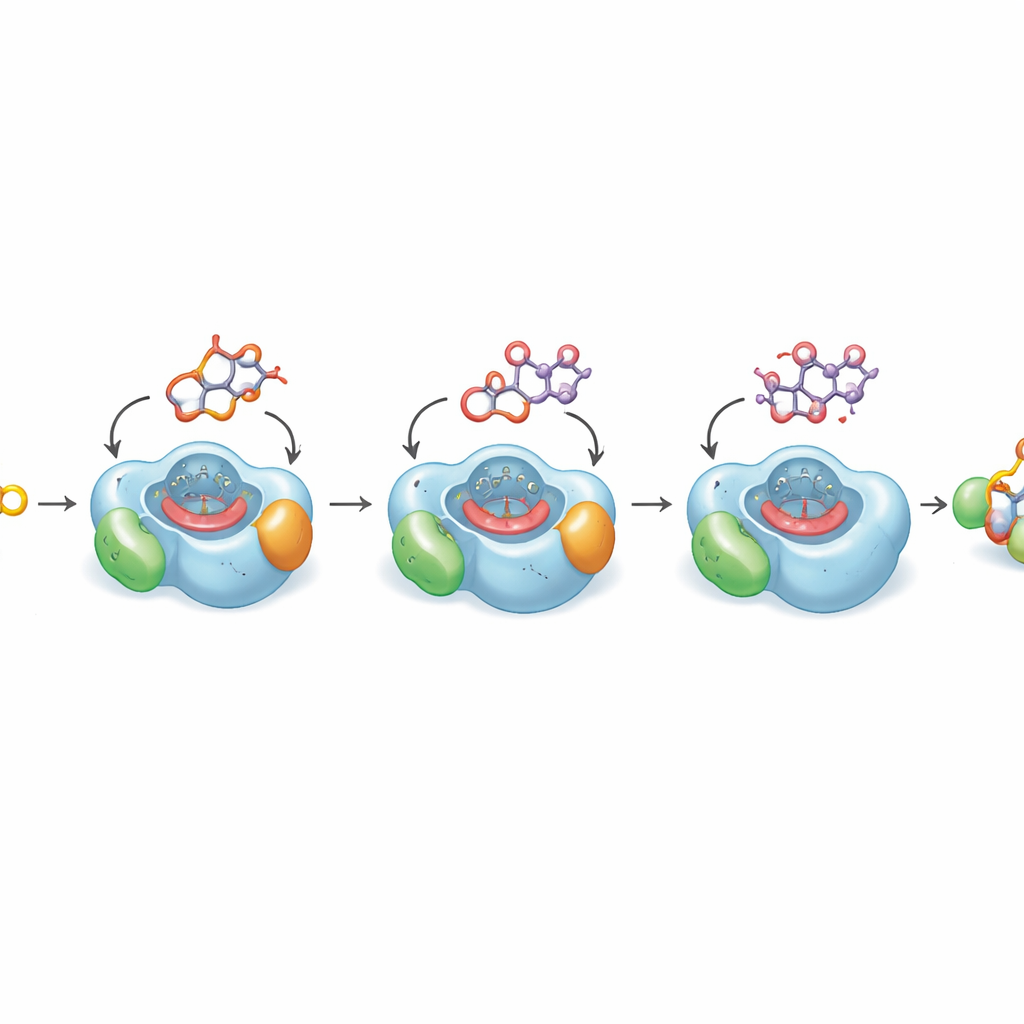
Vendo por que a última etapa é tão lenta
Para entender por que a oxidação final chave é intrinsecamente lenta, os autores resolveram estruturas cristalinas de alta resolução da DoxA ligada a três intermediários sucessivos. Essas estruturas revelam como o núcleo plano do fármaco e seu açúcar ligado se acomodam em um bolso justo acima do grupo heme da enzima, o centro metálico reativo que realiza a oxidação. Para as etapas anteriores, o átomo de carbono que deve ser modificado fica próximo ao heme em uma posição ideal para a reação. Mas, no substrato final, a daunorrubicina, a porção da molécula que precisa ser hidroxilada se dobra para longe do heme em uma pequena cavidade oleosa, um arranjo que cálculos quânticos mostram ser energeticamente favorecido. Simulações computacionais em escalas de tempo de microssegundos confirmam que a molécula só ocasionalmente assume uma pose produtiva para essa última inserção de oxigênio. Esse viés estrutural explica por que a conversão para doxorrubicina é naturalmente ineficiente.
Construindo uma cepa melhor produtora de doxorrubicina
Munidos dessas percepções, os pesquisadores redesenharam racionalmente a bactéria em vez de depender de mutagênese aleatória. Introduziram um gene de reparo de DNA para estabilizar a produção, então instalaram cópias extras de doxA, os parceiros redox ótimos fdx4 e fdr3, e o ligante auxiliar dnrV sob promotores cuidadosamente escolhidos para balancear suas quantidades. Também ajustaram as condições de cultivo e usaram resinas especiais para absorver intermediários tóxicos e pegajosos. Em frascos de laboratório e em um biorreator de 20 litros, a melhor cepa engenheirada produziu 336 miligramas de doxorrubicina por litro de cultura com uma proporção de 81:19 de doxorrubicina para daunorrubicina — um aumento de cerca de 180% em relação à cepa inicial e uma mistura de produto muito mais limpa.
O que isso significa para o fornecimento futuro de medicamentos contra o câncer
Ao dissecar tanto o sistema de suporte elétrico quanto a estrutura 3D de uma enzima-chave, este trabalho explica por que um microrganismo de importância médica tem desempenho inferior na produção da nossa antraciclina mais valiosa. Combinar a DoxA com seus parceiros redox naturais, adicionar uma proteína auxiliar que se liga ao fármaco e reequilibrar a expressão gênica transformaram um produtor relutante em um eficiente. Embora ajustes adicionais na enzima possam acelerar ainda mais a etapa química final, o estudo já aproxima muito a fabricação totalmente biológica da doxorrubicina da realidade industrial. Para pacientes e sistemas de saúde, tais avanços podem se traduzir em acesso mais seguro, escalável e econômico a um fármaco de quimioterapia fundamental.
Citação: Koroleva, A., Artukka, E., Yamada, K. et al. Metabolic engineering of doxorubicin biosynthesis through P450-redox partner optimization and structural analysis of DoxA. Nat Commun 17, 2358 (2026). https://doi.org/10.1038/s41467-026-69194-6
Palavras-chave: produção de doxorrubicina, biossíntese de antraciclinas, engenharia de enzimas, fabricação microbiana de fármacos, citocromo P450