Clear Sky Science · pt
A ativação da proteína quinase C atípica impulsiona a excreção intestinal de glicose no diabetes mellitus
Transformando o Intestino numa Válvula de Açúcar
Pessoas com diabetes convivem com açúcar em excesso circulando no sangue. Cirurgias bariátricas como o bypass gástrico podem normalizar a glicemia de forma surpreendentemente rápida, mesmo antes de ocorrer perda de peso significativa, mas como isso acontece tem sido um mistério. Este estudo revela uma "válvula de açúcar" baseada no intestino — um mecanismo pelo qual o intestino retira glicose do sangue e despeja parte dela de volta no lúmen intestinal — sugerindo um novo alvo farmacológico que poderia imitar os benefícios da cirurgia sem a operação.
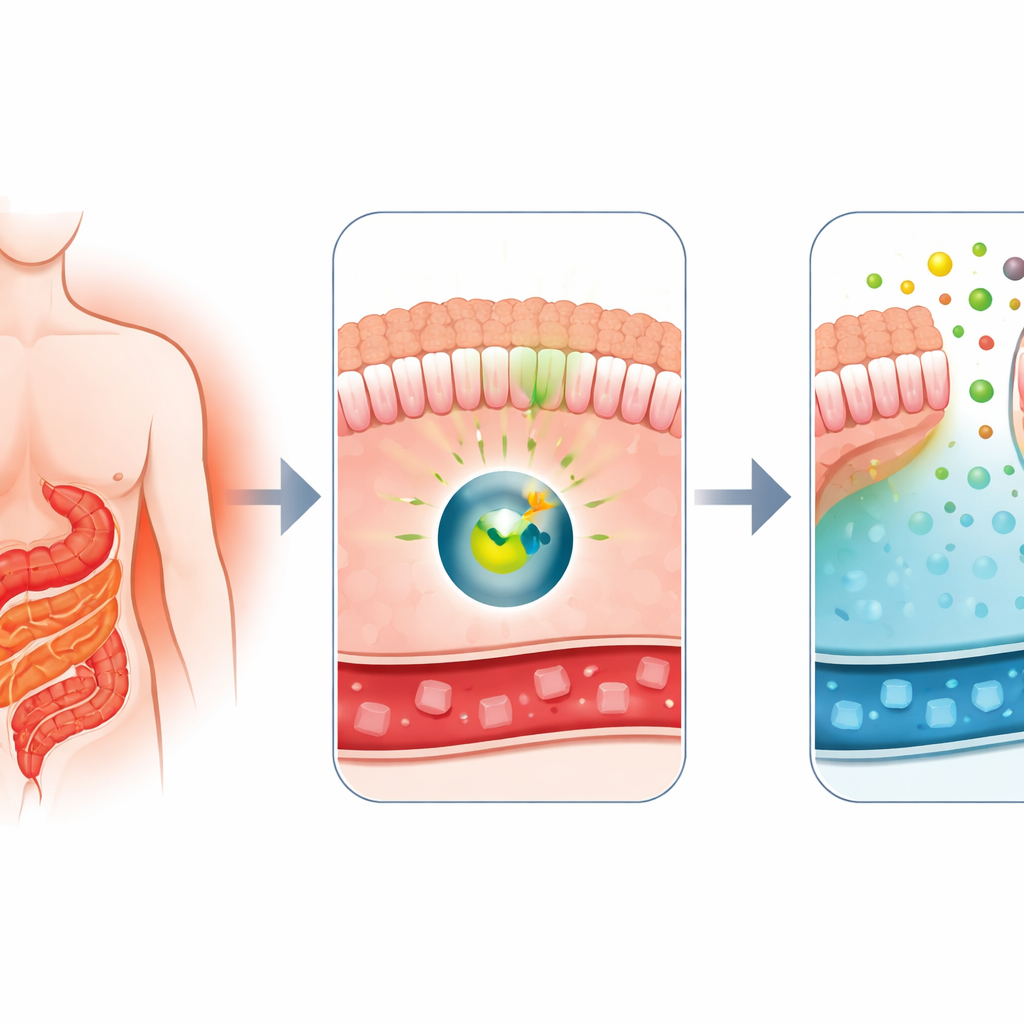
Por que a Cirurgia Muda a Glicemia Tão Rápido
Médicos sabem há muito tempo que o bypass gástrico em Y de Roux, uma cirurgia comum para perda de peso, é também um dos tratamentos mais eficazes para o diabetes tipo 2. Logo após a cirurgia, a glicemia dos pacientes frequentemente melhora dramaticamente, mesmo antes de grande perda de peso. Trabalhos anteriores deste grupo mostraram que, após o bypass, partes do intestino delgado passam a se comportar como uma esponja, absorvendo glicose da corrente sanguínea e liberando parte dela no interior do trato intestinal. Esse comportamento incomum, chamado excreção intestinal de glicose, parecia depender de uma proteína transportadora chamada GLUT1. A grande pergunta era: qual interruptor molecular faz o intestino mudar para esse modo de eliminação de açúcar?
Usando Big Data para Encontrar um Interruptor Molecular
Para procurar esse interruptor, os pesquisadores usaram um sistema computacional de descoberta de drogas em larga escala baseado no Connectivity Map, um banco de dados que reúne como milhares de compostos alteram a atividade gênica em células. Eles compararam padrões de expressão gênica de cinco situações em que a excreção intestinal de glicose é alta — incluindo tecido de ratos operados com bypass e células tratadas com um sinal de crescimento intestinal — com padrões produzidos por drogas conhecidas. Uma classe de compostos destacou-se consistentemente: ativadores da proteína quinase C (PKC), uma família de enzimas que transmitem sinais dentro das células. Ao investigar mais a fundo, a equipe concentrou-se no subgrupo “atípico” das PKC, especialmente uma isoforma chamada PKCζ, cuja atividade em células intestinais mais se assemelhava ao estado tipo bypass capaz de excretar glicose.
A Bomba de Açúcar das Células Intestinais em Ação
Aproximando-se das células intestinais individuais por meio de RNA-seq de célula única, os autores descobriram que a cirurgia de bypass aumenta tanto PKCζ quanto GLUT1 em células específicas absorventes de nutrientes que revestem o intestino delgado distal. Em culturas celulares e organoides intestinais humanos, aumentar artificialmente PKCζ ou tratar com prostratina — um composto de origem vegetal que ativa com segurança essas PKC atípicas — fez com que o GLUT1 chegasse à superfície celular. Lá, o GLUT1 atuou como uma bomba bidirecional: retirou mais glicose do lado voltado para o sangue das células e permitiu que o excesso saísse para o lúmen intestinal. Importante, esse redirecionamento do açúcar não acelerou de forma relevante a queima intracelular de glicose (glicólise), indicando que o efeito principal era a eliminação da glicose, não a produção extra de energia.
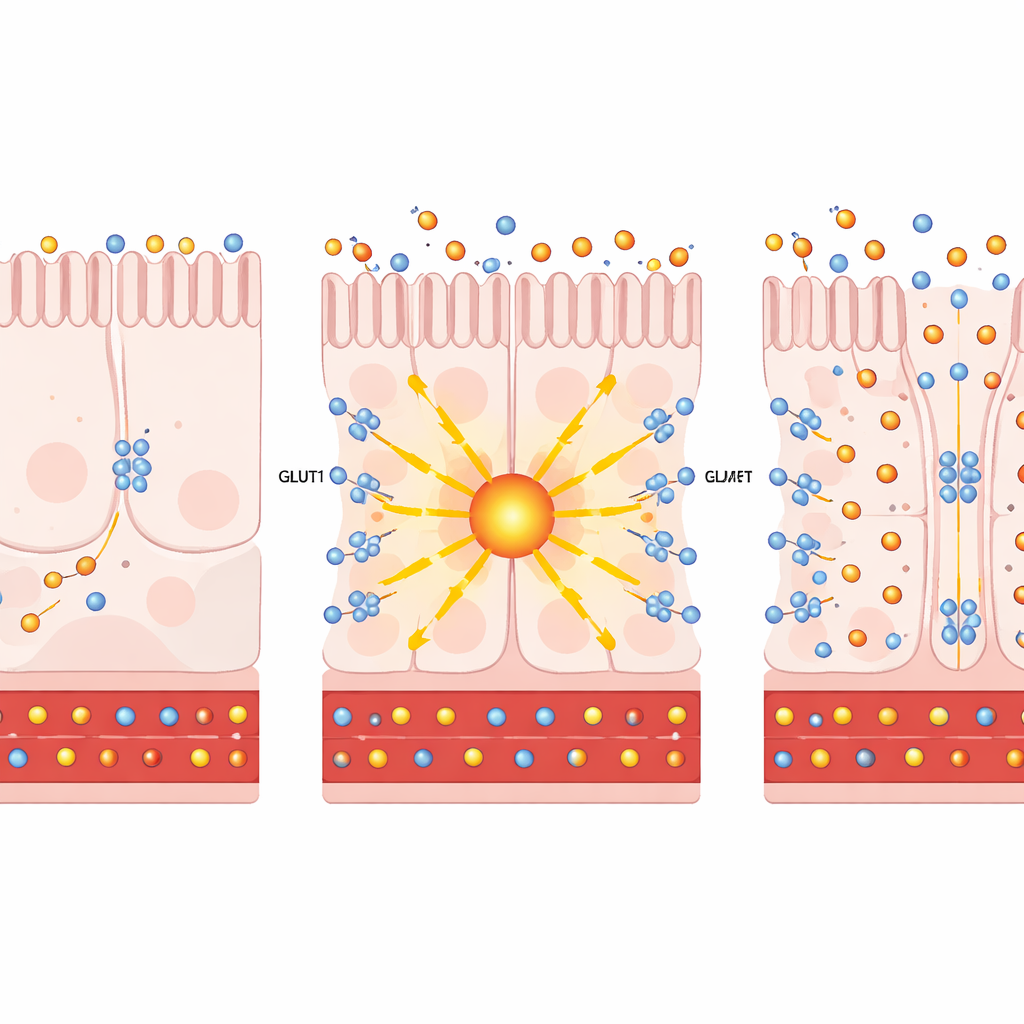
Das Células aos Camundongos: Imitando a Cirurgia Sem Bisturi
Em seguida, a equipe testou se ativar essa via em animais vivos poderia melhorar o diabetes. Em camundongos obesos e resistentes à insulina, entregar PKCζ adicional especificamente ao intestino levou a ganho de peso mais lento, glicemia de jejum mais baixa e melhor tolerância à glicose. Traçadores de açúcar radioativos mostraram mais captação de glicose pelo intestino distal e eliminação no lúmen intestinal. Um quadro semelhante surgiu em modelos murinos diabéticos tratados com prostratina: eles ganharam menos peso, toleraram melhor cargas de glicose e direcionaram mais glicose para o trato intestinal, tudo isso sem alterações nos níveis de insulina, na ingestão alimentar ou na integridade da barreira intestinal. Em cortes de tecido, o GLUT1 apareceu tanto no lado voltado para o sangue quanto no lado voltado para o lúmen, perfeitamente posicionado para puxar glicose da circulação e empurrá-la para o intestino.
O Que Isso Pode Significar para o Cuidado Futuro do Diabetes
Para um público não especializado, a mensagem-chave é que o intestino pode ser convertido em uma rota controlada de escape para o excesso de glicose no sangue. Ao ativar uma enzima específica dentro das células intestinais — a PKC atípica — os pesquisadores conseguiram induzir as células a transportar mais transportadores GLUT1 para sua superfície e comportar-se como um dreno reversível, retirando glicose do sangue e despejando parte dela de volta no intestino. Em camundongos, essa eliminação intestinal de glicose melhorou a glicemia e limitou o ganho de peso sem superestimular a insulina, alterar o apetite ou danificar o intestino. Embora a prostratina e compostos relacionados ainda não sejam medicamentos aprovados para diabetes, este trabalho aponta a via aPKC–GLUT1 como um alvo promissor para futuras terapias que poderiam reproduzir parte dos benefícios metabólicos do bypass gástrico sem exigir cirurgia.
Citação: Kang, C.W., Hong, ZY., Oh, J.H. et al. Atypical protein kinase C activation drives intestinal glucose excretion in diabetes mellitus. Nat Commun 17, 2417 (2026). https://doi.org/10.1038/s41467-026-69193-7
Palavras-chave: excreção intestinal de glicose, diabetes tipo 2, transportador GLUT1, proteína quinase C atípica, prostratina