Clear Sky Science · pt
O sinal autócrino TGFβ1 desencadeado por MerTK regula a resposta microglial à neurodegeneração
Como a equipe de limpeza do cérebro molda a doença
Quando neurônios no cérebro e no nervo óptico morrem, deixam para trás um rastro de detritos. Células imunes especializadas chamadas microglias atuam como a equipe de limpeza do cérebro, engolindo esse resíduo. Mas as microglias fazem mais do que apenas arrumar: a forma como reagem pode proteger os circuitos neurais ou agravar doenças como o Alzheimer. Este estudo revela um circuito oculto de autocomunicação dentro das microglias que é ativado por detritos de fibras nervosas em degeneração e ajuda a determinar a intensidade da resposta dessas células ao dano.
Um gatilho oculto em fibras nervosas moribundas
Para investigar esse processo, os pesquisadores usaram um modelo de camundongo no qual o nervo óptico é esmagado, fazendo com que as longas projeções dos neurônios oculares degenerem sem matar os corpos celulares. Isso isola de forma limpa as consequências da degradação do axônio. Na superfície dessas fibras em degeneração, uma molécula gordurosa vira para fora, atuando como um sinal de “me coma” para as microglias nas proximidades. Esses sinais são detectados por um receptor nas microglias chamado MerTK, um membro de uma pequena família de proteínas que reconhecem detritos. Ao deletar seletivamente MerTK nas microglias, a equipe mostrou que, sem esse receptor, as microglias não montavam sua resposta habitual à lesão: dividiam-se menos, migravam menos e ativavam menos genes ligados ao controle de dano e à inflamação.
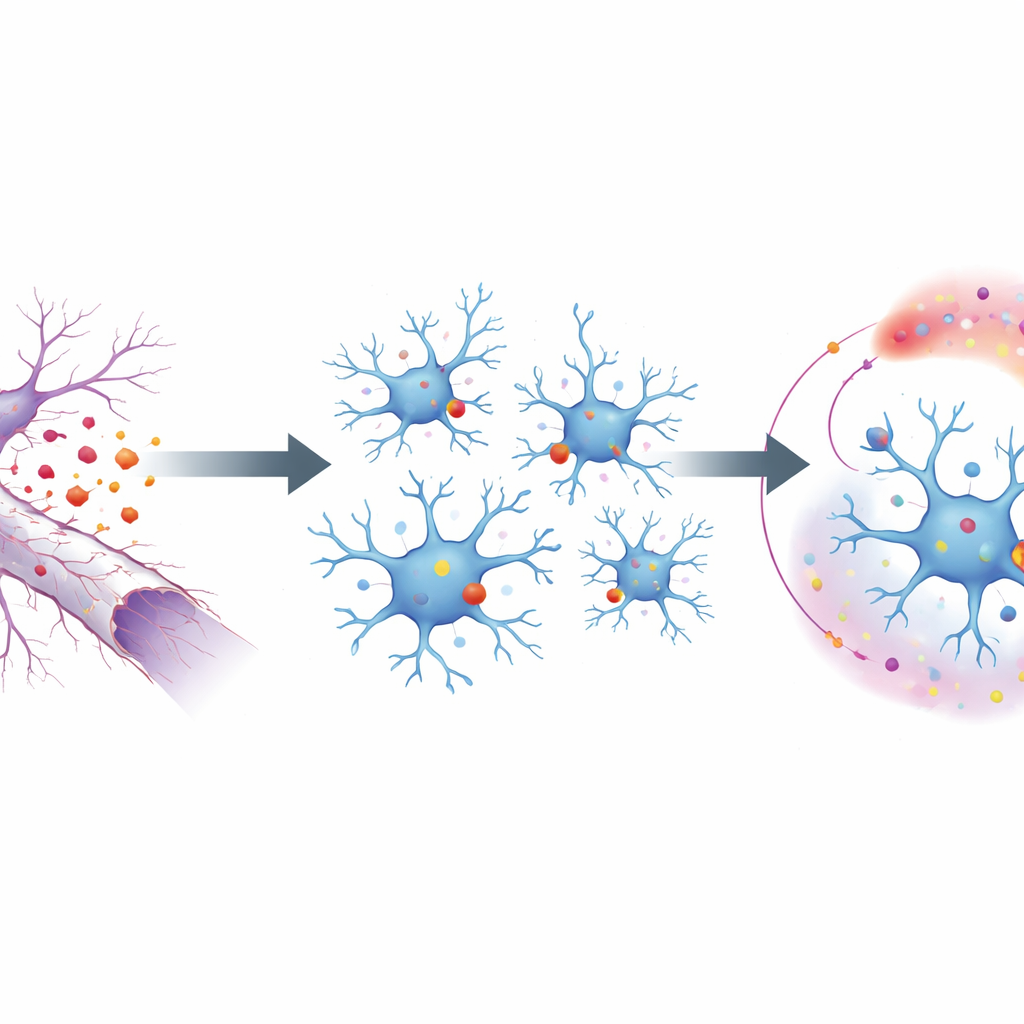
Do sinal de superfície à reprogramação genética
Ao olhar dentro das microglias, os cientistas traçaram como o sinal de superfície de MerTK é convertido em mudanças na atividade gênica. Eles descobriram que MerTK ativa um retransmissor molecular chamado fosfolipase C, que por sua vez aumenta dois controladores mestres no núcleo, PU.1 e IRF8. Esses fatores atuam como supervisores na linha de montagem microglial, ligando muitos genes necessários para um estado ativado. Usando mapas de ligação ao DNA, a equipe descobriu que PU.1 e IRF8 se ligam diretamente a um sítio específico no gene que codifica TGFβ1, uma potente proteína de sinalização. Quando esse sítio de ligação foi mutado para que os supervisores não pudessem mais ancorar ali, as microglias em nervos lesionados não conseguiram aumentar a produção de TGFβ1, embora outras funções basais permanecessem intactas.
Um laço de autorreforço nas microglias
A próxima questão foi o que o TGFβ1 realmente faz nesse contexto. O estudo mostra que as microglias produzem TGFβ1 e então respondem a ele mesmas, formando um circuito autócrino, ou de auto-feedback. Quando TGFβ1 ou seus receptores foram removidos geneticamente apenas das microglias, a lesão ainda causou degeneração axonal, mas as microglias não exibiram mais seu programa completo de ativação. Elas proliferaram menos e expressaram menos genes de resposta a danos e inflamatórios, embora muitos marcadores de identidade homeostática continuassem suprimidos por outros sinais. Uma molécula chave a jusante da sinalização TGFβ, chamada SMAD2 fosforilada, apareceu especificamente nos núcleos microgliais após a lesão e praticamente desapareceu quando TGFβ1 ou seus receptores foram nocauteados, confirmando que o circuito de auto-feedback foi interrompido.
Do nervo óptico de camundongo aos cérebros de Alzheimer
Para testar se essa via importa além de um modelo de lesão artificial, os autores examinaram um modelo de camundongo amplamente usado para doença de Alzheimer. Nesses animais, microglias agrupadas em torno de placas amiloides exibiram altos níveis de PU.1, IRF8, TGFβ1 e sinalização TGFβ ativada, ecoando as descobertas no nervo óptico. A equipe então recorreu a dados humanos de sequenciamento de RNA de núcleo único de tecido cerebral de pacientes com Alzheimer. Lá, as microglias se destacaram como as principais células que expressam os homólogos humanos de MerTK, PU.1, IRF8 e TGFB1. Em seções de cérebro pós‑mortem de pacientes, as microglias também mostraram fortes sinais de sinalização TGFβ ativa, em contraste com tecido de doadores controle. Em conjunto, essas observações sustentam que o mesmo circuito de autocomunicação opera na doença humana.
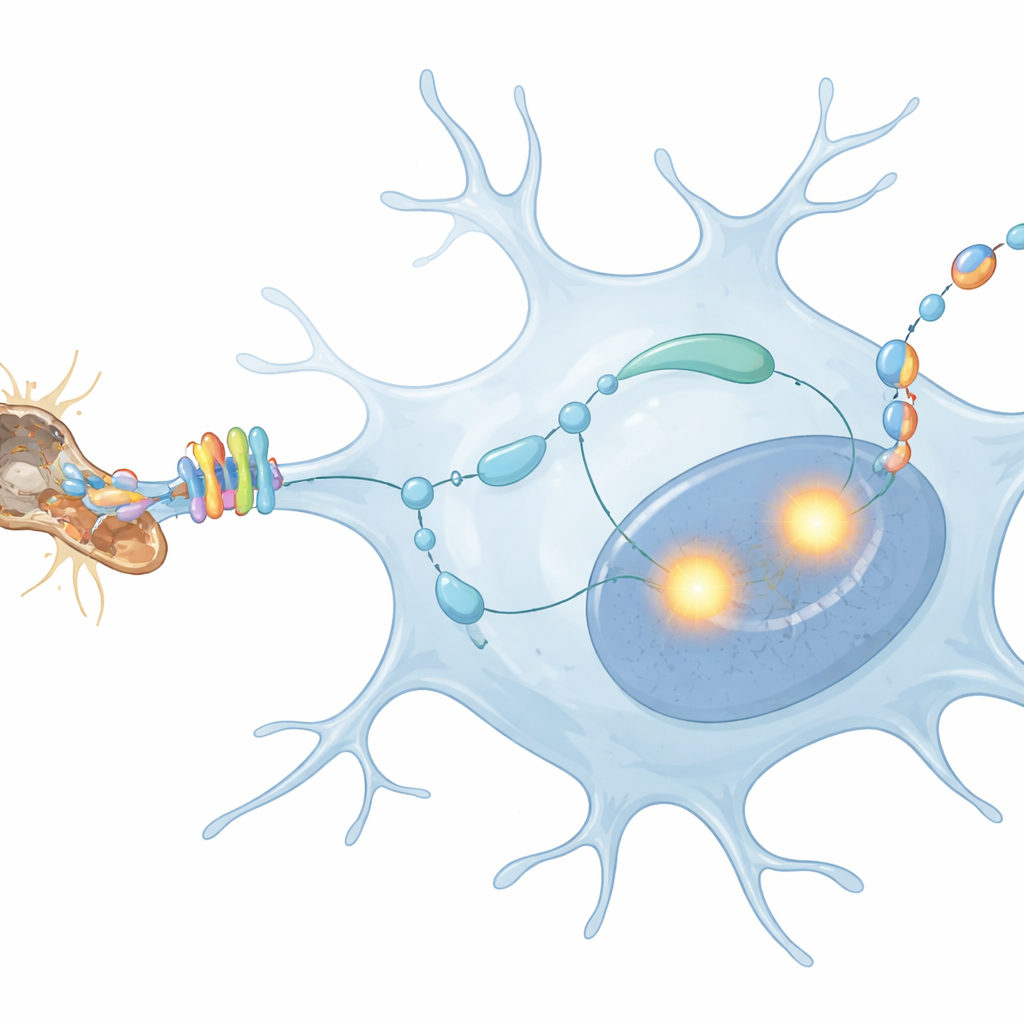
Por que essa conversa interna importa para a saúde cerebral
Este trabalho revela uma cadeia de eventos em que detritos de fibras nervosas em degeneração ativam MerTK nas microglias, que então aumentam PU.1 e IRF8, os quais por sua vez induzem as microglias a produzir TGFβ1 que retorna para elas mesmas. Essa auto‑conversa aguça e sustenta sua resposta à neurodegeneração. Para um leitor leigo, a mensagem principal é que as células faxineiras do cérebro não são apenas agentes passivos de limpeza; elas escutam ativamente seus próprios sinais, e esse laço de feedback pode influenciar se suas ações ajudam a proteger os neurônios ou aceleram doenças como o Alzheimer. Entender e possivelmente modular esse circuito pode abrir novas vias para moderar inflamações prejudiciais mantendo a limpeza benéfica que as microglias proporcionam.
Citação: Huang, Y., Deng, Z., Zhou, Z. et al. MerTK-triggered TGFβ1 autocrine signal regulates microglial response to neurodegeneration. Nat Commun 17, 2312 (2026). https://doi.org/10.1038/s41467-026-69189-3
Palavras-chave: microglia, neurodegeneração, doença de Alzheimer, inflamação cerebral, sinalização TGF-beta