Clear Sky Science · pt
O mecanismo de bombeamento de Na+ impulsionado por redox na NADH-quinona oxidoredutase de Vibrio cholerae depende de mudanças conformacionais dinâmicas
Como a usina de energia do cólera virou alvo de medicamentos
A bactéria que causa o cólera, Vibrio cholerae, sobrevive e se multiplica fazendo funcionar uma minúscula usina molecular na membrana celular. Este estudo revela, com detalhes sem precedentes, como um de seus motores-chave — uma enzima chamada Na⁺-NQR — muda de forma enquanto bombeia íons sódio para fora da célula. Compreender essa máquina molecular não apenas satisfaz a curiosidade básica sobre como a vida converte alimento em energia utilizável, mas também aponta novas maneiras de projetar antibióticos que desativem bactérias nocivas sem afetar células humanas.
Um motor movido a sódio em bactérias
Muitas bactérias marinhas e patogênicas dependem da Na⁺-NQR como o primeiro passo em sua cadeia respiratória, a série de reações que extrai energia dos nutrientes. A Na⁺-NQR localiza-se na membrana interna e retira elétrons de uma molécula combustível chamada NADH, transferindo-os por uma cadeia de moléculas “auxiliares” coloridas (chamadas cofatores) até a quinona, outra pequena molécula embutida na membrana. À medida que os elétrons fluem, a enzima usa essa energia para empurrar íons sódio (Na⁺) do interior da célula para o exterior, criando um gradiente de sódio. Esse gradiente é como uma bateria carregada: alimenta o motor flagelar bacteriano para natação, ajuda a produzir ATP (a moeda de energia da célula) e dirige a captação de nutrientes e a expulsão de drogas. Como a Na⁺-NQR existe apenas em bactérias e é muito diferente da enzima relacionada em nossas mitocôndrias, ela é um alvo atraente para antibióticos altamente seletivos.
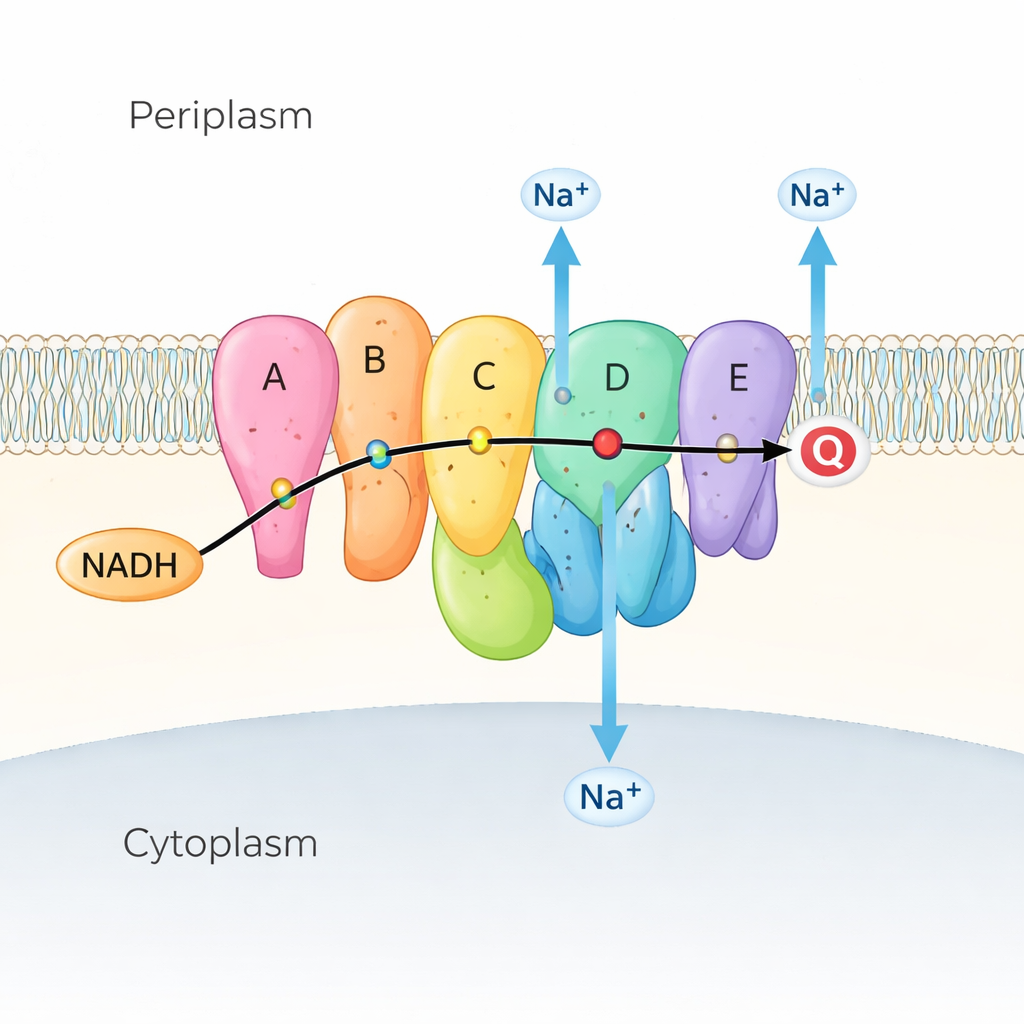
Observando a máquina em movimento
Snapshots anteriores por raios X e crio-microscopia eletrônica mostraram onde os subunidades e cofatores da Na⁺-NQR ficam, mas também revelaram um enigma: alguns saltos eletrônicos críticos estavam muito distantes para que os elétrons se movessem eficientemente, a menos que a proteína mudasse de forma. Os autores enfrentaram isso capturando a Na⁺-NQR em muitas condições ligeiramente diferentes. Eles usaram mutantes que removem cofatores específicos, fármacos que atolam a reação em estágios particulares e soluções com e sem sódio. Com crio-EM de alta resolução e análise de imagem avançada, eles conseguiram separar e reconstruir múltiplas conformações da mesma enzima, transformando snapshots estáticos em um filme de seu ciclo de trabalho.
Um braço flexível e uma braçadeira que se desloca
Uma descoberta-chave envolve uma subunidade citoplasmática flexível, NqrF, que portam dois cofatores que carregam elétrons. A equipe identificou três posições para seu domínio “semelhante à ferredoxina” — apelidadas de estados “up” (acima), “middle” (intermediário) e “down” (abaixo). No raro mas crucial estado “down”, esse pequeno domínio balança para dentro de um bolso formado por duas subunidades de membrana, NqrD e NqrE, aproximando seu cluster ferro-enxofre o suficiente para transferir um elétron adiante. Enquanto isso, uma subunidade periplásmica (externa) chamada NqrC comporta-se como uma braçadeira móvel. Em uma conformação (“estável”), ela se apoia contra outra subunidade de membrana, NqrB, posicionada para passar elétrons em direção ao aceitador quinona final. Em uma segunda conformação (“deslocada”), NqrC move-se em direção a NqrD/E, aproximando seu cofator flavina para aceitar um elétron do centro ferro-enxofre deles. Esses movimentos mostram que NqrF e NqrC atuam como mensageiros dinâmicos, conectando grandes lacunas na cadeia de cofatores.
Como mudanças de forma bombeiam sódio
O coração da bomba de sódio reside nas subunidades emparelhadas NqrD e NqrE, que formam um feixe central de hélices transmembrana. Usando tanto estruturas quanto simulações de dinâmica molecular em nível atômico, os autores mostram que quando o cluster ferro-enxofre em NqrD/E é reduzido (ganha um elétron), ele cria um sítio carregado negativamente que atrai um íon Na⁺ e algumas moléculas de água do lado citoplasmático, formando um bolso de ligação transitório. Aminoácidos hidrofóbicos acima e abaixo desse bolso comportam-se como portões interno e externo, controlando o acesso ao íon. Quando NqrD/E mudam de uma forma “aberta para dentro” para uma forma “aberta para fora”, o Na⁺ move-se em direção ao lado periplásmico e é eventualmente liberado conforme o cluster ferro-enxofre é reoxidados. Simulações mostram o Na⁺ permanecendo parcialmente hidratado, mas nunca vendo um túnel contínuo cheio de água, sugerindo que a enzima é fortemente vedada contra vazamentos indesejados de prótons.
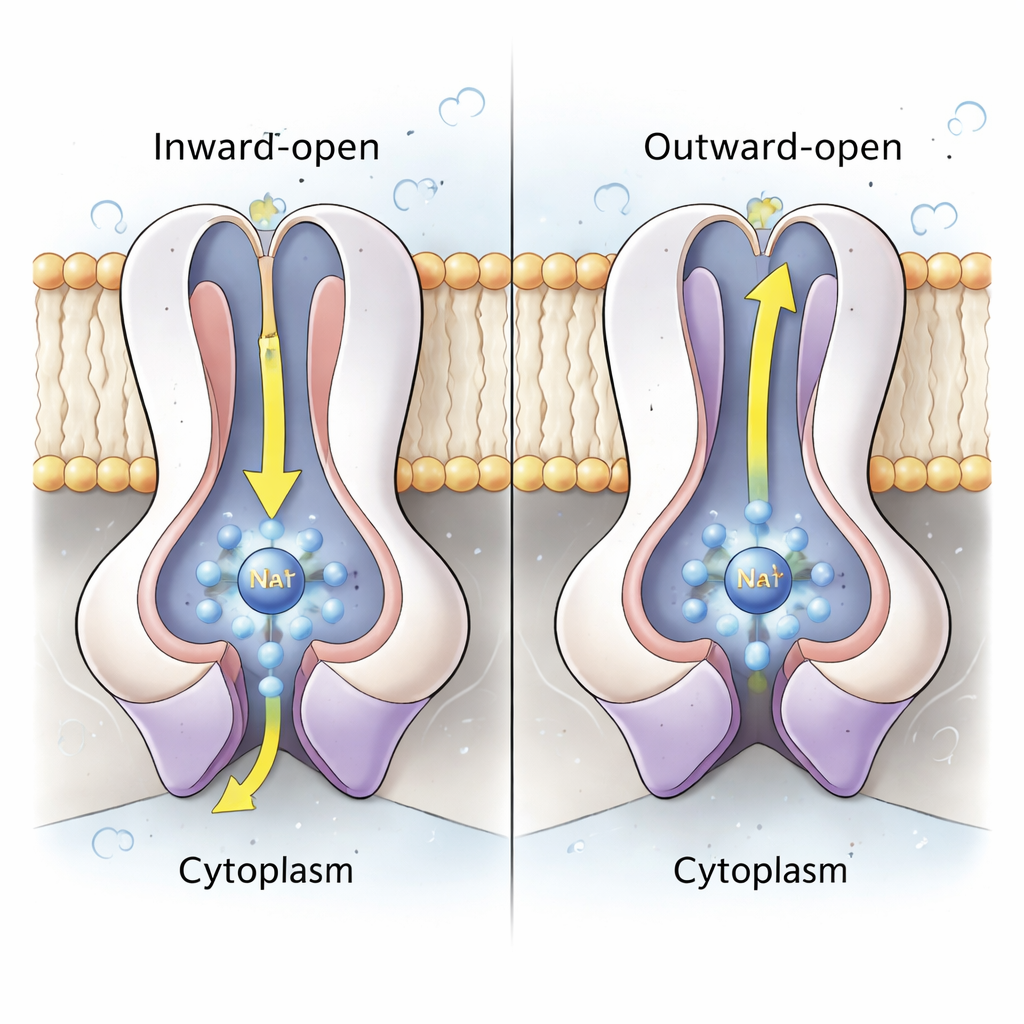
Um ciclo coordenado que trava a direção
Ao combinar todos os seus estados estruturais e simulações, os pesquisadores propõem um ciclo de seis passos. Primeiro, o NADH se liga e doa elétrons para NqrF, que então passa um elétron para NqrD/E, desencadeando a captação de Na⁺ do citoplasma e carregando o bolso central. A consequente mudança conformacional de NqrD/E para a forma aberta para fora tanto expulsa Na⁺ para a periplasma quanto incentiva NqrC a mover-se para aceitar o elétron. Passos subsequentes transferem elétrons ao cofator flavina final e ao riboflavina e, finalmente, para a quinona, que deve receber dois elétrons para tornar-se quinol. Importante, as mesmas mudanças de forma que movem o Na⁺ também afrouxam e enrijecem alternadamente NqrF e NqrC, tornando o fluxo de elétrons para frente provável apenas quando Na⁺ está sendo bombeado para fora e desencorajando escorregamento reverso. Esse acoplamento ajuda a enzima a bombear Na⁺ contra um gradiente já existente, mantendo a “bateria” bacteriana carregada.
Por que isso importa para a medicina e a biologia
Para um público não especializado, este trabalho mostra como a vida constrói máquinas coreografadas com precisão a partir de proteínas, onde pequenas mudanças de carga disparam grandes movimentos úteis. Para a pesquisa em doenças infecciosas, fica claro que a translocação de Na⁺ na Na⁺-NQR ocorre principalmente através do núcleo NqrD/E, e não pela subunidade NqrB anteriormente suspeita. Esse insight refina onde futuros fármacos devem se ligar para melhor interromper o motor que alimenta Vibrio cholerae e outros patógenos, poupando as enzimas humanas. Mais amplamente, o estudo fornece um plano estrutural de como reações de oxirredução podem ser conectadas ao bombeamento iônico — um princípio de projeto que a natureza reutiliza em muitas formas de máquinas bioenergéticas.
Citação: Ishikawa-Fukuda, M., Seki, T., Kishikawa, Ji. et al. The redox driven Na+-pumping mechanism in Vibrio cholerae NADH-quinone oxidoreductase relies on dynamic conformational changes. Nat Commun 17, 1394 (2026). https://doi.org/10.1038/s41467-026-69182-w
Palavras-chave: bomba de sódio, respiração bacteriana, Na+-NQR, crio-EM, alvos antibióticos