Clear Sky Science · pt
hnRNPM coopera com BCAS2 para modular o splicing alternativo durante o desenvolvimento do ovócito
Por que a qualidade do óvulo importa
Toda vida humana começa com uma única célula-ovo, ainda que os cientistas continuem desvendando como essas células extraordinariamente grandes se preparam para o momento da fertilização. Muito antes de o espermatozoide chegar, os ovócitos em crescimento acumulam milhares de moléculas de RNA que orientarão sua maturação e os primeiros dias do desenvolvimento do embrião. Este estudo revela como uma proteína pouco conhecida, em conjunto com uma parceira, edita cuidadosamente essas mensagens nos óvulos de camundongo — e o que acontece quando esse sistema de edição falha.
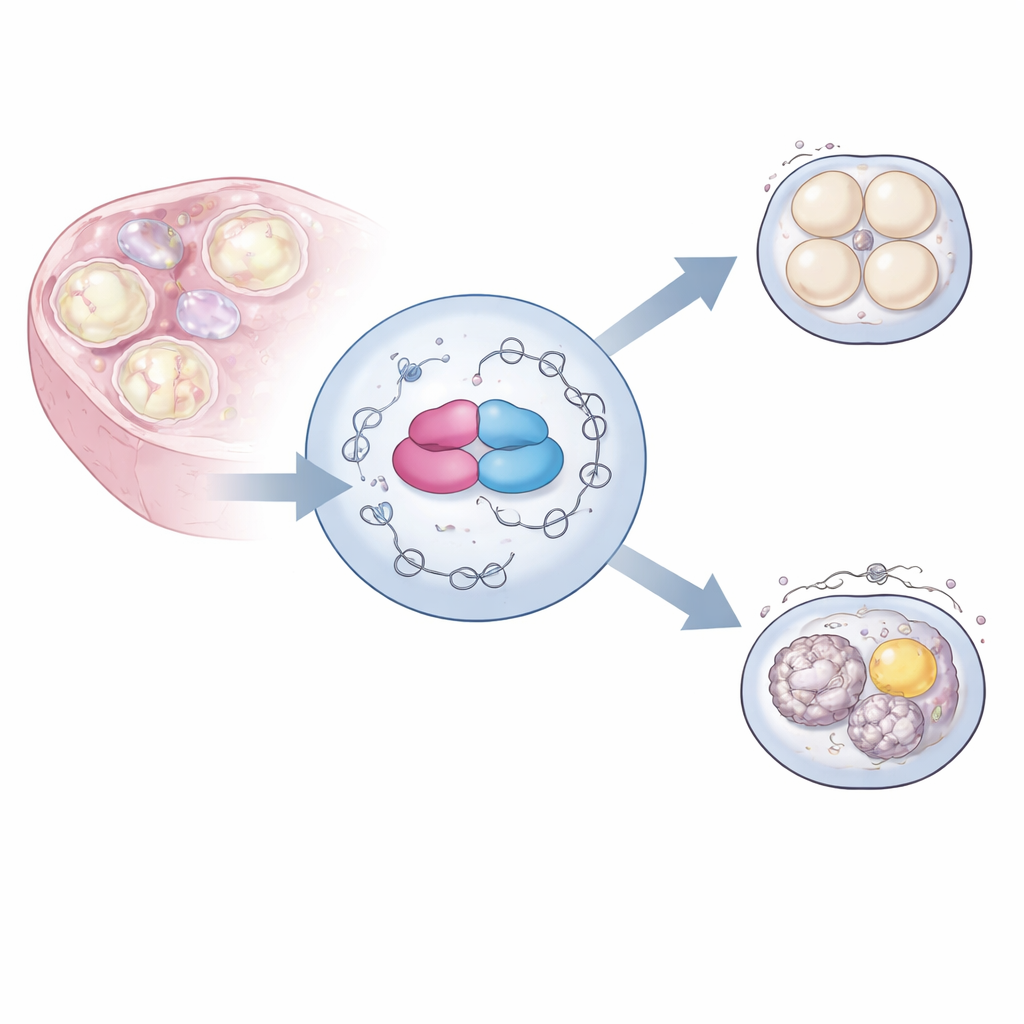
Guardas das mensagens genéticas
Os óvulos crescem no ovário por semanas enquanto seu DNA permanece em grande parte silencioso. Durante esse período, eles acumulam uma vasta biblioteca de mensagens de RNA materno copiadas do genoma anteriormente. Essas mensagens precisam ser aparadas e costuradas de maneiras diferentes, um processo chamado splicing alternativo, para produzir a mistura correta de variantes proteicas nos estágios adequados. Os autores concentraram-se em uma proteína chamada hnRNPM, parte de uma grande família que se liga ao RNA, e em sua parceira BCAS2, ambas abundantes no sistema reprodutor feminino. Trabalhos anteriores sugeriam que essas proteínas se ligam a muitos RNAs nos ovócitos, mas seu papel preciso na fertilidade permanecia incerto.
O que dá errado sem esse editor
Para investigar a função de hnRNPM, a equipe usou engenharia genética para remover o gene Hnrnpm especificamente dos precursores dos óvulos de camundongo. Os ovários dessas fêmeas pareciam normais e produziram números semelhantes de óvulos em comparação com controles. Ainda assim, quando esses óvulos foram fertilizados em laboratório, quase nunca se desenvolveram além das primeiras divisões, tornando as fêmeas completamente inférteis. Uma inspeção mais detalhada dos óvulos imaturos revelou aglomerados escuros no citoplasma normalmente claro. Microscopia eletrônica mostrou que um fino andaime interno chamado grade citoplasmática estava em grande parte ausente, e organelas-chave como mitocôndrias e gotículas de gordura estavam anormalmente agrupadas, em vez de distribuídas uniformemente. Essas alterações indicaram um problema profundo na organização interna do óvulo.
Maquinaria de divisão celular comprometida
Os mesmos óvulos mutantes também tiveram dificuldade para completar a meiose, a divisão celular especial que reduz o número de cromossomos pela metade. Quando os pesquisadores amadureceram os óvulos em cultura, eles podiam iniciar a meiose, mas geralmente travavam antes de concluí-la. Ao microscópio, as estruturas que separam os cromossomos — os fusos — estavam torcidas, multipolares ou mal ancoradas. Uma proteína chamada pericentrina, que ajuda a organizar os polos do fuso, aparecia tardiamente e nos locais errados. Juntos, esses defeitos faziam com que os óvulos não conseguissem alinhar e separar os cromossomos de maneira confiável, uma provável causa da falha completa de desenvolvimento após a fertilização.
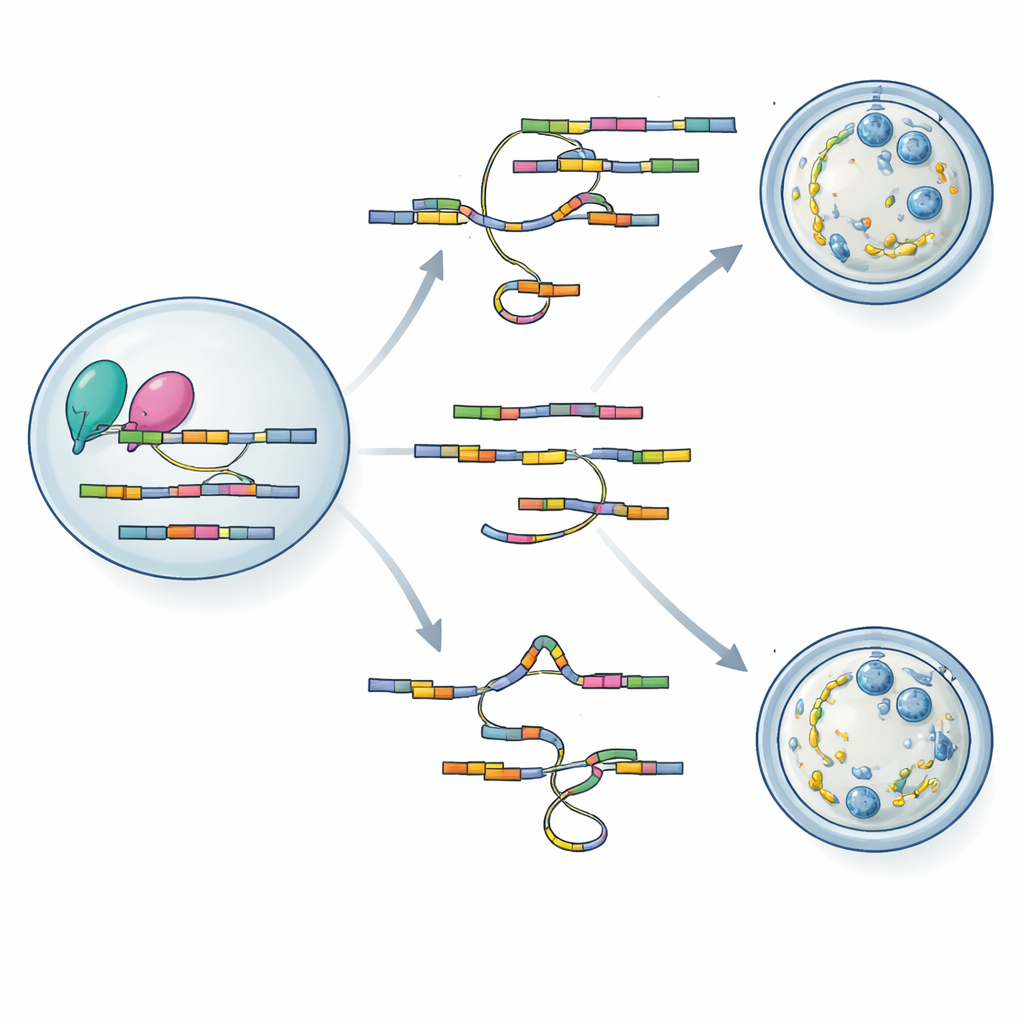
Lendo e reescrevendo instruções de RNA
Para entender como a perda de hnRNPM leva a defeitos tão abrangentes, a equipe recorreu a duas poderosas ferramentas de sequenciamento adaptadas para amostras microscópicas de óvulos. Usando SCAN-seq, que lê moléculas de RNA em comprimento total de óvulos individuais, descobriram mais de mil mudanças de splicing nos óvulos mutantes, incluindo muitas variantes de RNA até então desconhecidas. Genes envolvidos na construção da grade citoplasmática, no controle do comportamento dos fusos e na regulação do ciclo meiótico foram especialmente afetados. Um segundo método, LACE-seq, mapeou exatamente onde hnRNPM se liga aos RNAs, revelando preferência por trechos ricos em GU dentro de éxons. Ao sobrepor os dois conjuntos de dados, os autores mostraram que hnRNPM se posiciona diretamente sobre muitas das mensagens cujo splicing muda quando a proteína está ausente, vinculando sua atividade de ligação à precisão do splicing.
Um modelo de trabalho em equipe para o controle do óvulo
Estudos de interação proteica demonstraram que hnRNPM se associa fisicamente a BCAS2 e a componentes centrais da maquinaria de splicing. As duas parceiras se ligam a muitos dos mesmos alvos de RNA e frequentemente os alteram da mesma forma quando qualquer uma das proteínas é perturbada. Intrigantemente, a perda de hnRNPM reduziu os níveis de proteína BCAS2 e enfraqueceu a fixação de BCAS2 sobre alvos de RNA compartilhados, sugerindo que hnRNPM não apenas edita mensagens, mas também ajuda a estabilizar sua parceira nesses alvos. Os autores propõem um modelo no qual hnRNPM e BCAS2 formam um complexo cooperativo que ajusta RNAs maternos-chave durante o crescimento do ovócito, garantindo a montagem adequada da grade citoplasmática e divisões meióticas confiáveis.
O que isso significa para a fertilidade
Em termos simples, este trabalho demonstra que uma equipe molecular de edição — hnRNPM e BCAS2 — atua nos bastidores para preparar os óvulos para a vida após a fertilização. Quando essa equipe está ausente, a estrutura interna do óvulo desaba, sua maquinaria de classificação de cromossomos falha, e embora o óvulo seja produzido em números normais, ele não consegue sustentar o desenvolvimento embrionário. Como hnRNPM é altamente semelhante em camundongos e humanos, essas descobertas apontam para um sistema conservado de controle de qualidade que pode estar na raiz de certas formas de infertilidade feminina inexplicada e oferecer novos pontos de entrada para diagnóstico ou tratamento.
Citação: Zhou, S., Liu, D., Gan, S. et al. hnRNPM cooperates with BCAS2 to modulate alternative splicing during oocyte development. Nat Commun 17, 2681 (2026). https://doi.org/10.1038/s41467-026-69176-8
Palavras-chave: desenvolvimento do ovócito, splicing alternativo, infertilidade feminina, proteínas de ligação ao RNA, grade citoplasmática