Clear Sky Science · pt
Conjuntos em resolução atômica de proteínas intrinsecamente desordenadas com AlphaFold
Por que proteínas camaleônicas importam
Nossas células estão cheias de proteínas que nunca se fixam em uma única forma rígida. Essas proteínas “intrinsecamente desordenadas” comportam-se mais como macarrão flexível do que como máquinas bem dobradas, e ainda assim são centrais em processos que vão desde o sinal celular até doenças neurodegenerativas. Como elas estão em constante movimento e flexão, capturar toda a sua gama de formas em detalhe atômico é extremamente difícil e geralmente exige anos de experimentos e cálculos intensivos. Este artigo apresenta uma nova forma de aproveitar a inteligência artificial e a física em conjunto para mapear essas moléculas inquietas de maneira muito mais eficiente.
O desafio das moléculas inquietas
Ao contrário dos modelos didáticos de proteínas que mostram uma estrutura arrumada, as proteínas intrinsecamente desordenadas (IDPs) vagueiam por uma vasta paisagem de formas possíveis. Essa flexibilidade as ajuda a reconhecer muitos parceiros diferentes, mas também as torna notoriamente difíceis de estudar. Técnicas laboratoriais tradicionais, como ressonância magnética nuclear avançada e espalhamento de raios X, podem informar médias sobre muitas conformações, mas não cada forma individual. Simulações computacionais em detalhe atômico podem, em princípio, seguir cada átomo enquanto uma IDP se contorce, porém são extremamente custosas e dependem de modelos físicos finamente ajustados. Como resultado, a comunidade científica dispõe apenas de um conjunto limitado de ensembles precisos e detalhados de IDPs para aprender.
Combinando palpites inteligentes com regras físicas
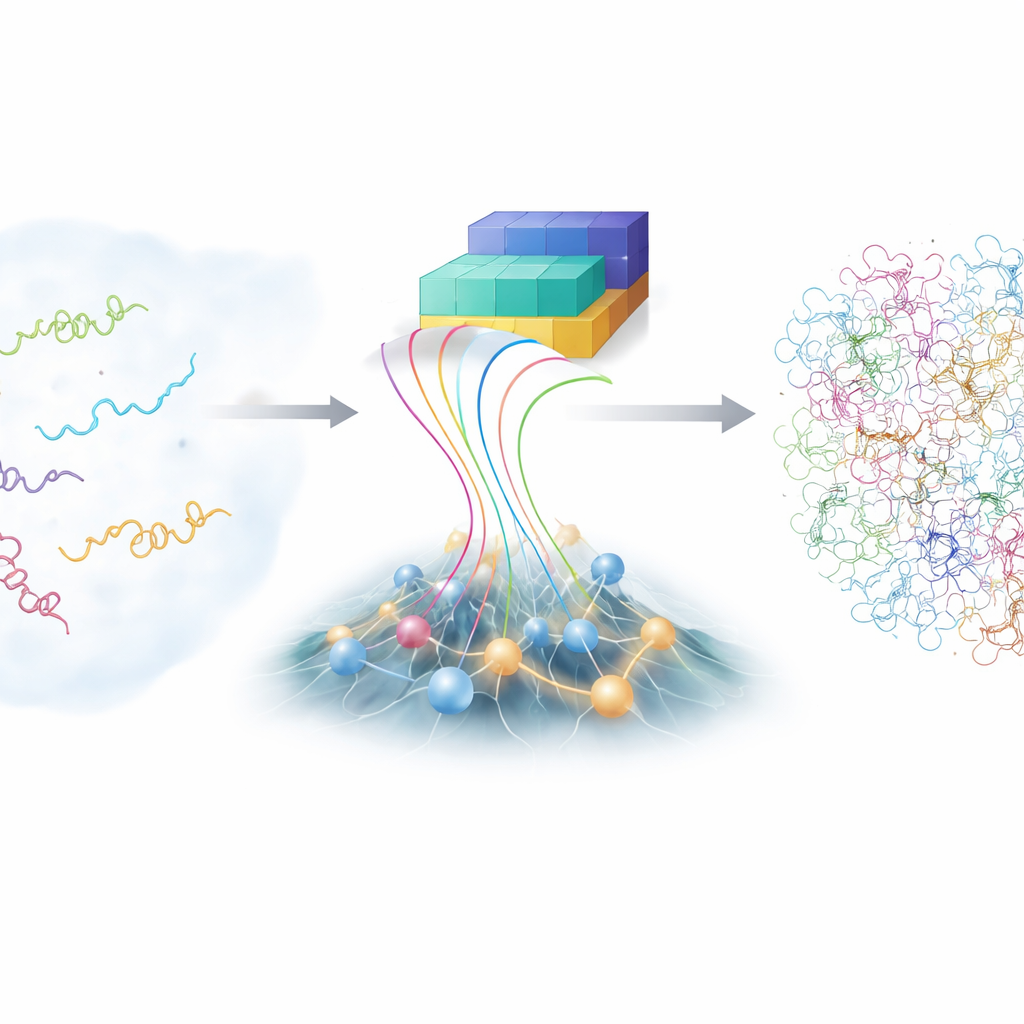
Nos últimos anos, a família AlphaFold de ferramentas de aprendizado profundo surpreendeu a biologia ao prever estruturas de proteínas a partir de suas sequências de aminoácidos. Para proteínas desordenadas, porém, a força habitual do AlphaFold—estimar uma única melhor forma—é menos útil, porque as IDPs não têm apenas uma. O que o AlphaFold fornece, entretanto, é informação rica sobre quão prováveis são as diferentes partes da cadeia estarem próximas ou distantes umas das outras. Os autores construíram uma nova estrutura, chamada bAIes, que trata essa informação derivada da IA como uma orientação suave e a combina com um modelo físico rápido que deliberadamente parte de uma visão de “bobina aleatória”, onde a cadeia explora todas as possíveis dobras e torções sem favorecer qualquer estrutura particular.
De emaranhados aleatórios a ensembles realistas
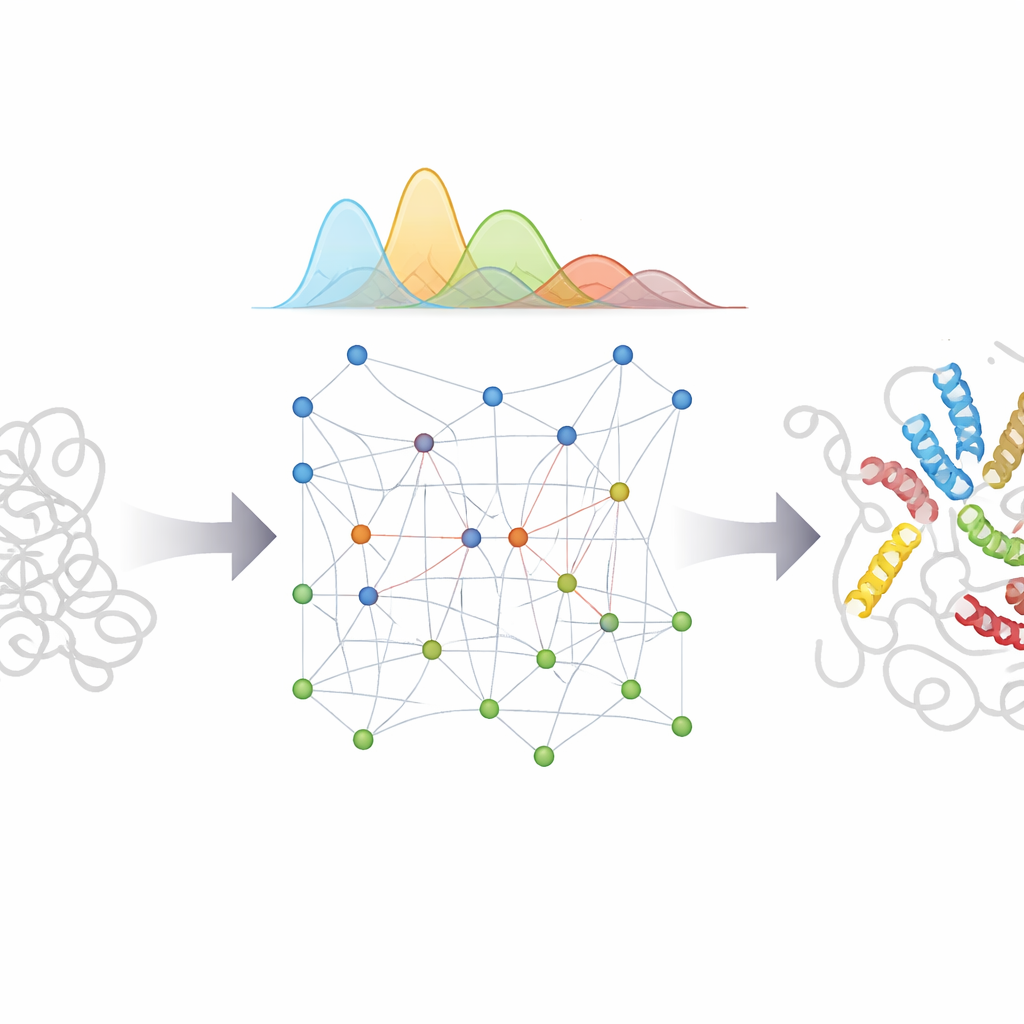
Primeiro, os pesquisadores construíram um modelo físico eficiente que reproduz como uma cadeia proteica completamente não estruturada se comporta, com base em estatísticas extraídas de milhares de estruturas proteicas conhecidas. Esse modelo serve como o “prior” — a expectativa básica de como uma IDP se move se não soubermos mais nada. Em seguida, o bAIes lê as previsões do AlphaFold sobre quais pares de resíduos tendem a se aproximar. Em vez de forçar a proteína a adotar um único padrão, ele converte esses indícios em restrições de distância suaves com incerteza incorporada, permitindo que a cadeia satisfaça as sugestões da IA somente quando elas forem consistentes com o quadro físico mais amplo.
Testando contra experimentos reais
Para verificar se essa abordagem funciona, a equipe aplicou o bAIes a um conjunto de 21 proteínas que variavam desde bobinas quase totalmente aleatórias até sistemas mais complexos com hélices transitórias e múltiplos domínios. Para cada uma, compararam os ensembles gerados por computador com uma ampla variedade de medidas experimentais que sondam tanto detalhes locais quanto tamanho e forma globais. Para proteínas muito flexíveis, como o peptídeo Aβ40 relacionado ao Alzheimer, o simples modelo de bobina aleatória já estava próximo da realidade, e o bAIes preservou esse bom acordo. Para proteínas parcialmente estruturadas, o bAIes melhorou a correspondência com os experimentos ao captar corretamente onde segmentos helicoidais curtos e regiões compactas surgem e desaparecem. De modo crucial, o método manteve-se robusto mesmo quando o AlphaFold estava excessivamente confiante e previra equivocadamente dobras estáveis onde experimentos em solução mostram desordem, porque o bAIes permite explicitamente erros na entrada da IA.
Superando ou igualando métodos existentes
Os autores então confrontaram o bAIes com simulações all-atom de alto custo rodadas em supercomputadores especializados, modelos coarse-grained que simplificam proteínas em esferas, e novos geradores de aprendizado profundo treinados em dados de simulação. Em múltiplos testes, o bAIes consistentemente igualou ou superou essas abordagens na reprodução de dados experimentais, ao mesmo tempo que exigia muito menos recurso computacional do que simulações em escala total. Também funcionou além das IDPs simples, lidando com proteínas com vários domínios rígidos ligados por conectores flexíveis e recuperando suas formas globais em solução. Quando os pesquisadores refinaram ainda mais os ensembles do bAIes com dados experimentais, o acordo melhorou ainda mais, mostrando que o método pode servir como um ponto de partida poderoso para modelagem integrativa.
O que isso significa para a biologia e a medicina
Ao casar o poder de reconhecimento de padrões do AlphaFold com um modelo físico cuidadosamente projetado e um tratamento bayesiano da incerteza, o bAIes oferece uma rota prática para “filmes” detalhados de proteínas desordenadas em vez de instantâneos únicos. Esses ensembles detalhados em nível atômico podem ajudar cientistas a entender como regiões flexíveis reconhecem parceiros, como o mau enovelamento e a agregação começam em doenças como Parkinson e Alzheimer, e como pequenas moléculas podem se ligar a alvos elusivos e mutáveis. Como o método é eficiente e disponível em software de código aberto, ele pode ser amplamente adotado para gerar ensembles realistas para muitas proteínas desordenadas, orientando experimentos e apoiando futuros sistemas de IA que visem prever não apenas uma estrutura, mas toda a gama de formas que as moléculas mais flexíveis da vida podem adotar.
Citação: Schnapka, V., Morozova, T.I., Sen, S. et al. Atomic resolution ensembles of intrinsically disordered proteins with Alphafold. Nat Commun 17, 2399 (2026). https://doi.org/10.1038/s41467-026-69172-y
Palavras-chave: proteínas intrinsecamente desordenadas, AlphaFold, modelagem bayesiana, conjuntos de proteínas, biologia estrutural