Clear Sky Science · pt
Impacto das forças do solvente e da simetria quebrada na montagem de proteínas projetadas em uma interface líquido-sólido
Por que esse minúsculo mundo sobre uma superfície importa
De células solares a sensores médicos, muitas tecnologias futuras dependerão da construção de estruturas precisas onde moléculas biológicas encontram materiais sólidos. Este estudo examina como “bastões” proteicos projetados se organizam sobre superfícies minerais em água salgada. A lição surpreendente é que a água imediatamente junto à superfície, e assimetrias sutis no cristal abaixo dela, podem mudar completamente como essas proteínas se alinham — às vezes produzindo padrões que a teoria clássica diz que não deveriam existir.
Projetando proteínas para se encaixar em um cristal
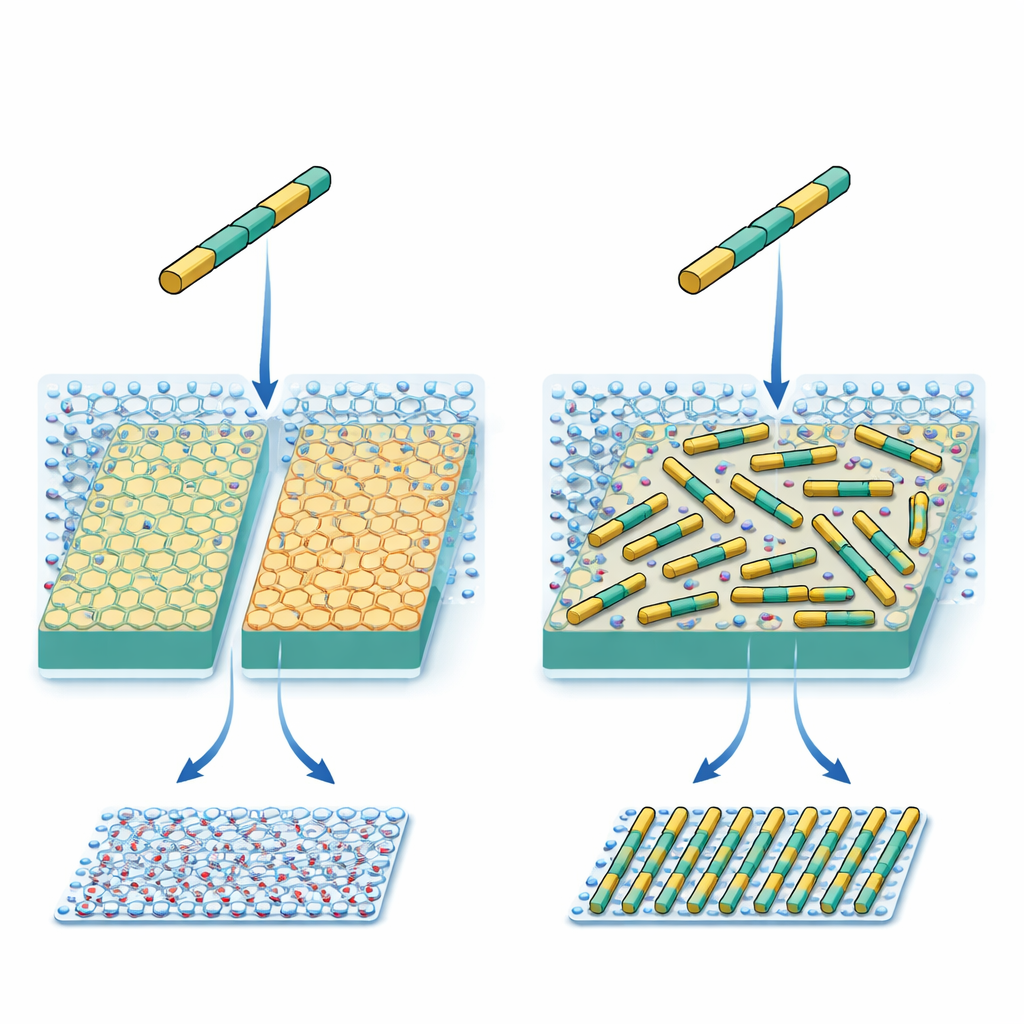
Os pesquisadores trabalham com uma proteína sintética em forma de bastão curto e rígido. Sua química de superfície e o espaçamento de grupos carregados foram cuidadosamente desenhados para coincidir com o padrão de íons potássio em um mineral comum chamado mica. Em princípio, isso deveria fazer com que cada bastão proteico preferisse três direções equivalentes na superfície cristalina, como o alinhamento ao longo de três raios de uma roda. Trabalhos anteriores mostraram que, mesmo com esse projeto cuidadoso, as proteínas formaram múltiplos padrões inesperados em vez de apenas o que os engenheiros tinham em mente. Essa inconsistência sugeriu que alguma força importante estava faltando nas regras de projeto atuais.
Duas superfícies quase idênticas, dois resultados muito diferentes
Para acompanhar o que acontecia, a equipe usou microscopia de força atômica em alta velocidade, que pode observar bastões proteicos individuais se moverem e se montarem sobre uma superfície em tempo real. Eles compararam duas formas de mica estreitamente relacionadas. Ambas expõem a mesma rede de potássio, mas suas estruturas atômicas internas diferem ligeiramente, o que por sua vez altera como a água se organiza em camadas logo acima da superfície. Em níveis moderados de sal, os bastões formaram um tapete denso porém localmente desordenado em ambas as superfícies, com apenas pequenos trechos alinhados. Quando a concentração de sal foi elevada muito, no entanto, o comportamento se dividiu: em um tipo de mica, os bastões permaneceram desordenados ao longo das três direções, enquanto no outro eles espontaneamente formaram longas filas paralelas e espaçadas uniformemente por toda a superfície.
Camadas de água e simetria quebrada
Modelagem computacional dos minerais e da água circundante ajudou a explicar essa personalidade dupla. Na forma mais simétrica da mica, a primeira e a segunda camadas de moléculas de água preservam um padrão regular hexagonal. Na forma menos simétrica, átomos internos e grupos enterrados dentro do cristal quebram essa simetria trifurcada, e esse padrão quebrado é transmitido para as camadas de água próximas, que desenvolvem regiões em faixas. As proteínas não tocam apenas o cristal nu; elas interagem também com essa água estruturada. Como resultado, uma orientação dos bastões torna-se ligeiramente mais favorável que as outras duas, mesmo que a combinação proteína–cristal projetada sugerisse que as três deveriam ser iguais.
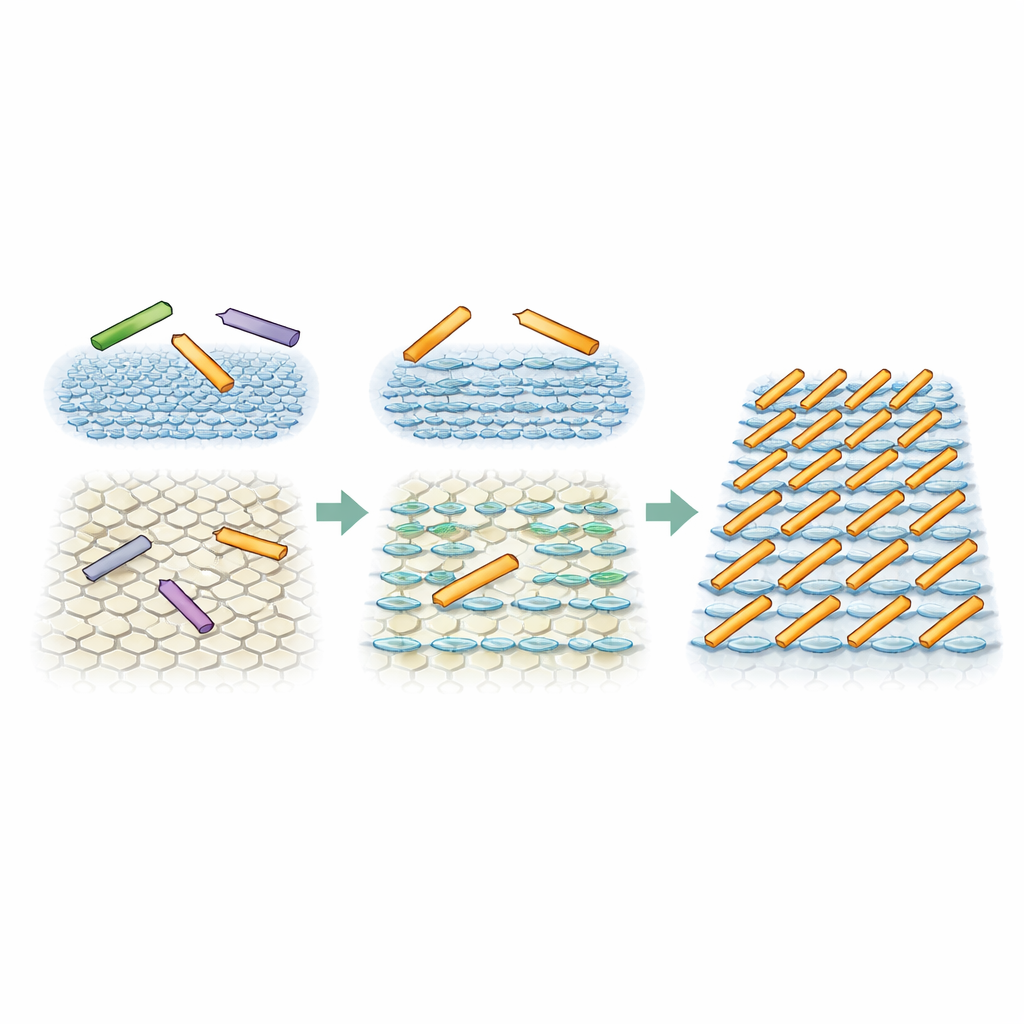
Simulações revelam uma fase inesperada
Para testar se um viés direcional sutil do ambiente da superfície poderia realmente explicar os padrões observados, os pesquisadores executaram simulações Monte Carlo de retângulos rígidos simples representando os bastões proteicos. Em um conjunto de simulações, as três orientações tinham igual probabilidade, imitando a superfície totalmente simétrica. Nesse caso, os bastões permaneceram em um estado de alta densidade porém desordenado, com alinhamentos apenas temporários ou limitados, exatamente como visto em um tipo de mica. Em um segundo conjunto, uma direção foi tornada apenas modestamente mais favorável — cerca de duas vezes mais provável que as outras duas — representando a influência das camadas de água em faixas. Nessas condições, e quando os bastões podiam se mover o suficiente, o sistema evoluiu naturalmente para um estado com filas paralelas e espaçadas uniformemente. Esta é a chamada fase smética, que a teoria de longa data diz que não deveria aparecer para bastões não interagentes em duas dimensões, ainda assim o pequeno empurrão direcional da interface a tornou estável.
Repensando como projetamos materiais bioinspirados
Em poucas palavras, este trabalho mostra que a química proteína–superfície finamente ajustada não é suficiente para prever como proteínas projetadas se organizarão em materiais reais. A água entre a proteína e o sólido, e a maneira como o cristal quebra sutilmente a simetria, podem direcionar o autoensamblamento para padrões que os modelos de livro-texto nunca antecipariam. Ao combinar microscopia em alta velocidade, aprendizado de máquina para quantificar ordem e simulações baseadas em física, o estudo delineia um caminho para incorporar esses efeitos ocultos do solvente e da simetria em futuras ferramentas de projeto de proteínas. Para quem pretende projetar materiais híbridos bio–inorgânicos confiáveis, a mensagem é clara: é preciso projetar não apenas para a proteína e a superfície, mas também para a camada estruturada de água que os conecta.
Citação: Yadav Schmid, S., Helfrecht, B., Stegmann, A. et al. Impact of solvent forces and broken symmetry on the assembly of designed proteins at a liquid-solid interface. Nat Commun 17, 2446 (2026). https://doi.org/10.1038/s41467-026-69170-0
Palavras-chave: autoensamblagem de proteínas, interfaces líquido-sólido, estrutura da água interfacial, ordenamento smético, materiais bioinspirados