Clear Sky Science · pt
Uma abordagem integrativa em biologia estrutural revela a organização dinâmica do complexo chaperona quaternário R2SP
Como as Células Constroem Máquinas Moleculares Complexas
Dentro de cada célula, muitas proteínas não funcionam sozinhas — elas precisam se encaixar em máquinas elaboradas antes de poderem desempenhar suas funções. Acertar essa etapa de montagem é vital para respiração saudável, movimento e até fertilidade. Este artigo explora um desses ajudantes de montagem, uma “equipe de construção” molecular chamada complexo R2SP, e mostra como ele é organizado e como funciona. Entender o R2SP importa porque, quando seus componentes falham, estruturas minúsculas semelhantes a pelos nas células, chamadas cílios, não se movem corretamente, causando problemas respiratórios crônicos e outras doenças.
As Equipes de Construção Celular R2TP e R2SP
As células dependem de equipes de proteínas auxiliares, conhecidas como complexos chaperona, para guiar outras proteínas até as formas multipartes corretas. Uma equipe estudada há muito, chamada R2TP, é encontrada em muitos tecidos e ajuda a montar grandes máquinas, como as fábricas de RNA e os sensores de dano no DNA. R2SP é um primo próximo do R2TP: ambos são construídos em torno do mesmo motor em forma de anel, composto por duas proteínas parceiras, RUVBL1 e RUVBL2, que consumem a molécula de energia ATP. O que difere são os adaptadores acessórios que conectam os clientes a esse motor. R2TP usa adaptadores chamados RPAP3 e PIH1D1, enquanto R2SP usa SPAG1 e PIH1D2. Essas pequenas diferenças nas peças conferem às duas máquinas listas de clientes diferentes e conectam o R2SP, em particular, à construção dos cílios móveis que varrem muco e fluidos sobre os tecidos.
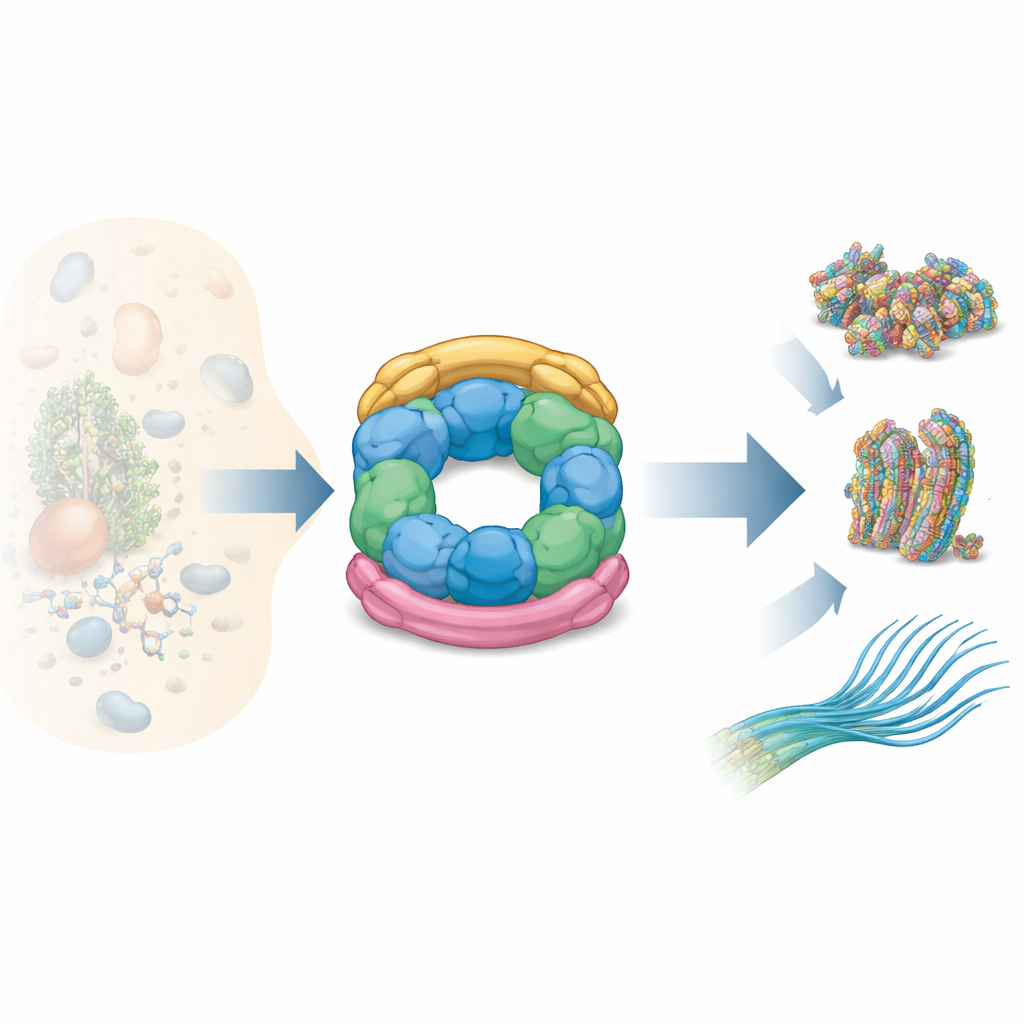
Como as Peças do R2SP se Encaixam
Os autores combinaram várias técnicas estruturais — ressonância magnética nuclear, criomicroscopia eletrônica e espectrometria de massa com cross‑linking — com testes bioquímicos para mapear como o R2SP é montado. Eles mostraram que a porção final (cauda) do SPAG1 agarra o anel RUVBL1/RUVBL2 de uma forma que se assemelha à ligação do RPAP3 no R2TP, mas com ajustes chave na forma e nos pontos de contato. Um segundo adaptador, PIH1D2, encaixa‑se sob o anel e também alcança para tocar domínios laterais flexíveis do motor. Esses domínios laterais atuam como braços com dobradiça que ajudam a transmitir movimentos do núcleo consumidor de ATP para os clientes ligados. Os dados revelam que SPAG1 e PIH1D2 não se prendem de forma independente: eles cooperam, formando uma unidade acoplada que prende o anel por cima e por baixo, estabilizando uma arquitetura tridimensional distintiva.
Um Anel Dinâmico que Muda de Marcha
Além de imagens estáticas, a equipe investigou como o R2SP se comporta. Usando medidas de interação, descobriram que o motor RUVBL1/RUVBL2 pode existir tanto como um anel único quanto como um anel duplo empilhado. Quando SPAG1 e PIH1D2 se ligam, eles deslocam fortemente esse equilíbrio em favor da forma de anel único e podem decorá‑la com até três pares de adaptadores. Ao mesmo tempo, os adaptadores aumentam marcadamente a atividade de consumo de ATP do motor e alteram a velocidade com que moléculas semelhantes ao ATP se ligam e se desligam dos sítios ativos. Comparado ao sistema R2TP, SPAG1 e PIH1D2 favorecem etapas diferentes na liberação de nucleotídeos, sugerindo que R2SP ajusta o ciclo energético do motor central à sua maneira. Esse uso de energia finamente controlado acredita‑se impulsionar a montagem em etapas dos complexos clientes necessários para os cílios móveis.
Uma Plataforma Flexível para Construir Componentes de Cílios
Ao integrar todas as restrições estruturais em um único modelo, os autores propõem que o R2SP atua como uma plataforma flexível de muitos braços. A cauda de SPAG1 ancora‑se firmemente no topo do anel, enquanto suas outras regiões e os dois domínios de PIH1D2 se estendem em direção ao lado mais aberto, em forma de braço, do motor. É nesse lado que proteínas clientes e chaperonas auxiliares, como HSP70 e HSP90, provavelmente se acoplam. Como até três unidades SPAG1–PIH1D2 podem se anexar a um anel e os braços flexíveis movem‑se constantemente, todo o complexo assemelha‑se a um polvo cujos tentáculos podem agarrar várias peças clientes ao mesmo tempo, coordená‑las e passá‑las para serem montadas em estruturas ciliares maiores.
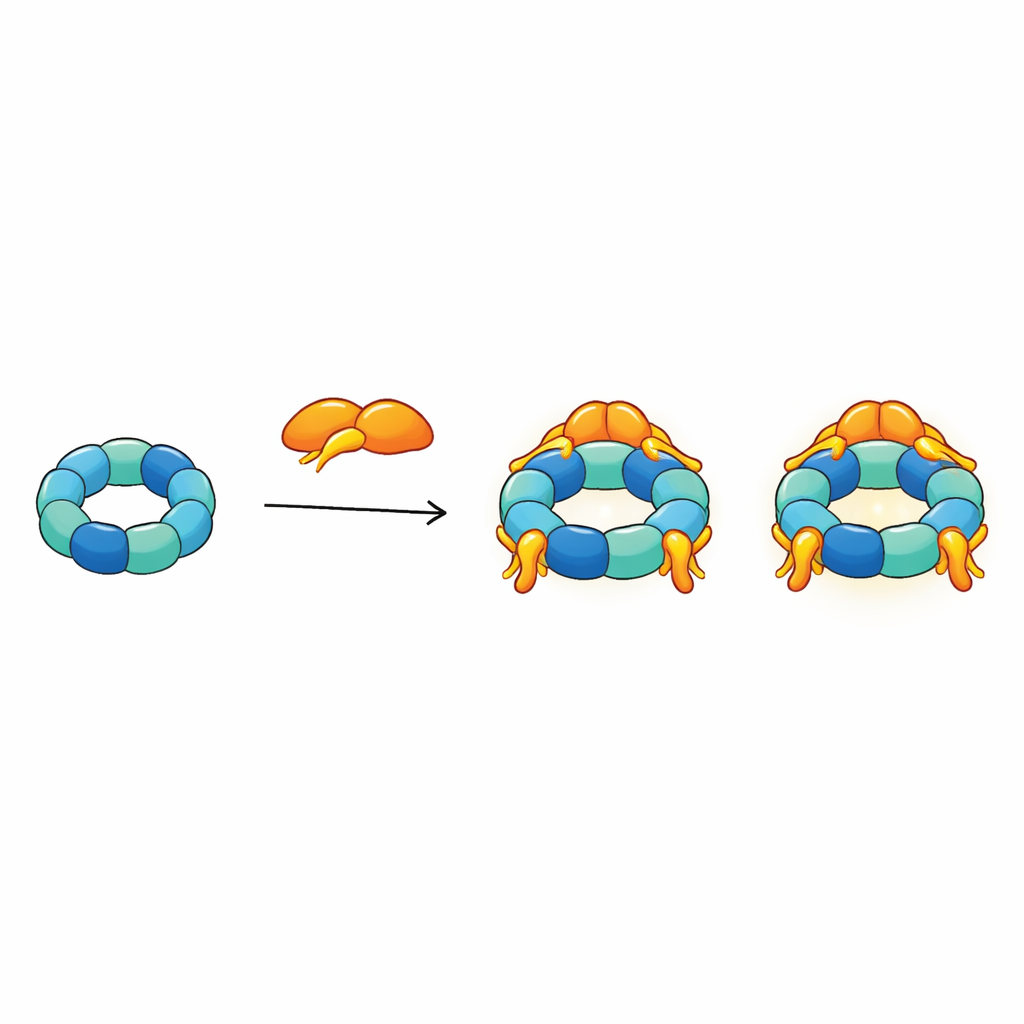
O Que Isso Significa para Saúde e Doença
Para não especialistas, a mensagem principal é que R2SP é uma versão especializada de uma máquina geral de construção celular, reconfigurada pela troca de apenas dois adaptadores. Essa troca altera tanto o controle do motor central quanto o posicionamento dos clientes, explicando por que R2SP se concentra em construir partes para cílios móveis enquanto R2TP serve outras fábricas celulares. Defeitos em SPAG1 já são conhecidos por causar discinesia ciliar primária, um distúrbio marcado por infecções crônicas e problemas de fertilidade. Ao revelar o layout detalhado e os princípios de funcionamento do R2SP, este estudo lança as bases para entender como mutações específicas perturbam a montagem de cílios e pode, eventualmente, orientar tratamentos direcionados que restaurem ou modulam essa equipe molecular de construção crucial.
Citação: Santo, P.E., Chagot, ME., Gizardin-Fredon, H. et al. An integrative structural biology approach reveals the dynamic organization of the R2SP quaternary chaperone complex. Nat Commun 17, 2605 (2026). https://doi.org/10.1038/s41467-026-69157-x
Palavras-chave: chaperonas moleculares, montagem de complexos proteicos, cílios móveis, biologia estrutural, RUVBL1 RUVBL2