Clear Sky Science · pt
Mecanismo molecular de importação de fosfato pelo transportador bacteriano PstSCAB
Por que nutrientes minúsculos importam para nós
Cada célula viva, de neurônios humanos a bactérias do solo, depende do fósforo. Esse elemento ajuda a armazenar energia, construir o DNA e manter a integridade das membranas celulares. No ambiente, porém, o fosfato utilizável — a forma de fósforo que as células conseguem realmente importar — costuma ser escasso. Muitas bactérias patogênicas dependem de uma máquina molecular ultraeficiente, chamada transportador PstSCAB, para capturar fosfato quando ele está em falta. Entender exatamente como essa máquina funciona não é apenas uma questão de ciência básica; pode abrir caminhos para novas formas de desarmar infecções, privando as bactérias desse nutriente vital.
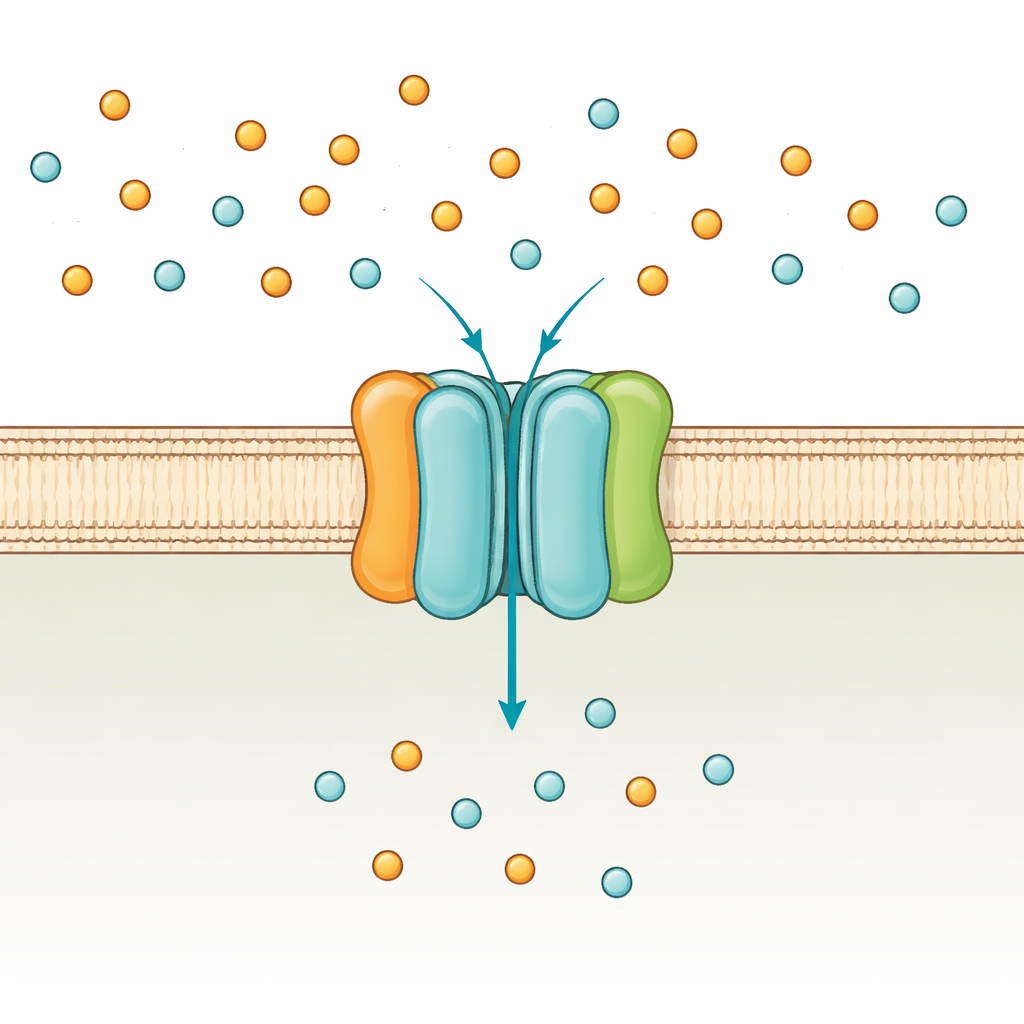
O porteiro do fosfato da célula
Bactérias como Escherichia coli usam duas vias principais para captar fosfato: um sistema de baixa afinidade que funciona quando o fosfato é abundante, e o sistema de alta afinidade PstSCAB, que é ativado em condições de escassez. O PstSCAB está inserido na membrana celular e é movido por ATP, a moeda energética universal da célula. É composto por cinco partes: duas subunidades embebidas na membrana (PstA e PstC) que formam o canal, uma proteína solúvel “captadora” fora da membrana (PstS) que agarra o fosfato, e um par de subunidades internas (PstB) que hidrolisam ATP para impulsionar o transporte. Como esse sistema também ajuda a controlar muitos genes ligados à virulência bacteriana, mutações em PstSCAB podem enfraquecer patógenos que causam infecções do trato urinário, sepse em animais de criação e tuberculose.
Capturando a máquina em ação
Até agora, os cientistas tinham apenas visões parciais do PstSCAB, principalmente da proteína captadora PstS isoladamente. Neste estudo, os pesquisadores usaram criomicroscopia eletrônica de alta resolução para visualizar o transportador inteiro em vários passos-chave de seu ciclo de trabalho. Eles reconstituíram as proteínas bacterianas em “nanodiscos” de membrana artificiais e os congelaram tão rapidamente que as moléculas ficaram presas em movimento. Ajustando cuidadosamente as proteínas e adicionando ou retirando ATP, obtiveram estruturas de três estados principais: uma forma de repouso voltada para o interior sem a captadora acoplada, um estado pré-translocação onde a PstS carregada de fosfato se acopla ao complexo de membrana, e um intermediário catalítico ligado a ATP em que o fosfato está retido dentro do transportador.
Como mudanças de forma movem o fosfato
As imagens revelam como mudanças de forma coordenadas transferem o fosfato do exterior para o interior da célula. No estado de repouso, o canal formado por PstA e PstC abre apenas para o interior celular; o lado externo está selado por um conjunto de resíduos que fazem as vezes de “portão”, o que impede que o fosfato entre do meio externo. Quando a PstS carregada de fosfato se acopla no estado pré-translocação, ela se encaixa entre alças flexíveis de PstA e PstC, mas, de forma notável, as subunidades de membrana mal mudam de forma. A verdadeira mudança ocorre quando a PstS começa a abrir suas duas lobos para liberar o fosfato e, em conjunto, as duas subunidades PstB se aproximam para ligar o ATP. Essa ligação ao ATP prende PstB como um dímero e puxa hélices conectantes em PstA e PstC, invertendo todo o poro para uma conformação voltada para fora que expõe um bolso específico de ligação ao fosfato para o lado externo.
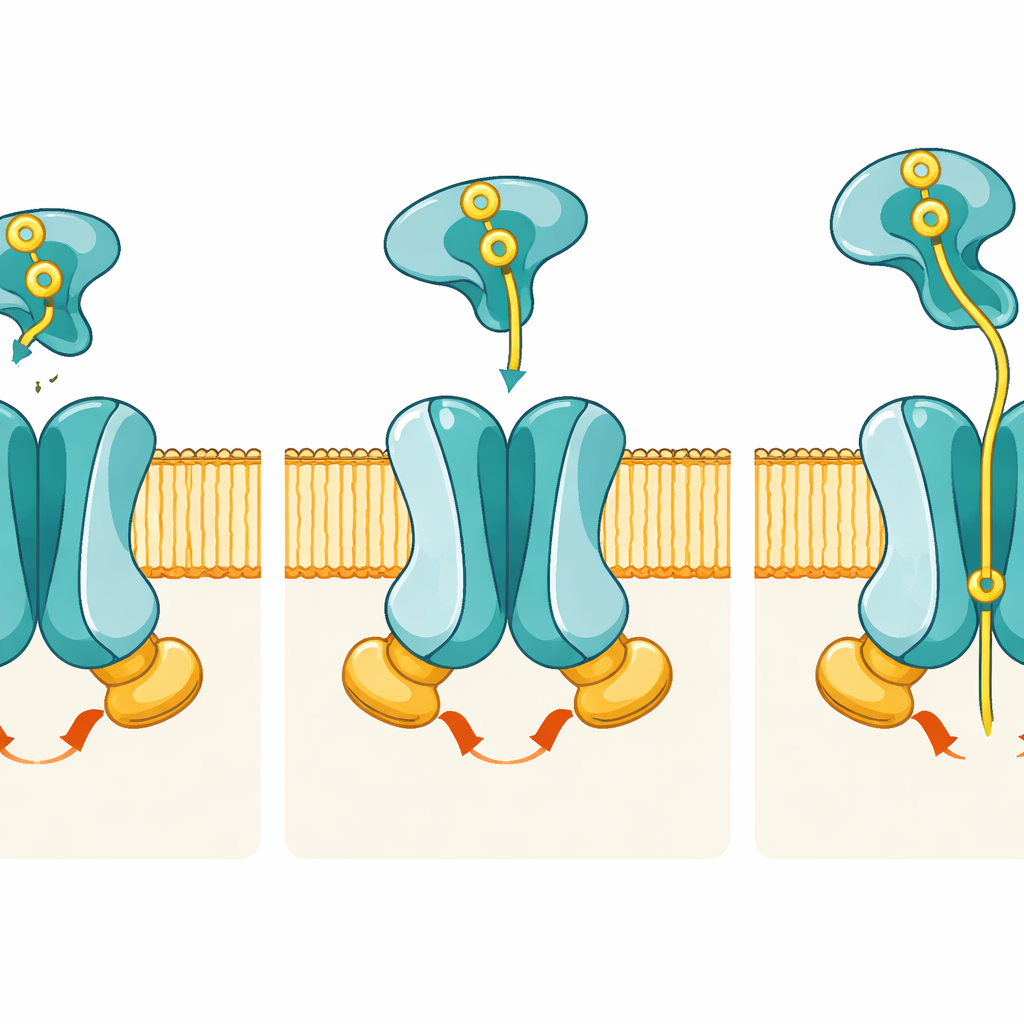
Um bolso sob medida para o fosfato
Na estrutura voltada para fora, ligada ao ATP, os autores encontram uma densidade no meio da região de membrana que corresponde a um íon fosfato. Esse íon é apoiado por aminoácidos carregados positivamente — particularmente duas argininas, uma de PstA e outra de PstC — que funcionam como pontas moleculares agarrando o fosfato, que é carregado negativamente. Simulações computacionais mostram que o fosfato permanece firmemente ligado nesse bolso ao longo de microssegundos, e experimentos genéticos confirmam sua importância: quando esses resíduos-chave são mutados, o transportador ainda hidrolisa ATP, mas importa fosfato muito mal. Essa separação entre “onde a energia é gasta” e “onde a carga é reconhecida” destaca quão precisamente ajustada a máquina é para o fosfato.
De instantâneos estruturais à promessa médica
Juntas, as estruturas e os testes bioquímicos de suporte delineiam um ciclo completo: a PstS captura o fosfato no exterior, acopla-se ao transportador voltado para dentro e então — acoplado à ligação e à quebra de ATP por PstB — desencadeia uma inversão que passa o fosfato para o bolso na membrana e, finalmente, para o interior da célula. Depois que o ATP é hidrolisado, a máquina relaxa de volta ao estado de repouso, pronta para outra rodada. Para um leitor leigo, a mensagem principal é que agora temos um roteiro em nível atômico de como muitas bactérias sobrevivem em ambientes pobres em fosfato e regulam sua virulência. Esse mapa detalhado pode orientar o design de fármacos, anticorpos ou peptídeos que emperrem o transportador ou bloqueiem sua proteína captadora, potencialmente transformando um portão essencial de nutrientes em um alvo terapêutico vulnerável.
Citação: Xiao, H., Li, S., Qi, R. et al. Molecular mechanism of phosphate import by the bacterial PstSCAB transporter. Nat Commun 17, 2294 (2026). https://doi.org/10.1038/s41467-026-69153-1
Palavras-chave: transporte de fosfato, captação de nutrientes bacteriana, transportador ABC, PstSCAB, alvos antibacterianos