Clear Sky Science · pt
Alquenilação e alcinilação seletivas em estágio avançado do N-Me de medicamentos e aminas terciárias não ativadas usando catálise fotoredox
Por que modificar medicamentos antigos ainda importa
Muitos medicamentos atuais funcionam bem, mas ainda podem ser aprimorados em termos de segurança, efeitos colaterais ou precisão ao atingir seus alvos no organismo. Químicos têm se interessado cada vez mais em “ajustar” suavemente fármacos já existentes em fases avançadas do desenvolvimento, em vez de inventar moléculas completamente novas do zero. Este estudo mostra como feixes de luz visível podem ser usados para acoplar novas peças a um tipo comum de bloco de construção farmacêutico, criando candidatos antidepressivos aprimorados e abrindo um caminho mais rápido para tratamentos refinados.
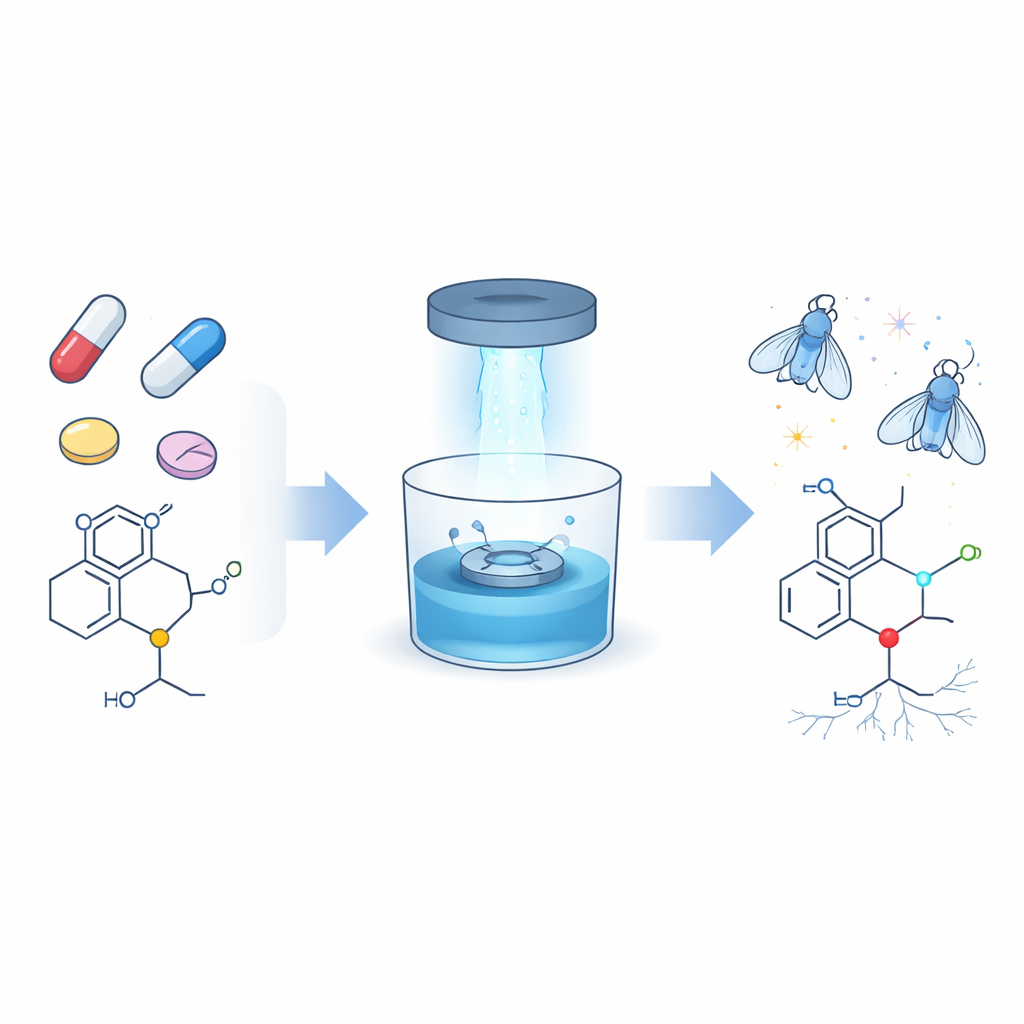
Melhorando uma característica comum em muitos medicamentos
Uma parcela surpreendentemente grande dos medicamentos modernos — mais de dois em cada cinco — contém fragmentos ricos em nitrogênio chamados aminas, e a maioria destes é de um subtipo conhecido como aminas terciárias. Elas aparecem em antibióticos, medicamentos contra o câncer, antialérgicos, analgésicos e antidepressivos. Até agora, os químicos enfrentavam dificuldade para modificar seletivamente apenas uma pequena parte desses grupos, a unidade N-metil, quando ela está cercada por várias ligações carbono–hidrogênio quase idênticas. Os autores buscaram desenvolver uma forma suave e confiável de anexar novos “pontos de pega”, especificamente ligações carbono–carbono duplas (alquenos) e triplas (alquinos), nessa posição N-metil sem perturbar o restante da molécula do medicamento.
Usando luz para reconfigurar uma ligação por vez
A equipe recorreu à catálise fotoredox, uma tecnologia que usa luz visível e um catalisador fotoativo para movimentar elétrons isolados e desencadear reações sob condições brandas. Em seu sistema, luz azul excita um catalisador orgânico, que temporariamente retira um elétron da amina terciária. Essa etapa gera um radical de curta vida na posição N-metil que pode se unir a moléculas parceiras cuidadosamente escolhidas contendo grupos vinil ou alcinil. Ao ajustar as condições da reação — escolha de solvente, base e aditivos — os pesquisadores alcançaram altos rendimentos e excelente controle, de modo que o novo grupo se fixa quase exclusivamente na posição N-metil, mesmo quando vários sítios semelhantes estão presentes. Eles demonstraram isso em um amplo painel de aminas simples e depois em medicamentos reais, incluindo anti-histamínicos, remédios cardíacos, anti-infecciosos e vários antidepressivos.
Do ajuste químico a uma ação antidepressiva melhor
Para avaliar se essas alterações estruturais poderiam ter relevância médica, os autores focaram no imipramina, um antidepressivo tricíclico usado há muito tempo. Projetaram e modelaram mais de vinte variantes do imipramina nas quais a nova extensão vinil ou alcinil carregava anéis aromáticos que poderiam se encaixar em um bolso hidrofóbico do transportador de serotonina humano, uma proteína que controla os níveis do mensageiro relacionado ao humor, a serotonina. Acoplamentos computacionais sugeriram que muitas dessas moléculas modificadas deveriam se ligar tão bem quanto, ou melhor que, o fármaco parental. Os candidatos mais promissores foram então sintetizados usando o novo método acionado por luz e testados em sistemas vivos: um modelo de depressão em moscas-das-frutas baseado em isolamento social e, para os dois melhores compostos, em células nervosas de camundongo que transportam serotonina ativamente.
Como moscas e células revelaram fármacos mais eficazes
Em moscas-das-frutas machos isoladas, comportamento semelhante à depressão se manifesta como aumento da agressividade. Administrar imipramina reduz essa agressividade, refletindo sua ação antidepressiva em humanos. Notavelmente, várias das derivadas de imipramina produzidas pelo novo método reduziram a agressividade tão bem quanto, e quatro candidatos mostraram-se ainda melhores que a própria imipramina. Em células hipocampais de camundongo em cultura, dois compostos líderes bloquearam a recaptação de serotonina mais fortemente que a imipramina, conforme confirmado tanto por medição química direta da serotonina quanto por um corante fluorescente que acende quando é absorvido pelas células. Esses testes indicam que mudanças sutis em estágio avançado na posição N-metil podem de fato aumentar a potência antidepressiva, em vez de apenas alterar a molécula no papel.
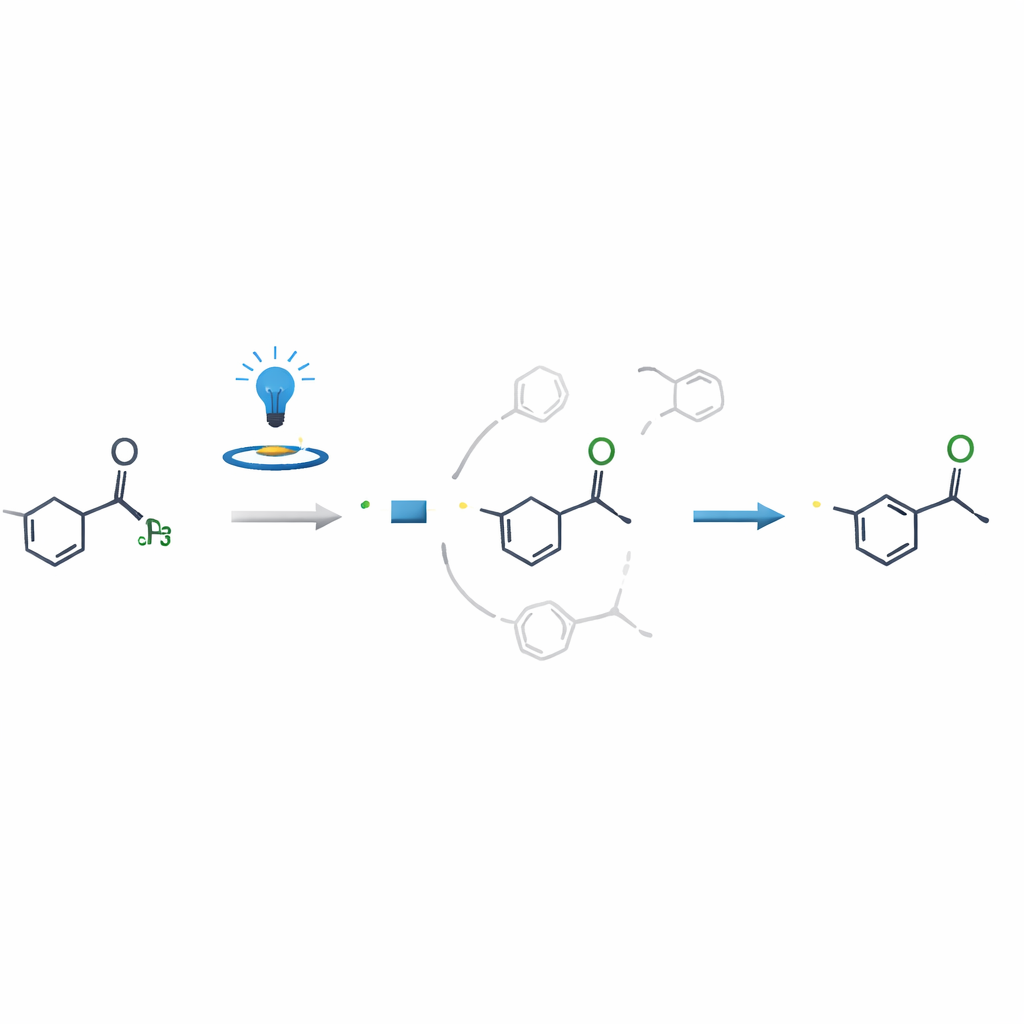
Por que a reação é tão seletiva
Uma questão científica central foi por que a reação modifica o grupo N-metil de forma tão limpa quando outras posições próximas parecem igualmente reativas. Por meio de experimentos de controle, medições de spin eletrônico e cálculos computacionais detalhados, os autores mostraram que o ponto decisório crucial não é quando o radical é formado pela primeira vez, mas quando esse radical adiciona-se ao parceiro vinil ou alcinil. A via que leva do radical N-metil ao produto final é energeticamente mais favorável e muito mais rápida do que rotas concorrentes, direcionando efetivamente a reação para um único resultado. Essa percepção ajuda a explicar a alta seletividade e pode orientar estratégias semelhantes em outras moléculas complexas.
O que este trabalho significa para medicamentos futuros
No geral, o estudo introduz uma maneira prática de atualizar cirurgicamente medicamentos existentes que contêm aminas terciárias, adicionando pontos químicos compactos que podem ajustar como eles interagem com alvos biológicos ou se ligam a outros componentes. Ao mostrar que modificações em estágio avançado podem transformar um antidepressivo consagrado em variantes ainda mais eficazes em modelos simples de animais e células, o trabalho aponta para uma combinação poderosa de química sintética moderna, computação e biologia. À medida que a abordagem for estendida a outros medicamentos, ela pode acelerar o refinamento de candidatos farmacêuticos e ajudar a renovar terapias antigas com desempenho e segurança aprimorados.
Citação: Paul, S., Mahato, S., Mahapatra, S.K. et al. Late-stage N-Me selective alkenylation and alkynylation of drugs and unactivated tertiary amines using photoredox catalysis. Nat Commun 17, 2695 (2026). https://doi.org/10.1038/s41467-026-69131-7
Palavras-chave: catálise fotoredox, funcionalização em estágio avançado, aminas terciárias, desenvolvimento de medicamentos antidepressivos, transportador de serotonina