Clear Sky Science · pt
Terapia bacteriana projetada suprime Escherichia coli enterohemorrágica por competição metabólica e silenciamento de virulência
Bactérias amistosas como remédio vivo
Intoxicação alimentar causada por certas linhagens de Escherichia coli pode fazer muito mais do que provocar um mal‑estar estomacal. Algumas dessas chamadas E. coli enterohemorrágicas (EHEC) liberam toxinas potentes que podem desencadear insuficiência renal, especialmente em crianças, e antibióticos convencionais podem, na verdade, agravar o quadro. Este estudo explora um tipo diferente de tratamento: usar um probiótico projetado e um açúcar encontrado no leite materno humano, embalados em microcápsulas inteligentes, para competir com bactérias perigosas e silenciar seu comportamento nocivo sem perturbar o restante do ecossistema intestinal.
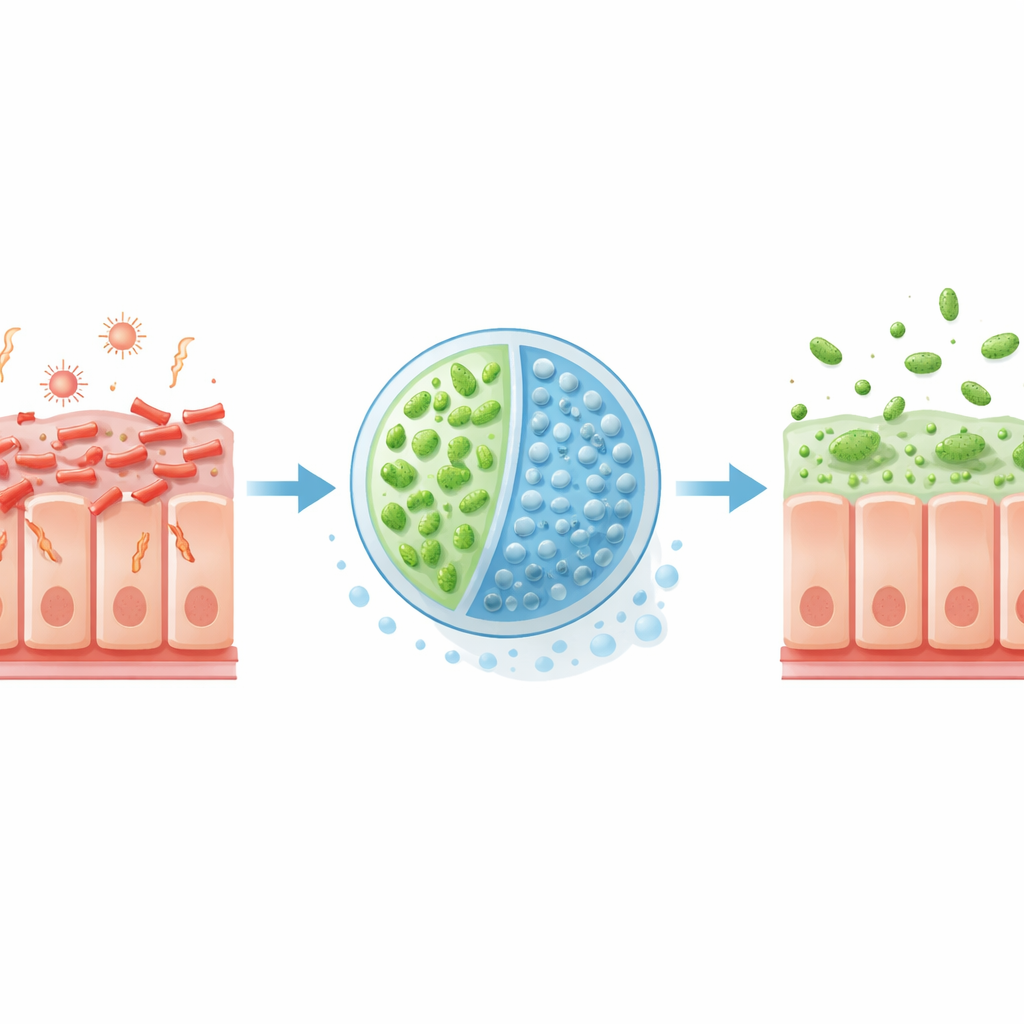
Por que algumas E. coli são tão perigosas
A EHEC é um germe transmitido por alimentos, frequentemente adquirido por carne malcozida ou produtos contaminados. Uma vez no intestino, ela se prende firmemente às células intestinais e injeta proteínas que remodelam a superfície celular, esculpindo pontos de apoio que ajudam a bactéria a aderir e se espalhar. Ao mesmo tempo, a EHEC produz toxinas de Shiga, que podem entrar na corrente sanguínea e danificar vasos sanguíneos, às vezes levando a uma condição com risco de vida chamada síndrome hemolítico‑urêmica. Como muitos antibióticos estressam essas bactérias e desencadeiam ainda mais liberação de toxinas, os médicos têm poucas opções seguras além do suporte clínico, tornando abordagens novas e direcionadas altamente desejáveis.
Reprogramando um probiótico para privar e desarmar a EHEC
Os pesquisadores recorreram à Escherichia coli Nissle 1917, uma linhagem probiótica usada há muito tempo, e a reprogramaram em um microrganismo terapêutico chamado EcN3. Eles equiparam o EcN3 com genes extras que lhe permitem degradar com mais eficiência um ácido açúcar, o ácido glucurônico, que a EHEC prefere como fonte de alimento no intestino grosso. Também deram ao EcN3 uma enzima que divide o açúcar do leite materno 2′‑fucosilactose em duas partes: lactose e fucose. A lactose atua como um "interruptor" interno que liga o sistema aprimorado de utilização de nutrientes no EcN3, ajudando‑o a absorver o ácido glucurônico e privar a EHEC desse combustível. A fucose, por sua vez, serve como um sinal que diz à EHEC para reduzir genes de virulência chave, diminuindo sua capacidade de formar aderências fortes e causar danos.
Cápsulas inteligentes que liberam a terapia no lugar certo
Simplesmente administrar bactérias projetadas e açúcar ao intestino não é suficiente: o ácido estomacal pode matar o probiótico, e outros microrganismos podem consumir o açúcar antes que ele alcance o cólon. Para resolver isso, a equipe construiu microesferas multicompartmentadas—pequenas bolinhas feitas de gel de alginato com duas câmaras internas separadas. Uma câmara carrega o EcN3, e a outra carrega 2′‑fucosilactose, mantendo‑os separados até que as esferas alcancem o intestino grosso. Essas microcápsulas resistem à degradação em fluido simulado do estômago, mas se dissolvem em condições semelhantes às do cólon, liberando tanto as bactérias projetadas quanto o açúcar exatamente onde são necessários. Em camundongos, o sistema encapsulado levou a maior sobrevivência do EcN3 e a ativação mais forte de seus genes projetados do que a administração dos mesmos componentes sem cápsulas.
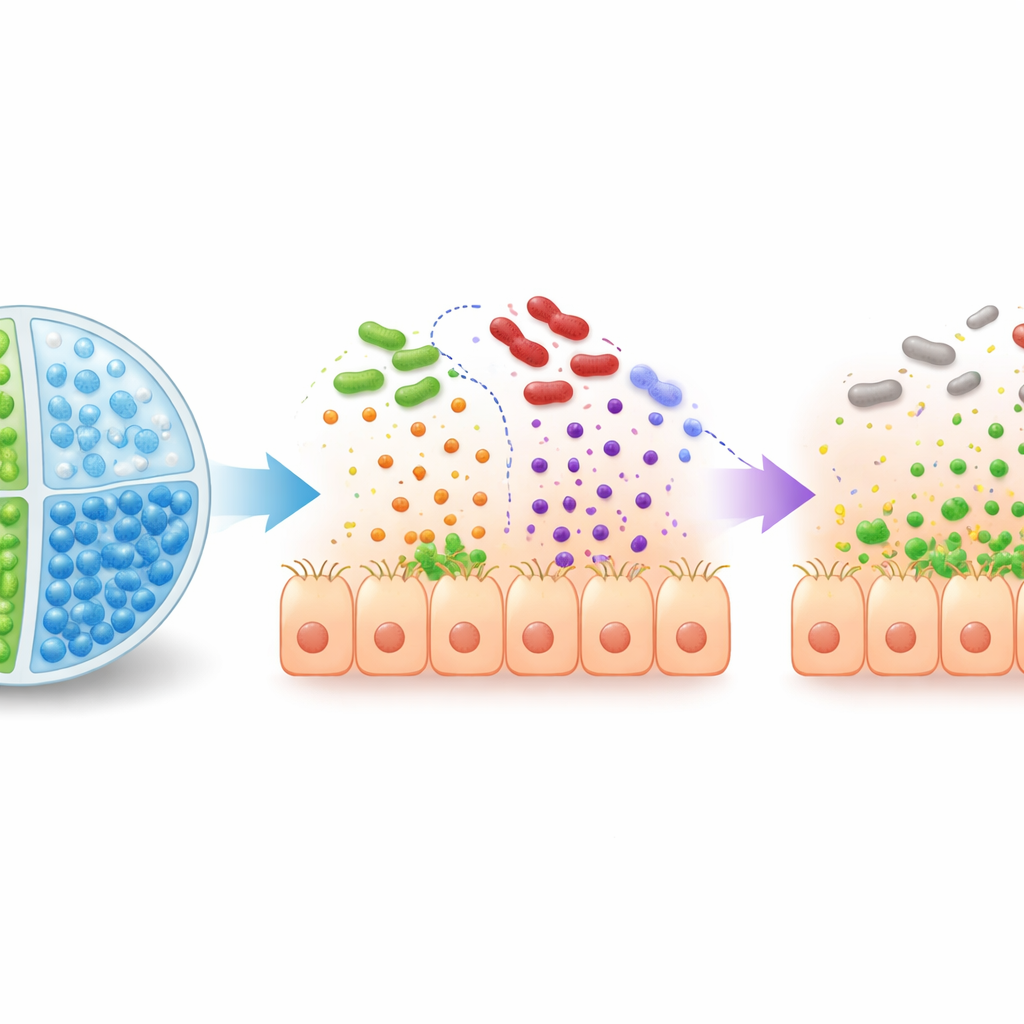
Testando a proteção em modelos animais
A equipe testou a estratégia em coelhos lactentes infectados com EHEC e em camundongos infectados com Citrobacter rodentium, um patógeno intimamente relacionado que imita muitos aspectos da doença humana. Quando tratados após a infecção com EcN3 mais 2′‑fucosilactose, os animais apresentaram menos patógenos no intestino, menor expressão dos genes de adesão das bactérias e menos dano ao tecido intestinal—tudo isso sem aumentar a produção de toxina de Shiga. Como medida preventiva, a combinação livre (não encapsulada) funcionou mal porque o açúcar foi rapidamente consumido pela microbiota existente. Em contraste, quando EcN3 e 2′‑fucosilactose foram entregues juntos em microesferas de câmara dupla, tanto coelhos quanto camundongos tiveram colonização patogênica drasticamente reduzida, doença mais branda e melhor sobrevivência.
Ajuda para os bons micróbios e recuperação da barreira intestinal
Usando sequenciamento de DNA para perfilar as bactérias intestinais, os cientistas descobriram que a infecção perturbou o equilíbrio microbiano normal, aumentando Citrobacter nocivo enquanto enfraquecia grupos benéficos. O tratamento com as microcápsulas projetadas não só reduziu os níveis do patógeno como também restaurou a comunidade para um estado mais saudável, especialmente aumentando espécies de Lactobacillus conhecidas por apoiar a saúde intestinal. Medidas da função da barreira intestinal contaram uma história semelhante: animais que receberam a terapia encapsulada apresentaram níveis maiores de genes relacionados ao muco e às junções apertadas, camadas de muco protetoras mais espessas e menor vazamento de traçador fluorescente do intestino para a corrente sanguínea, indicando paredes intestinais mais firmes e menos inflamadas.
Um vislumbre do futuro do cuidado de infecções sem antibióticos
No geral, este trabalho demonstra uma estratégia direcionada e de duplo ataque contra uma infecção transmitida por alimentos notoriamente difícil de tratar. Ao combinar um probiótico projetado que compete por alimento e percebe um sinal de açúcar benigno com microcápsulas que entregam ambos os componentes ao cólon, a terapia enfraquece a EHEC, reduz seus números e protege o intestino sem depender de antibióticos tradicionais. Embora sejam necessários mais estudos de segurança e ensaios clínicos, a abordagem ilustra como medicamentos vivos e materiais inteligentes poderão, um dia, fornecer maneiras precisas e amigas do microbioma para manejar infecções intestinais severas e reduzir a dependência de fármacos convencionais.
Citação: Ma, G., Liu, R., Li, X. et al. Engineered bacterial therapy suppresses Enterohemorrhagic Escherichia coli through metabolic competition and virulence silencing. Nat Commun 17, 2307 (2026). https://doi.org/10.1038/s41467-026-69126-4
Palavras-chave: probióticos projetados, terapia para infecções intestinais, EHEC, microbioma, microesferas para entrega de fármacos