Clear Sky Science · pt
Dopante dinâmico de cromo promove ativação da água na interface em óxido spinel de cobalto para evolução de oxigênio eficiente em ambiente ácido
Por que esta pesquisa importa para a energia limpa
Produzir combustível de hidrogênio a partir da água poderia alimentar a indústria e o transporte sem emissões de carbono, mas os dispositivos mais eficientes hoje dependem de metais preciosos raros e caros. Este estudo investiga como um material de baixo custo, cuidadosamente projetado com base em cobalto e cromo, pode substituir esses metais em uma das etapas mais difíceis da separação da água: gerar oxigênio em condições ácidas, como nas eletrólises de água com membrana de troca de prótons no estilo comercial (PEMWEs). 
O desafio de gerar oxigênio a partir da água
As PEMWEs modernas são atraentes porque convertem rapidamente eletricidade de solar ou eólica em hidrogênio, mesmo quando a alimentação de energia oscila. Contudo, no lado produtor de oxigênio desses dispositivos, a reação é lenta e severa. Ela ocorre em um ambiente ácido e envolve o movimento acoplado de prótons e elétrons. Atualmente essa etapa costuma ser realizada por catalisadores de óxidos de irídio e rutênio — metais escassos e caros. O óxido de cobalto (Co3O4) surgiu como uma alternativa promissora, mas em meio ácido tende a corroer: átomos de cobalto se dissolvem no líquido, a superfície se sobreoxida formando fases instáveis e o catalisador se degrada progressivamente.
Um ajuste inteligente: adicionar átomos de cromo
Os autores mostram que a introdução de uma pequena quantidade de cromo no óxido spinel de cobalto remodela tanto a estrutura eletrônica interna do sólido quanto a fina camada de água em sua superfície. Eles sintetizam nanopartículas minúsculas e uniformes de óxido de cobalto dopado com cromo (Cr‑Co3O4) e confirmam, por difração e microscopia eletrônica, que o material preserva a estrutura spinel original. Técnicas espectroscópicas avançadas revelam que os átomos de cromo se acomodam em posições tetraédricas específicas na rede e estão dispersos como átomos isolados, em vez de formarem partículas separadas de óxido de cromo. Esse arranjo cria um ambiente local cromo‑oxigênio‑cobalto que reduz ligeiramente a carga média nos átomos de cobalto, tornando‑os menos propensos à sobreoxidação.
Melhor desempenho em condições ácidas severas
Quando testado em ácido sulfúrico, o catalisador dopado com cromo precisa de muito menos sobretensão que o óxido de cobalto não dopado para atingir a mesma densidade de corrente, indicando que acelera a produção de oxigênio. Ele também supera os óxidos comerciais de rutênio e irídio em densidades de corrente mais altas e, o que é crucial, mantém sua atividade por pelo menos 160 horas, enquanto os outros catalisadores se degradam. Medições elétricas mostram que a carga se move com mais facilidade através da interface entre o catalisador dopado e o líquido. Quando integrado a um dispositivo completo de eletrólise com PEM, o Cr‑Co3O4 usado como catalisador no lado do oxigênio, pareado com um catalisador padrão de platina no lado do hidrogênio, opera de forma estável por mais de 750 horas em correntes relevantes para a indústria, demonstrando durabilidade prática.
Como o cromo remodela a camada de água
Para ir além de números de desempenho, os pesquisadores investigam como a superfície do catalisador e as moléculas de água próximas evoluem durante a operação. Medições in situ por raios X e Raman mostram que, no óxido de cobalto puro, os átomos de cobalto se sobreoxidam fortemente em altas voltagens, um precursor da degradação estrutural. No material dopado, em contraste, o estado de oxidação do cobalto permanece quase constante enquanto o cromo muda gradualmente, indicando que o cromo atua como um “amortecedor” eletrônico que protege o cobalto. Medições sensíveis à superfície revelam ainda que, sob tensões de operação, os átomos de cromo ligam‑se progressivamente a grupos hidroxila (OH). Essas hidroxilas de superfície alteram a estrutura da camada de água em contato com o eletrodo: espectroscopia no infravermelho mostra que as redes de ligações de hidrogênio enfraquecem e que a fração de moléculas de água mais móveis, mais “livres”, aumenta. Como essas moléculas de água se dissociam mais facilmente, a reação que transforma água em oxigênio acelera. 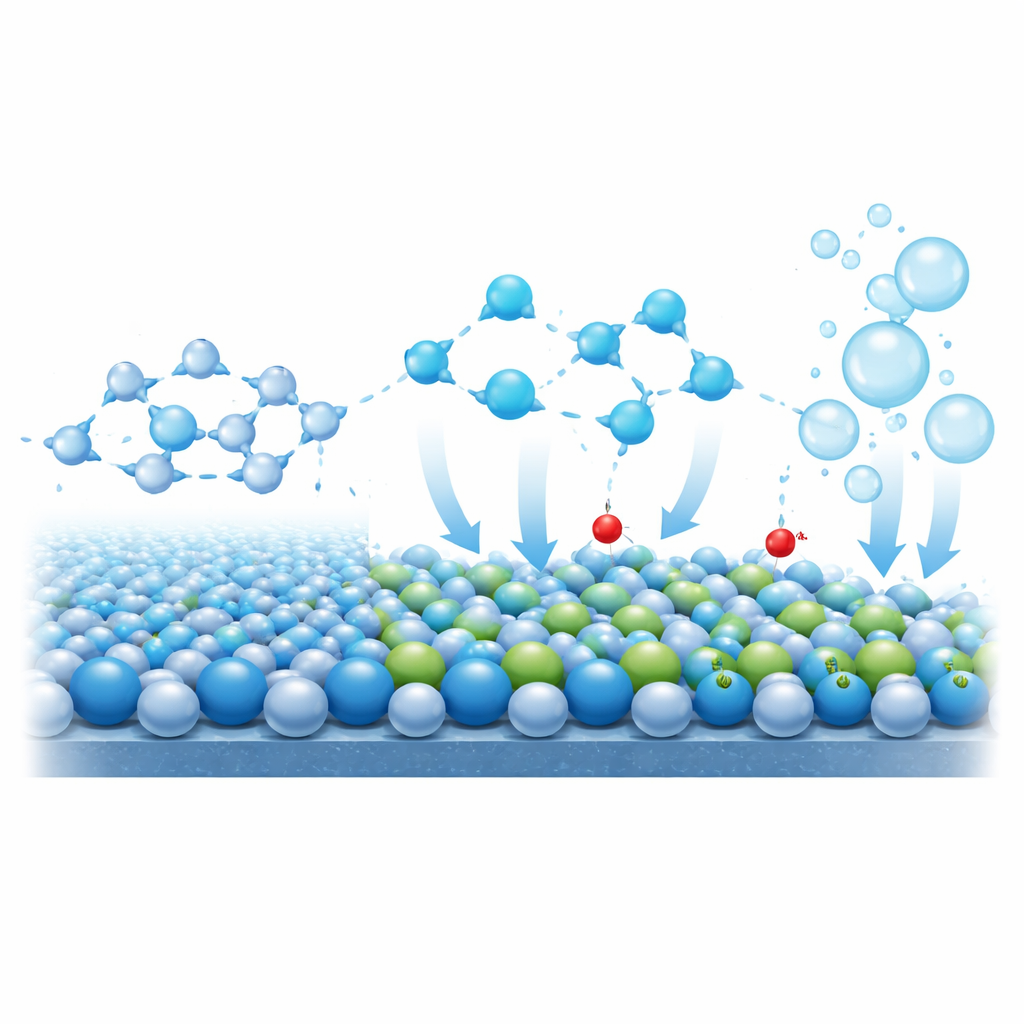
Conectando teoria e experimento
Simulações computacionais corroboram esse quadro. Cálculos mostram que o cromo prefere os mesmos sítios na rede identificados experimentalmente e tende a doar densidade eletrônica para o cobalto vizinho. A energia necessária para dividir uma molécula de água na superfície dopada é menor do que no óxido de cobalto puro, especialmente quando já existe uma hidroxila no sítio de cromo, refletindo o achado experimental de que superfícies ricas em hidroxila são mais ativas. As simulações também indicam que arrancar um átomo de cobalto da superfície dopada requer mais energia, explicando a maior resistência à dissolução. Diagramas gerais de energia de reação confirmam que a etapa mais difícil na sequência de formação de oxigênio fica mais fácil depois da introdução do cromo.
O que isso significa para futuros dispositivos de eletrólise
Conjuntamente, esses resultados mostram que uma pequena quantidade do dopante certo pode mudar dramaticamente o comportamento tanto dos elétrons quanto das moléculas de água na superfície de um catalisador. Ao usar o cromo para estabilizar o cobalto e fomentar uma camada de água facilmente ativada e fracamente ligada, a equipe cria um catalisador robusto, sem metais preciosos, que rivaliza com óxidos nobres em condições ácidas exigentes. Para o leitor leigo, a conclusão principal é que a engenharia atômica inteligente — alguns átomos de cromo nos locais certos — pode fazer com que materiais acessíveis realizem o trabalho árduo de dividir a água, aproximando a produção em larga escala de hidrogênio verde da realidade.
Citação: Wu, L., Zhao, B., Huang, W. et al. Dynamic chromium dopant promotes interfacial water activation on cobalt spinel oxide for efficient oxygen evolution in acid. Nat Commun 17, 2598 (2026). https://doi.org/10.1038/s41467-026-69124-6
Palavras-chave: hidrogênio verde, eletrólise da água, reação de evolução do oxigênio, catalisador de óxido de cobalto, água na interface