Clear Sky Science · pt
Um fosfaalumeno(3) isolável capaz de ativação de pequenas moléculas por modos únicos de reatividade
Quebrando ligações resistentes com uma nova ferramenta química
Químicos estão sempre em busca de maneiras de persuadir moléculas relutantes a reagir. Muitas substâncias comuns, do hidrogênio molecular ao dióxido de carbono, são notavelmente estáveis, o que as torna difíceis de transformar em produtos úteis. Este artigo relata uma molécula recém‑projetada, composta de alumínio e fósforo, capaz de se ligar a esses parceiros resistentes e abrir suas ligações. Entender e controlar esse tipo de ativação de ligação pode, no futuro, ajudar a transformar gases residuais em matérias‑primas ou oferecer rotas mais suaves e economizadoras de metais para produzir produtos químicos finos e materiais.
Uma ligação desenhada entre alumínio e fósforo
No cerne do estudo está um tipo raro de conexão entre dois elementos dos grupos principais: alumínio e fósforo. Os pesquisadores elaboraram uma molécula, chamada “3” no artigo, na qual esses dois átomos compartilham uma ligação dupla compacta. Para evitar que esse par reativo se desmonte, eles o envolveram em uma estrutura orgânica voluminosa que o protege de reações acidentais. Usando duas rotas sintéticas diferentes, obtiveram esse complexo em forma isolável e cultivaram cristais individuais adequados para difração de raios X, confirmando que o fósforo está ligado ao alumínio por uma ligação curta, semelhante a uma dupla ligação, enquanto cada átomo é suportado por ligantes contendo nitrogênio ao redor. Cálculos mostraram que os elétrons são compartilhados de forma desigual entre alumínio e fósforo, tornando a ligação polarizada e pronta para ser atacada por outras moléculas.
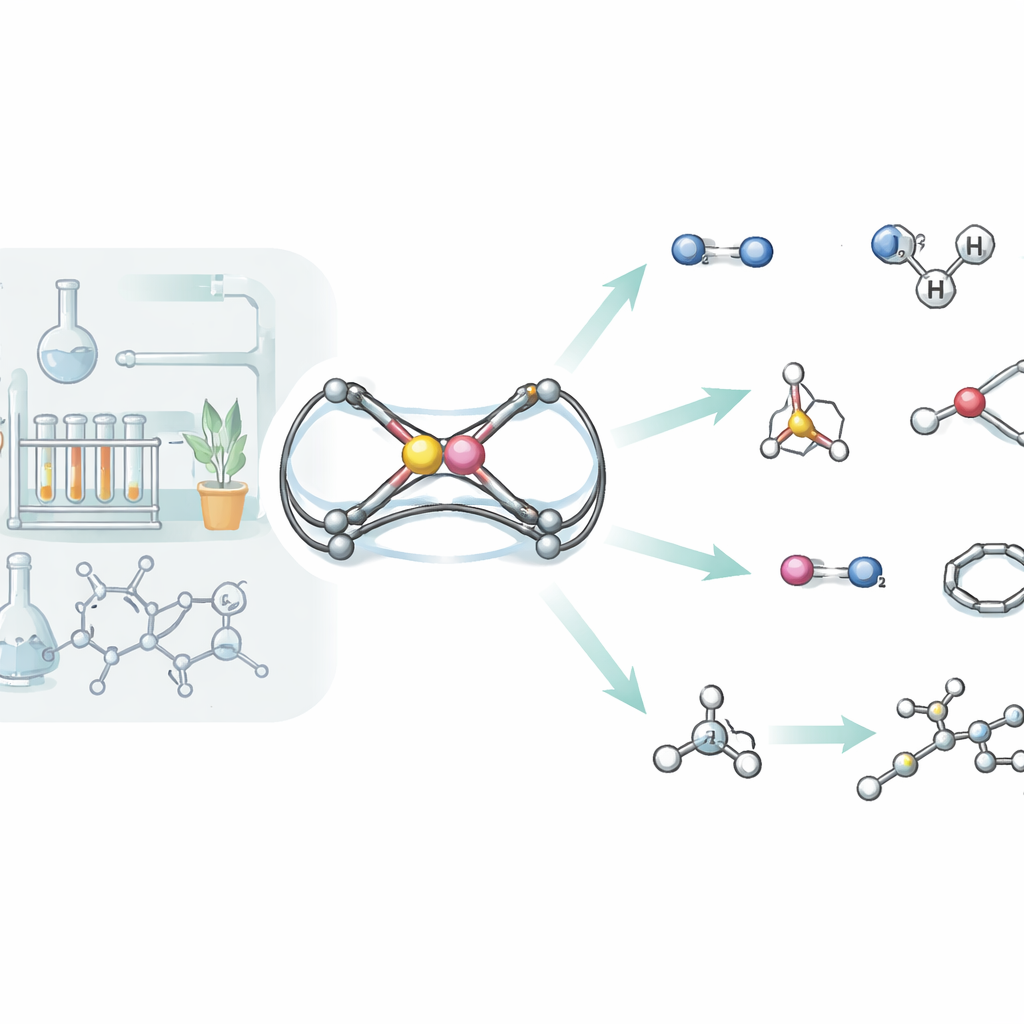
Como a nova molécula lida com o hidrogênio gasoso
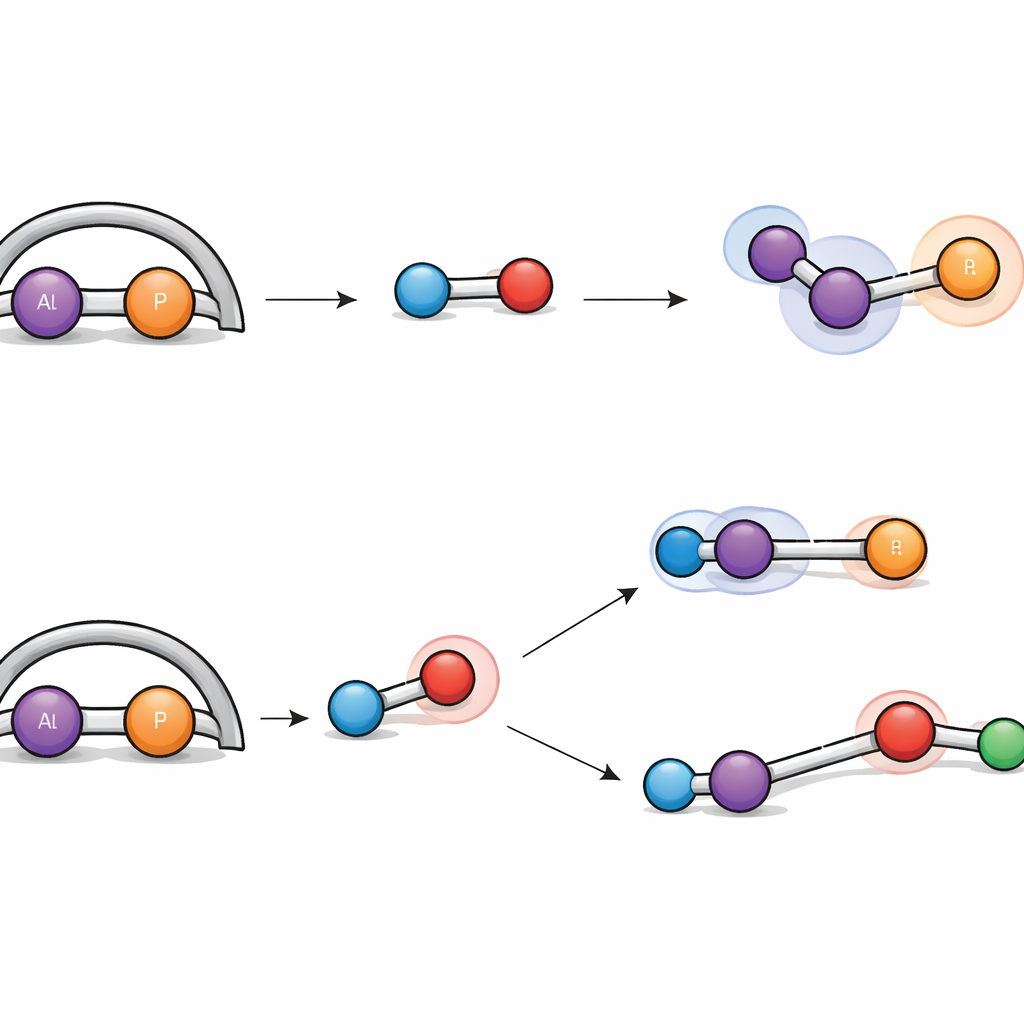
O hidrogênio gasoso é notoriamente difícil de dividir sem o uso de metais preciosos, ainda assim a nova unidade alumínio‑fósforo consegue justamente isso. Quando exposto ao hidrogênio em condições brandas, o complexo reage de duas maneiras distintas. Em uma via, a ligação H–H simplesmente adiciona‑se sobre a ligação dupla alumínio–fósforo, convertendo‑a em duas ligações simples e anexando um hidrogênio a cada átomo. Na outra, a molécula de hidrogênio é dissociada cooperativamente pelo alumínio e por um átomo de nitrogênio vizinho, um comportamento que lembra os chamados “pares de Lewis frustrados”, que ativam hidrogênio sem catalisadores metálicos tradicionais. Simulações computacionais detalhadas traçaram ambas as rotas, mostrando que suas barreiras energéticas são semelhantes, o que explica por que ambos os produtos se formam lado a lado.
Desmontando uma galeria de pequenas moléculas
O hidrogênio é apenas o começo. A equipe testou sistematicamente como sua estrutura alumínio‑fósforo reage com uma ampla gama de pequenas moléculas, incluindo fósforo branco, isocianetos, dióxido de carbono, óxido nitroso, azida de trimetilsilila, dímeros de selênio, silanos, aminas, estireno e alcinos simples. Em muitas dessas reações, a ligação Al=P original é completamente rompida, com os dois átomos terminando em estruturas maiores em forma de gaiola ou anel que incorporam fragmentos da molécula reagente. Por exemplo, o fósforo branco (P4) é aberto e reconstruído em uma gaiola alumínio‑fósforo, enquanto o dióxido de carbono se insere duas vezes para formar um anel de seis membros que conecta alumínio e fósforo por meio de duas novas pontes carbono‑oxigênio. Com silanos e aminas, a molécula comporta‑se mais como uma ligação dupla clássica: a unidade Si–H ou N–H adiciona‑se de modo ordenado através de Al=P, demonstrando novamente o caráter de “ligação π” dessa ligação incomum.
Por que a estrutura circundante importa
Uma das lições-chave do trabalho é que a estrutura volumosa e rica em nitrogênio ao redor da unidade Al=P não é apenas um andaime; ela direciona como e onde as reações ocorrem. Ao comparar seus resultados com sistemas alumínio‑fósforo anteriores, mais efêmeros, os autores mostram que pequenas mudanças nos ligantes de suporte alteram o equilíbrio entre diferentes vias, como adição simples através da dupla ligação versus clivagem mais elaborada de ligações e formação de anéis. Análises sofisticadas da distribuição eletrônica revelaram forte polarização da ligação Al=P e destacaram como átomos de nitrogênio vizinhos podem cooperar com o alumínio, especialmente na ativação do hidrogênio. A massa estérica — o aglomerado físico de grandes grupos — também direciona as moléculas entrantes para um sítio reativo ou outro.
O que isso significa para a química futura
Para um não especialista, a sopa de letras de reagentes neste estudo pode parecer distante, mas a mensagem subjacente é clara: ao ajustar cuidadosamente tanto a ligação quanto a forma ao redor de elementos dos grupos principais, os químicos podem construir ferramentas ágeis que rivalizam ou complementam catalisadores metálicos tradicionais. Este complexo alumínio‑fósforo isolável não só sobrevive em um frasco, como também enfrenta um amplo conjunto de pequenas moléculas resistentes em condições brandas, clivando hidrogênio, rearranjando fósforo branco e capturando dióxido de carbono. O trabalho mostra que mudanças sutis no “manípulo” de uma molécula podem redirecionar profundamente sua reatividade, oferecendo um roteiro para projetar futuros catalisadores que ajudem a converter moléculas simples e estáveis em produtos mais valiosos com precisão e eficiência.
Citação: Cha, Y., Yang, Z., Zhuang, X. et al. An isolable phosphaalumene(3) capable of small molecule activation via unique modes of reactivity. Nat Commun 17, 2390 (2026). https://doi.org/10.1038/s41467-026-69118-4
Palavras-chave: ativação de pequenas moléculas, química dos elementos principais, ligação dupla alumínio‑fósforo, par de Lewis frustrado, mecanismos de ativação de ligação