Clear Sky Science · pt
Mecanismo de inibição das β−1,3-glucano sintetases fúngicas por antifúngicos triterpenóides
Por que conter infecções fúngicas é importante
Infecções por fungos matam silenciosamente mais de um milhão de pessoas a cada ano e ameaçam colheitas e ecossistemas em todo o mundo. Os médicos já trabalham com uma lista curta de medicamentos antifúngicos, e alguns fungos perigosos estão evoluindo para escapar dessas drogas. Este estudo revela, em detalhe molecular, como uma nova classe de antifúngicos se liga e desliga uma enzima-chave que os fungos precisam para construir sua parede celular protetora. Compreender esse processo oferece um roteiro para projetar tratamentos melhores que possam superar fungos resistentes.
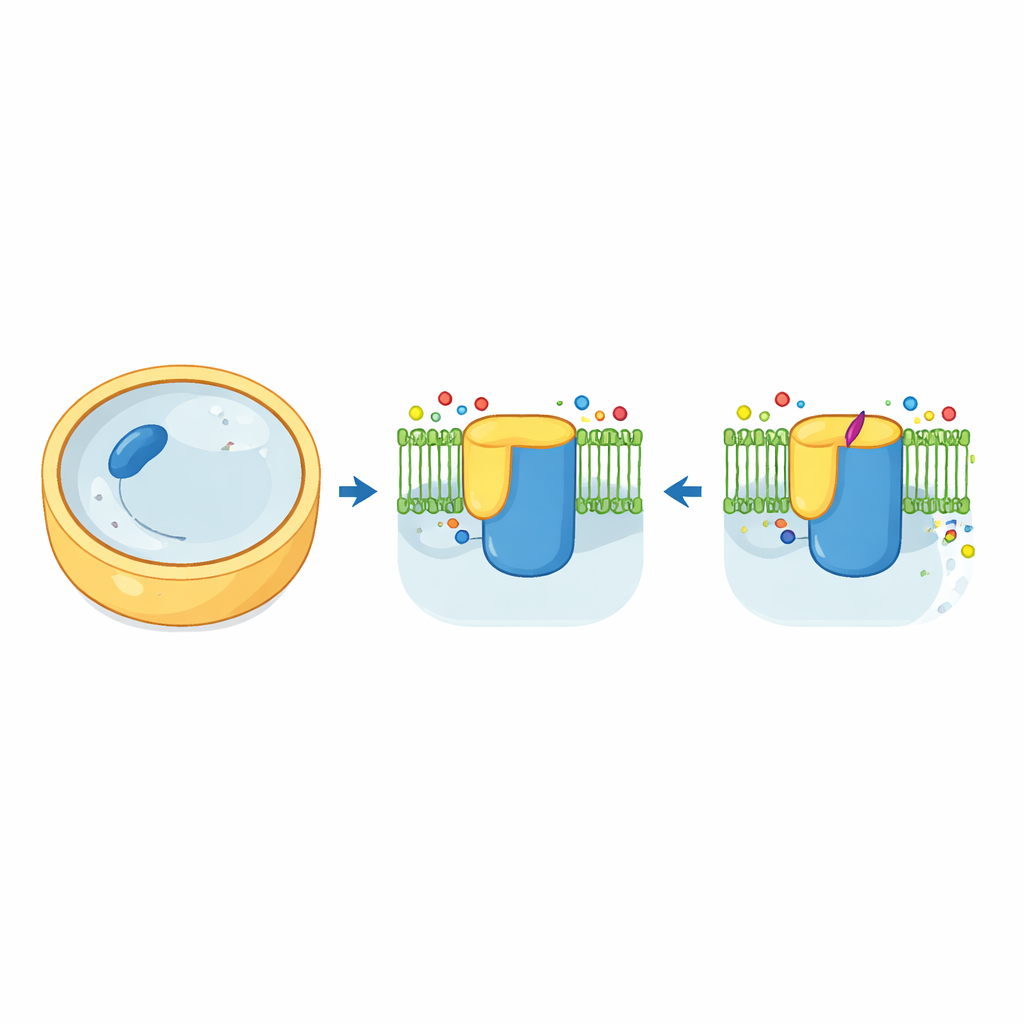
O fabricante de “tijolos” da parede celular fúngica
Células fúngicas são envoltas por uma parede resistente feita em grande parte de um polímero de açúcar chamado beta-1,3-glucano. A enzima que fabrica e exporta esse polímero, conhecida como beta-1,3-glucano sintetase, atua como um fabricante de tijolos combinado com uma esteira transportadora. Em levedura de padeiro, essa máquina é composta por duas versões muito semelhantes, Fks1 e Fks2, cada uma embutida na membrana celular e controlada por uma pequena proteína auxiliar chamada Rho1. Usando crio-microscopia eletrônica, os autores capturaram vistas tridimensionais de alta resolução de Fks1 e Fks2 em sua forma natural. As estruturas revelam um grande “banco de trabalho” citosólico ligado a uma floresta de hélices que atravessam a membrana, com uma cavidade central que provavelmente serve como túnel por onde a cadeia crescente de glucano sai da célula.
Como um fármaco de produto natural agarra a enzima
Drogas triterpenóides clinicamente importantes, incluindo o medicamento oral ibrexafungerp, têm origem em um composto natural chamado enfumafungina. Até agora, ninguém sabia exatamente onde essas drogas se ligam na glucano sintetase. Os pesquisadores resolveram estruturas de Fks1 e Fks2 ligadas à enfumafungina. Surpreendentemente, o fármaco não se encaixa no sítio ativo onde as unidades de açúcar são unidas. Em vez disso, ele se aloja na porção externa de uma única hélice transmembrana chamada TM5, posicionando-se na membrana cerca de três nanômetros afastado do centro catalítico e próximo ao provável canal de saída do glucano. Aminoácidos-chave nessa região abraçam o núcleo hidrofóbico do fármaco e fazem contato com sua cauda ácida, enquanto seu apêndice açucarado mal toca a proteína — o que explica por que químicos puderam modificar essa parte sem perder potência.
Drogas que congelam uma máquina em movimento
A primeira vista, a forma geral da enzima com e sem enfumafungina parece quase inalterada. A diferença crucial está em como os lipídios circundantes são organizados e em quão flexíveis certas hélices são. Quando o fármaco se liga, uma cadeia lateral aromática próxima gira para prender a enfumafungina no lugar e, junto com outro resíduo, estabiliza um lipídio ordenado ao lado do fármaco. Lipídios adicionais com aparência de esterol tornam-se organizados ao redor de um conjunto de hélices horizontais que ajudam a definir o caminho para a exportação do glucano. Esses lipídios atuam como cunhas e suportes, trancando as hélices e a entrada do canal em um arranjo “basal” específico. Testes genéticos mostram que alterar muitos pontos de contato do fármaco ou desses esteróis enfraquece a ligação do fármaco ou destrói a função da enzima, e mutações nesses sítios coincidem com mutações de resistência conhecidas em patógenos humanos e de plantas.
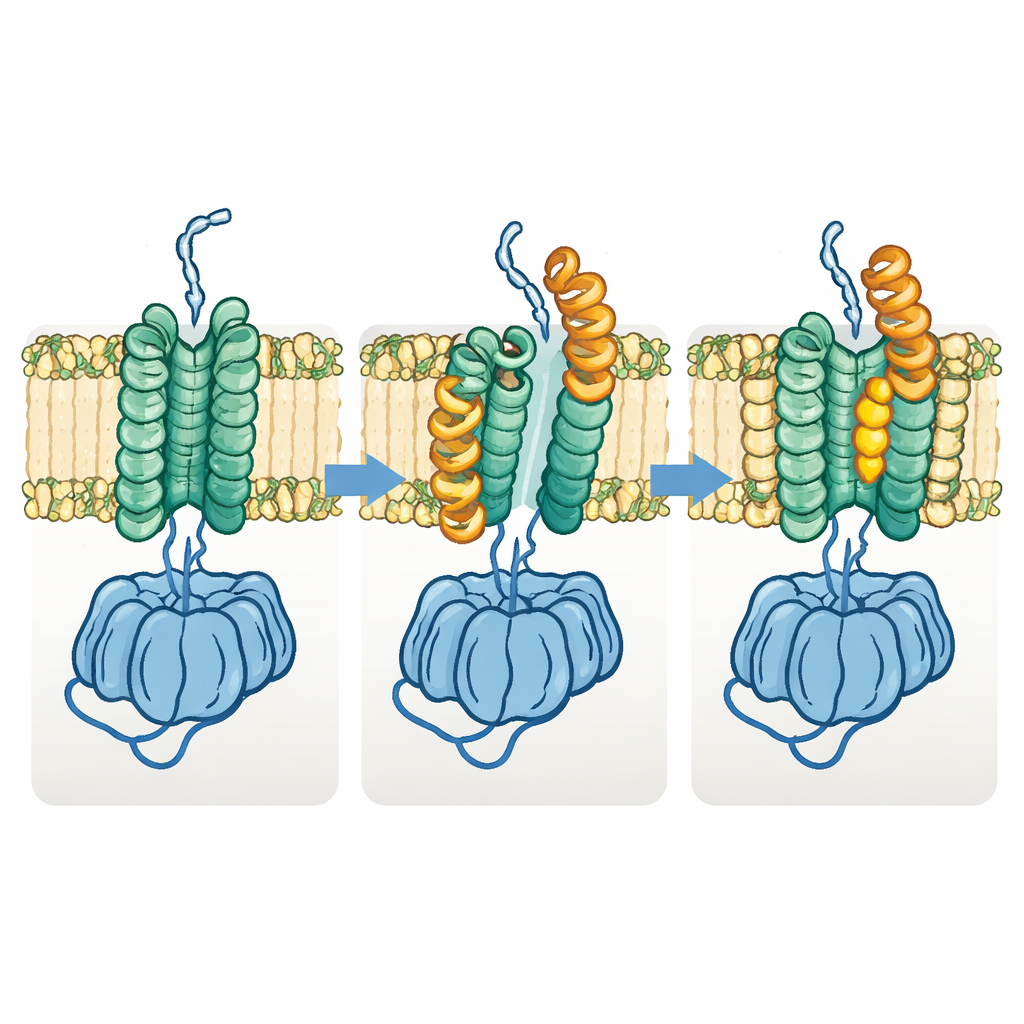
Uma mudança de forma necessária para o transporte do polímero
A equipe também descobriu uma forma distinta “aberta” de Fks1. Nesse estado, metade da região transmembrana desloca-se lateralmente e hélices horizontais-chave giram para fora, abrindo o espaço entre os dois feixes de membrana e ampliando o aparente túnel do glucano. A comparação de muitas estruturas sugere que a enzima cicla entre os estados basal e aberto durante a operação normal: o estado basal prepara e inicia a formação do polímero, enquanto o estado aberto permite que a cadeia em crescimento se mova lateralmente através da membrana em direção ao exterior. Quando os autores projetaram ligações dissulfeto destinadas a travar a enzima permanentemente em qualquer um dos estados, ambas as variantes perderam em grande parte a atividade, sustentando a ideia de que essa mudança de forma é essencial para a função.
O que isso significa para futuros antifúngicos
Ao mostrar que a enfumafungina e drogas relacionadas atuam não bloqueando o bolso catalítico, mas remodelando o ambiente lipídico local e congelando a glucano sintetase em seu estado basal, este estudo revela um modo de ação de fármaco não convencional. Também demonstra que Fks1 e Fks2 compartilham estruturas e respostas a fármacos quase idênticas, explicando por que ambos devem ser considerados ao enfrentar a resistência. Mais amplamente, o trabalho destaca como pequenas moléculas podem controlar proteínas de membrana “difíceis de drugar” ao se ligar a superfícies rasas e recrutar lipídios, oferecendo um plano conceitual para projetar antifúngicos de próxima geração que permaneçam eficazes mesmo enquanto os fungos evoluem.
Citação: You, ZL., Sun, L., Wang, LX. et al. Inhibition mechanism of the fungal β−1,3-glucan synthases by triterpenoid antifungal drugs. Nat Commun 17, 2347 (2026). https://doi.org/10.1038/s41467-026-69114-8
Palavras-chave: medicamentos antifúngicos, parede celular fúngica, glucano sintetase, resistência a medicamentos, crio-microscopia eletrônica