Clear Sky Science · pt
Estruturas por criomicroscopia eletrônica de intermediários da montagem portal-pescoço do bacteriófago T4 revelam um mecanismo de retenção do genoma viral
Como um vírus mantém seu DNA sob pressão
O bacteriófago T4 é um vírus que infecta a bactéria E. coli e empacota seu DNA tão firmemente dentro da cabeça que a pressão interna pode ser de cinco a sete vezes maior do que a de uma garrafa de champanhe. Mesmo assim, o DNA não vaza enquanto o vírus termina de construir o resto de seu corpo. Este estudo revela, em detalhe molecular, como o T4 resolve esse problema usando uma pequena dupla trava que funciona como uma antecâmara para seu material genético.
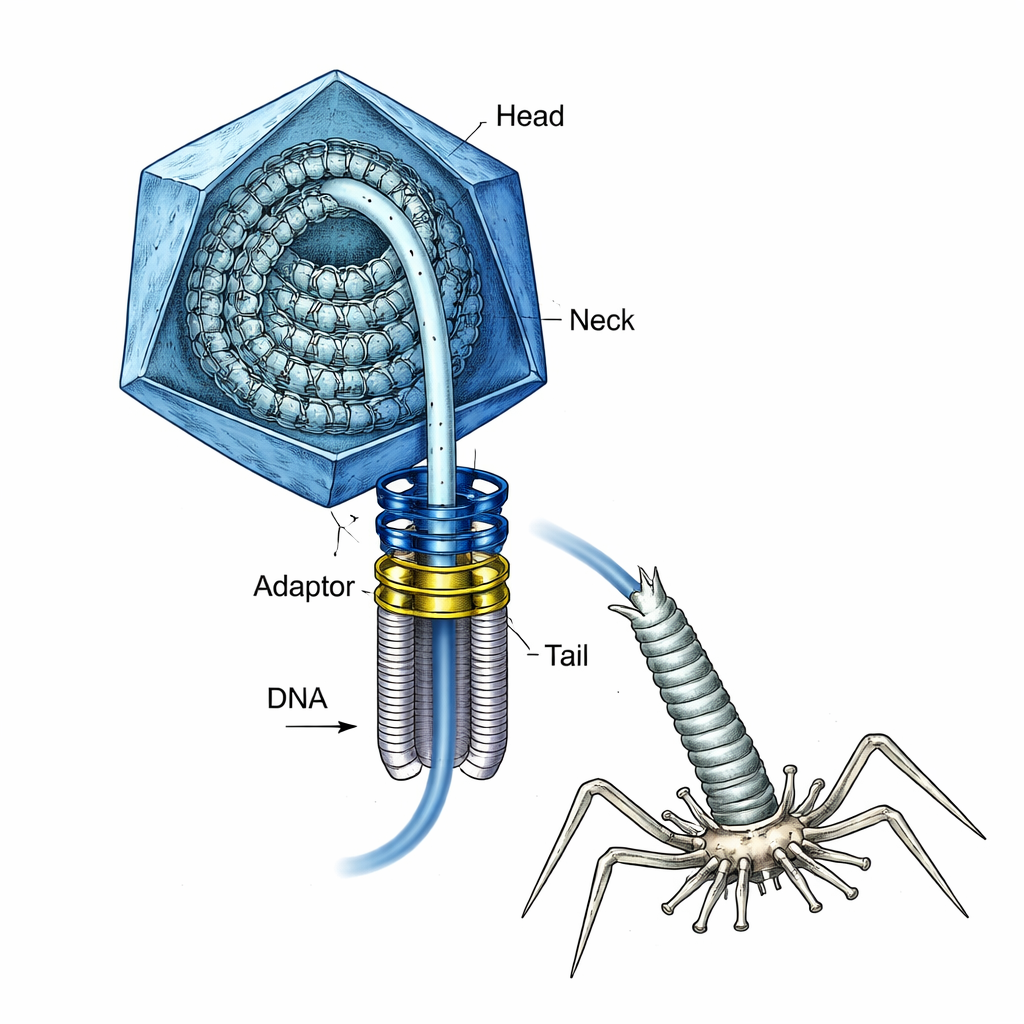
O vírus com uma mola carregada por dentro
O T4 há muito é uma ferramenta fundamental da biologia molecular e também serve de modelo para a construção de futuras vacinas e vetores de entrega gênica. Durante a montagem, o vírus primeiro constrói uma casca proteica vazia, ou cabeça, e um “portal” anelar especial em um dos vértices. Um potente motor molecular então enrola o DNA dentro da cabeça através desse portal até que a cabeça fique “cheia”. Nesse ponto, o motor deve se desprender, um pescoço e uma cauda devem ser anexados e, mais tarde, o DNA precisa ser injetado em uma bactéria — tudo sem permitir que o DNA pressurizado jorre para fora prematuramente. Como o vírus mantinha esse DNA altamente tensionado contido com segurança durante essas transições não era bem compreendido.
Reconstruindo o pescoço em laboratório
Os pesquisadores recriaram peças-chave do T4 em bactérias e as misturaram de formas controladas para observar como o pescoço — o conector entre cabeça e cauda — se monta. Duas proteínas virais, chamadas gp13 e gp14, foram produzidas separadamente. Sozinhas, flutuavam como unidades únicas, mas juntas se encaixavam em anéis empilhados que formam um túnel central para a passagem do DNA. Para surpresa dos cientistas, uma terceira proteína aparecia nessas preparações: Hfq, uma proteína bacteriana bem conhecida que normalmente ajuda a controlar RNA e a atividade gênica em E. coli. A espectrometria de massa confirmou que Hfq se ligava especificamente à gp14, sugerindo que o vírus toma emprestado essa proteína do hospedeiro como parte de seu pescoço.
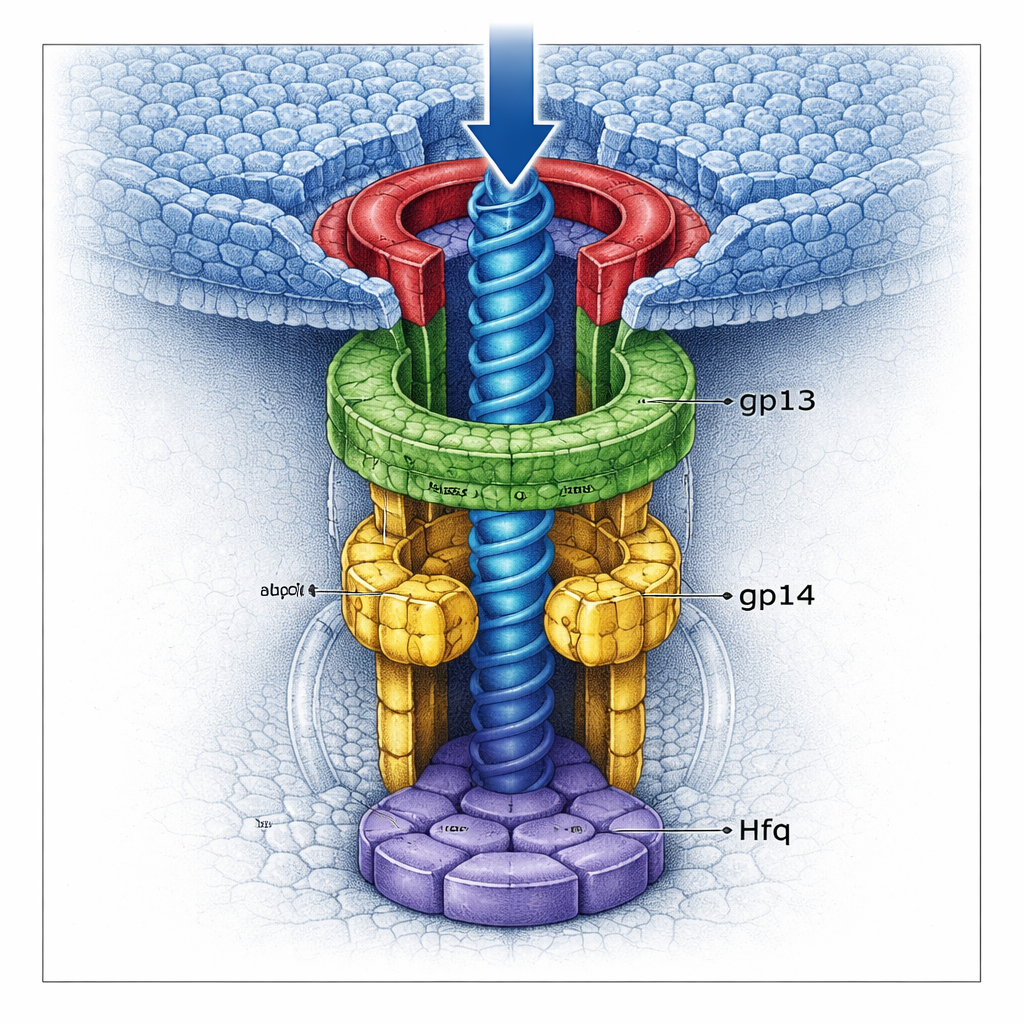
Uma dupla trava que prende o genoma
Usando criomicroscopia eletrônica de alta resolução, a equipe visualizou várias versões do complexo de pescoço em detalhe quase atômico. Eles descobriram que a gp13 forma um anel amplo que se adapta ao portal, enquanto a gp14 fica abaixo dele como um hexâmero, criando um canal mais estreito. Crucialmente, cada subunidade de gp14 contribui com uma longa alça que se projeta para o centro do túnel. Juntas, seis dessas “alças tampão” formam uma trava apertada que pode capturar o último segmento de DNA quando ele tenta sair da cabeça. Abaixo da gp14, a proteína Hfq sequestrada monta seu próprio hexâmero, tampando a base do canal como uma segunda porta. Quando o Hfq está presente, a estrutura gp13–gp14 fica mais completa e rígida, e as portas combinadas contraem ainda mais o túnel, tornando o vazamento de DNA muito menos provável.
Temporização, prevenção de erros e uma ajudante emprestada
O estudo também mostra que esse sistema é mais do que um tampão estático; é uma sequência cuidadosamente coreografada de mudanças conformacionais. Uma vez que a cabeça está cheia, a pressão interna empurra o portal para uma nova conformação que expõe sítios de ligação para a gp13. Um pescoço pré-montado gp13–gp14–Hfq então encaixa-se no portal. A gp13 flexiona, sobe e trava tanto no portal quanto na casca externa, entrelaçando o pescoço firmemente à cabeça. Ao longo dessa etapa, as alças tampão da gp14 e o tampão Hfq mantêm o DNA no lugar. O Hfq desempenha um segundo papel como fator de controle de qualidade: ao ocupar superfícies-chave na gp14, ele impede que a gp14 se ligue ao portal na posição errada, o que causaria a montagem inadequada do pescoço. Somente quando a cauda pré-construída chega é que uma proteína da ponta da cauda, a gp15, forma uma ligação ainda mais forte com a gp14, deslocando o Hfq e abrindo caminho para a liberação controlada do DNA para a cauda.
Por que isso importa além de um vírus
Em termos simples, o T4 usa uma trava de segurança de duas portas para conter uma poderosa “mola” de DNA enquanto termina de montar o resto do vírus. A primeira porta é construída a partir de sua própria proteína de pescoço, a gp14, e a segunda porta é tomada emprestada da proteína Hfq do hospedeiro, que o vírus usa temporariamente e depois descarta. Essa dupla trava garante que quase nenhum DNA seja perdido e que o vírus final seja totalmente infeccioso. Como muitos grandes vírus empacotam seus genomas sob pressões extremas semelhantes e compartilham uma arquitetura relacionada, este trabalho sugere que sistemas de travamento comparáveis, e até o sequestro temporário de proteínas do hospedeiro, podem ser comuns. Entender esses mecanismos pode orientar o desenho de vetores virais mais seguros para a medicina e apontar novas maneiras de bloquear vírus nocivos ao visar suas “travas” do genoma.
Citação: Han, L., Mao, Q., Zhu, J. et al. Cryo-EM structures of bacteriophage T4 portal-neck assembly intermediates reveal a viral genome retention mechanism. Nat Commun 17, 1964 (2026). https://doi.org/10.1038/s41467-026-69107-7
Palavras-chave: bacteriófago T4, montagem viral, crio-microscopia eletrônica, empacotamento do genoma, interação hospedeiro–vírus