Clear Sky Science · pt
Base estrutural da pausa durante a iniciação da transcrição em Mycobacterium tuberculosis
Como os interruptores genéticos de um germe podem travar
Mycobacterium tuberculosis, a bactéria que causa a tuberculose, precisa ligar e desligar genes constantemente para sobreviver no ambiente hostil do organismo. O trabalho descrito neste artigo investiga um dos passos iniciais desse controle genético, capturando uma “pausa” fugaz que ocorre justamente quando a célula começa a transcrever o DNA em RNA. Compreender essa pausa ajuda a explicar como o microrganismo decide se vai ativar totalmente um gene ou abortar a tentativa — e pode, eventualmente, revelar novos pontos fracos para antibióticos.
Iniciando a mensagem a partir do DNA
Em bactérias, uma grande máquina proteica chamada RNA polimerase percorre o DNA para produzir RNA, o primeiro passo rumo à produção de proteínas. Para começar, ela se associa a proteínas auxiliares conhecidas como fatores sigma, que a guiam a sítios específicos de início no DNA e ajudam a abrir uma pequena “bolha” na dupla hélice. Em Mycobacterium tuberculosis, um desses auxiliares, chamado sigma E, é especialmente importante quando a bactéria está sob estresse fora de sua membrana celular interna. Outro fator, CarD, ajuda a estabilizar a bolha de DNA aberta. Juntos, esses componentes formam um complexo de iniciação que sintetiza os primeiros blocos do RNA antes de ou se comprometer com uma mensagem de comprimento total ou desistir e liberar fragmentos curtos de RNA.
Uma pausa oculta com seis ou sete nucleotídeos
Estudos bioquímicos e em moléculas únicas anteriores sugeriam que a RNA polimerase frequentemente faz uma pausa muito cedo, quando a nova cadeia de RNA alcança apenas seis ou sete nucleotídeos. Mas essas pausas são extremamente breves e difíceis de observar diretamente, de modo que não havia estruturas de alta resolução disponíveis. Neste estudo, os autores usaram criomicroscopia eletrônica para congelar e visualizar múltiplas versões da maquinaria de iniciação de M. tuberculosis. Eles projetaram andaimes DNA–RNA que prendem o complexo quando o RNA tem seis ou sete unidades e resolveram estruturas para três estados principais: dois complexos de iniciação “regulares” e um complexo de iniciação em pausa distinto.
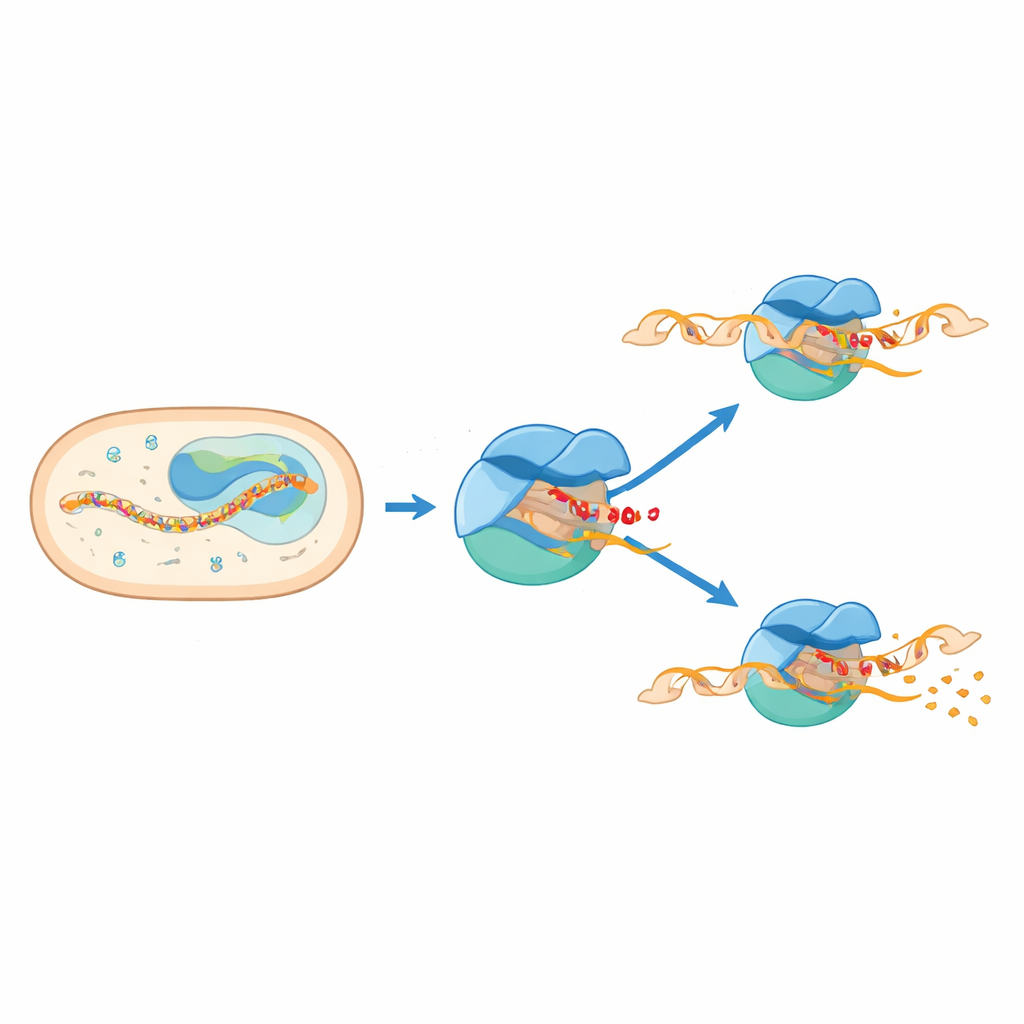
Quando duas partes da máquina colidem
As estruturas revelam que a pausa surge quando duas partes da maquinaria tentam ocupar o mesmo espaço. Um segmento flexível de sigma E, conhecido como região 3.2, se projeta no canal por onde o RNA em crescimento deve passar para sair da enzima. À medida que o RNA se alonga até seis ou sete unidades, sua ponta dianteira colide com esse laço saliente. Essa colisão força um movimento de rotação de um grande módulo dentro da RNA polimerase e distorce um elemento estrutural chave chamado helicoidal ponte. Ao mesmo tempo, o DNA imediatamente a montante do sítio ativo é puxado para dentro e parcialmente desenrolado, produzindo uma bolha “espremida” e com uma curvatura. Esses movimentos acoplados travam o complexo em um estado de pausa, meio avançado, que armazena tensão mecânica.
Um auxiliar que muda de forma estabiliza a bolha
CarD, o fator acessório, revela-se mais versátil do que se pensava. No complexo de iniciação não em pausa, CarD se insere no sulco menor de uma das fitas de DNA na borda da bolha, ajudando a manter a bolha aberta para que a RNA polimerase possa iniciar a síntese. No complexo em pausa, CarD move-se para envolver a fita de DNA oposta, a fita não molde, atuando em conjunto com sigma E para prender a bolha espremida com mais firmeza. Testes bioquímicos mostram que CarD aumenta a transcrição dependente de sigma E e influencia quantas moléculas de RNA se acumulam no estágio de seis a sete unidades. Esses achados sugerem que CarD tanto estabiliza o estado aberto inicial quanto ajuda o complexo em pausa a evitar o colapso prematuro.
Um ponto de checagem entre falha e compromisso
Ao comparar estruturas de alta resolução formadas em DNA parcialmente pré-aberto com estruturas de resolução mais baixa montadas em DNA totalmente pareado, os autores mostram que as mesmas formas básicas de pausa aparecem em condições mais naturais. Eles propõem que a colisão entre o RNA em crescimento e o laço 3.2 do sigma cria um ponto de checagem carregado de energia aos seis ou sete nucleotídeos de RNA. A partir desse estado preparado, o complexo pode seguir dois caminhos principais: pode liberar o RNA curto e reiniciar, uma tentativa abortiva, ou usar a tensão armazenada para se libertar da região do promotor e entrar em produção de RNA estável e de longo prazo. O reposicionamento de CarD e o afrouxamento da interação do fator sigma com o DNA a montante parecem orientar essa decisão.
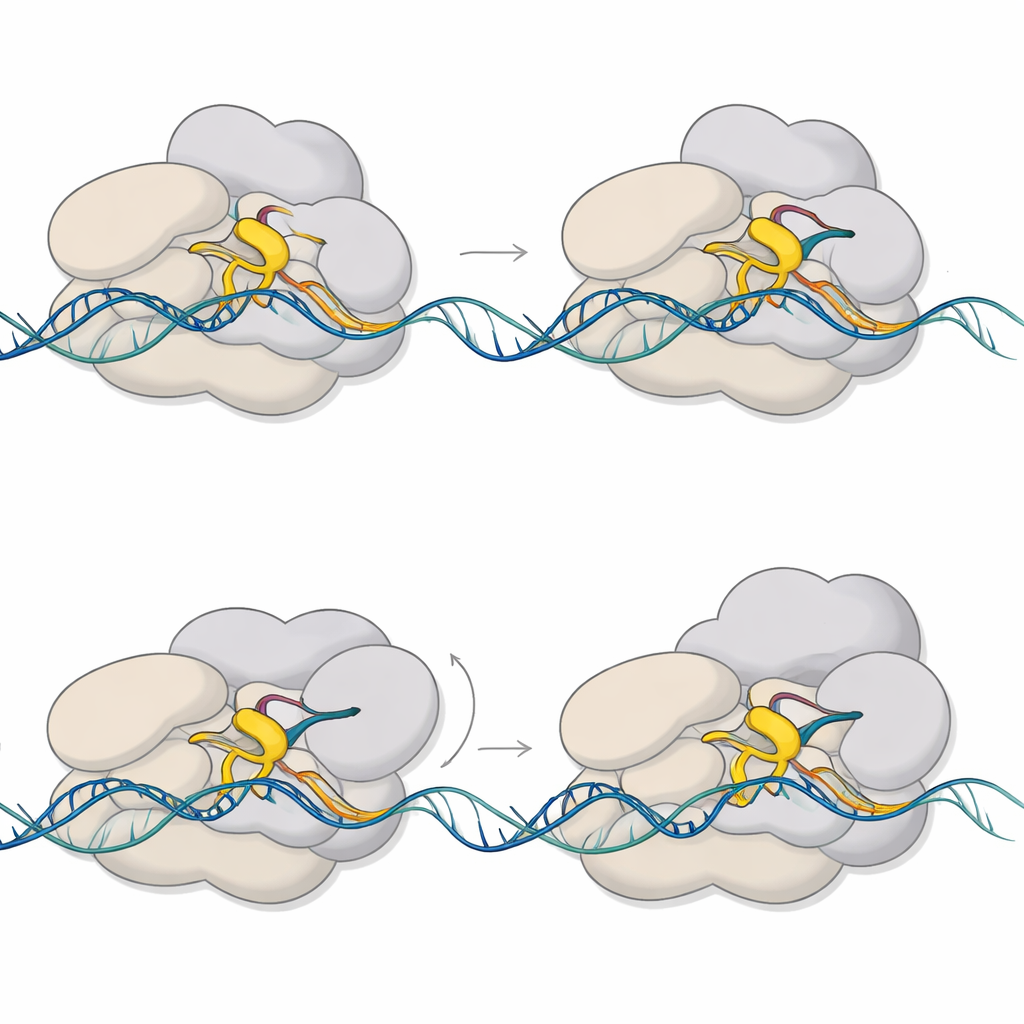
Por que isso importa para a tuberculose
Para um leitor leigo, a conclusão é que a bactéria da tuberculose não simplesmente liga genes como uma lâmpada. Em vez disso, ela hesita em um comprimento minúsculo de RNA, usando uma breve pausa mecânica como ponto de decisão entre abortar ou se comprometer com a ativação completa do gene. Este trabalho captura essa pausa em detalhe atômico, mostrando como um pequeno laço móvel, um núcleo que gira e uma bolha de DNA remodelada criam juntos um ponto de checagem controlável. Como sigma E e CarD são centrais para a resposta de M. tuberculosis ao estresse, esses insights podem, eventualmente, ajudar pesquisadores a projetar fármacos que travem esse passo inicial e reduzam a capacidade da bactéria de se adaptar e sobreviver.
Citação: Zheng, L., Xu, K. Structural basis of pausing during transcription initiation in mycobacterium tuberculosis. Nat Commun 17, 2197 (2026). https://doi.org/10.1038/s41467-026-69104-w
Palavras-chave: iniciação da transcrição, pausa da RNA polimerase, Mycobacterium tuberculosis, fatores sigma, crio-ME