Clear Sky Science · pt
ILC1s adiposos CD127+ induzidos por peritonite aguda expressam PD-L1 e atenuam a inflamação em camundongos
Por que a gordura abdominal pode ajudar a combater infecções letais
Quando bactérias vazam de um intestino perfurado para a cavidade abdominal, o corpo pode entrar em uma condição potencialmente fatal chamada sepse. Este estudo revela um aliado inesperado nessa luta: um conjunto especial de células imunes escondidas na gordura abdominal que migram para lá no início da infecção e funcionam como um freio integrado contra a inflamação descontrolada. Entender como essas células atuam pode inspirar novos tratamentos que acalmem infecções perigosas sem desligar completamente o sistema imune.
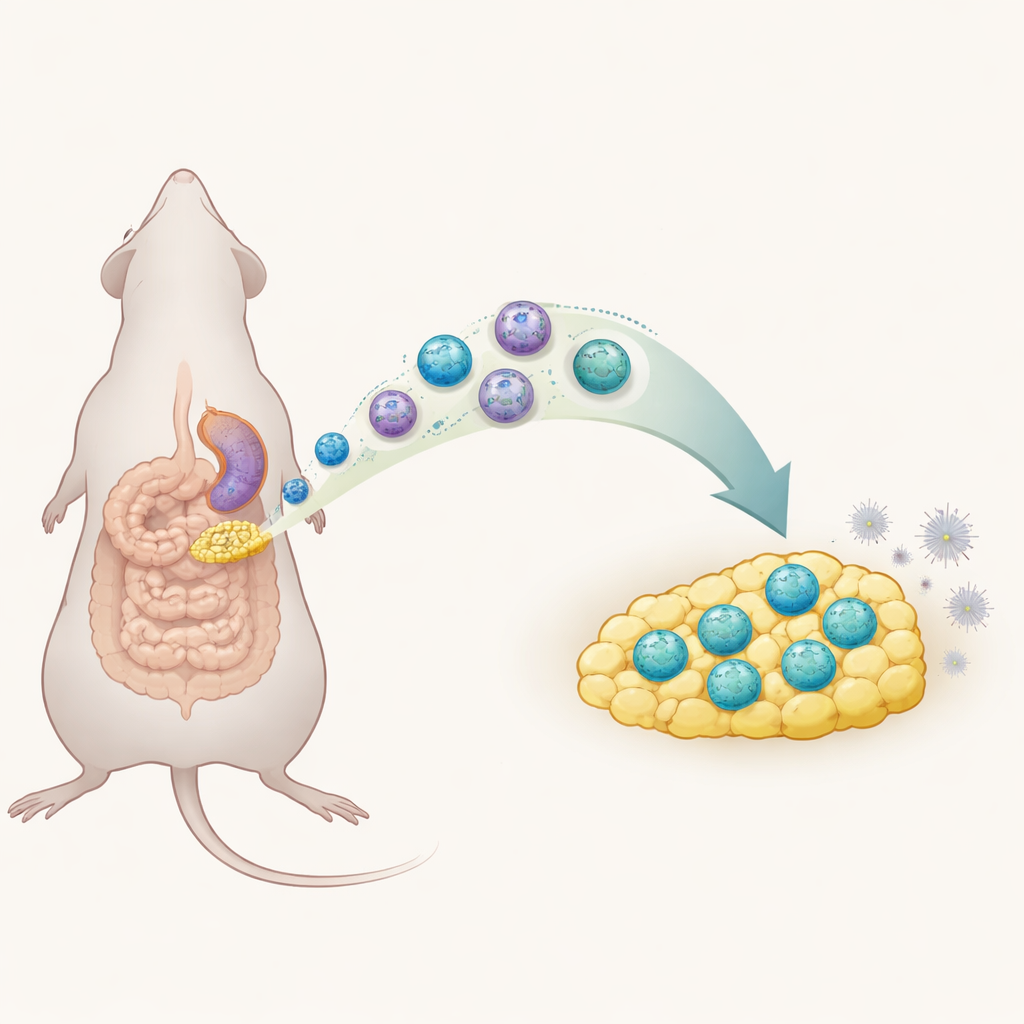
Um vazamento perigoso no abdome
A peritonite ocorre quando o revestimento da cavidade abdominal fica inflamado, na maioria das vezes porque bactérias escapam de um intestino perfurado. Se essa tempestade inicial de inflamação não for controlada, os pacientes podem desenvolver sepse, que ainda mata cerca de uma em cada cinco pessoas afetadas, apesar dos cuidados modernos. Os médicos podem tratar a infecção com cirurgia e antibióticos, mas dispõem de poucas ferramentas para direcionar a própria reação imune do corpo e evitar um excesso prejudicial. A gordura que recobre os intestinos, chamada tecido adiposo mesentérico, é conhecida por convergir para locais de dano intestinal, sugerindo que ela desempenha um papel ativo nessa resposta imune precoce.
Guardas ocultos na gordura abdominal
Nos últimos anos, os cientistas descobriram as “células linfoides inatas”, sentinelas imunes de ação rápida que vivem em muitos tecidos. Um subtipo, chamado ILCs do grupo 1, normalmente ajuda a desencadear reações inflamatórias fortes. Neste estudo com camundongos, os pesquisadores usaram um modelo cirúrgico padrão de peritonite para investigar como essas células se comportam no tecido adiposo mesentérico. Eles descobriram que, seis horas após a lesão, essa gordura apresentou sinais inflamatórios e um surto de células ILC1, enquanto outros tipos celulares relacionados quase não mudaram. Esse timing coincidiu com o pico de doença nos animais, sugerindo que as ILC1s estavam intimamente ligadas à fase inflamatória inicial no abdome.
Células viajantes que mudam sua natureza
Aprofundando-se, a equipe usou perfilamento avançado de célula única para dividir a população de ILC1 em subgrupos. Em condições normais, a maioria das ILC1s da gordura abdominal não expressava uma molécula chamada CD127 na superfície. Durante a peritonite aguda, no entanto, surgiu e se expandiu um novo grupo de ILC1s positivas para CD127. Esses recém‑chegados produziram menos da potente molécula inflamatória interferon‑gama do que suas contrapartes CD127‑negativas, indicando um comportamento incomumente contido. Os cientistas mostraram que muitas dessas células não apenas se dividiam localmente: em vez disso, ILC1s do baço viajaram pela corrente sanguínea até o tecido adiposo mesentérico, guiadas em parte por um sinal químico de “homing” chamado CXCL10 e seu receptor parceiro CXCR3. Uma vez na gordura, elas mudaram seus marcadores de superfície, adquirindo CD127 e adotando essa personalidade mais silenciosa e reguladora.
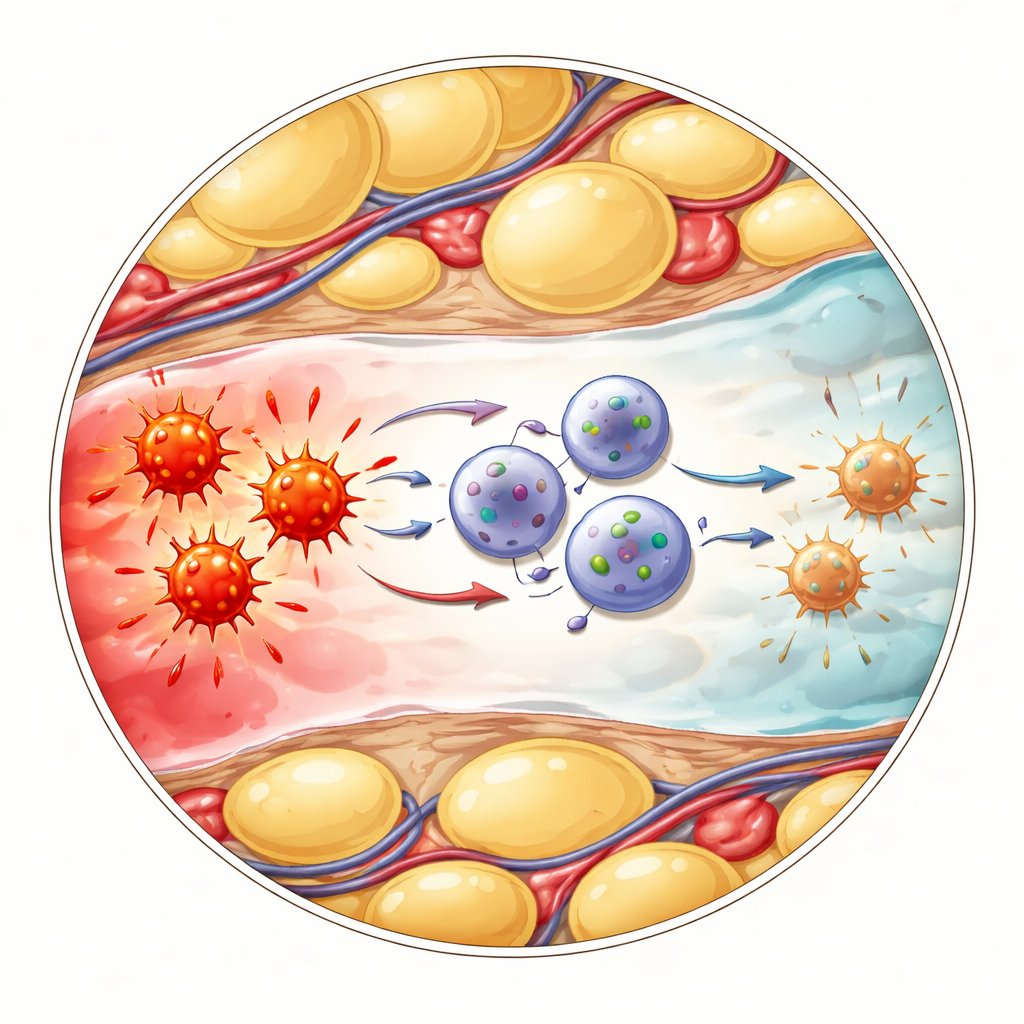
Como as células calmantes conversam com as células inflamadas
A próxima pergunta foi como essas ILC1s alteradas realmente reduziram a inflamação. Os pesquisadores focaram em outro grupo imune chamado células T gama‑delta, que respondem rapidamente ao perigo e podem liberar grandes quantidades da molécula de alarme TNF. Análises de célula única sugeriram que as ILC1s CD127‑positivas e as células T gama‑delta interagem por meio de uma via de “freio” bem conhecida envolvendo as proteínas de superfície PD‑L1 e PD‑1. Na gordura abdominal inflamada, as ILC1s recém‑chegadas aumentaram fortemente a expressão de PD‑L1, enquanto as células T gama‑delta próximas exibiram altos níveis de PD‑1. Quando a equipe bloqueou PD‑1 com anticorpos, as células T gama‑delta produziram mais TNF, confirmando que esse contato normalmente restringe sua saída inflamatória. Da mesma forma, camundongos geneticamente modificados para não ter ILC1s apresentaram doença mais grave, marcadores inflamatórios mais altos e aumento de TNF pelas células T gama‑delta — efeitos que puderam ser amenizados ao bloquear diretamente o TNF.
O que isso significa para tratamentos futuros
Ao juntar essas descobertas, os autores propõem um eixo “baço‑para‑gordura‑abdominal”: logo após as bactérias vazarem para o abdome, ILC1s deixam o baço, migram para o tecido adiposo mesentérico e lá se transformam em células ricas em CD127 e PD‑L1 que reduzem a produção de TNF pelas células T gama‑delta. Em vez de atiçar as chamas, essas ILC1s especializadas atuam como pacificadoras locais, evitando que a inflamação extrapole e possivelmente ajudando a impedir que a peritonite evolua para a sepse letal. A longo prazo, medicamentos que reforcem ou imitem esse circuito regulador na gordura abdominal poderiam oferecer uma nova maneira de tratar infecções graves — ajustando a resposta imune para que continue forte o suficiente para combater os germes, mas não tão intensa a ponto de colocar o paciente em risco.
Citação: Nagata, R., Akama, Y., Goncalves, P. et al. Acute peritonitis-induced adipose CD127+ ILC1s express PD-L1 and ameliorate inflammation in mice. Nat Commun 17, 2391 (2026). https://doi.org/10.1038/s41467-026-69100-0
Palavras-chave: peritonite, células linfoides inatas, tecido adiposo mesentérico, regulação imune, sepse