Clear Sky Science · pt
Melhorando a detecção de loops potenciador-promotor por meio de métodos de normalização para dados de interação de cromatina
Vendo os Laços Ocultos no Nosso DNA
Dentro de cada célula, longas fitas de DNA se dobram e formam laços em três dimensões, aproximando trechos distantes do genoma. Alguns desses laços conectam fisicamente interruptores liga-desliga chamados potenciadores (enhancers) aos genes que controlam, moldando como as células se desenvolvem e como doenças como o câncer surgem. Este artigo apresenta um novo método computacional, Raichu, que torna esses laços regulatórios sutis muito mais fáceis de detectar em experimentos genômicos em escala, abrindo uma janela mais nítida sobre como a dobra do DNA e a atividade gênica estão interligadas.
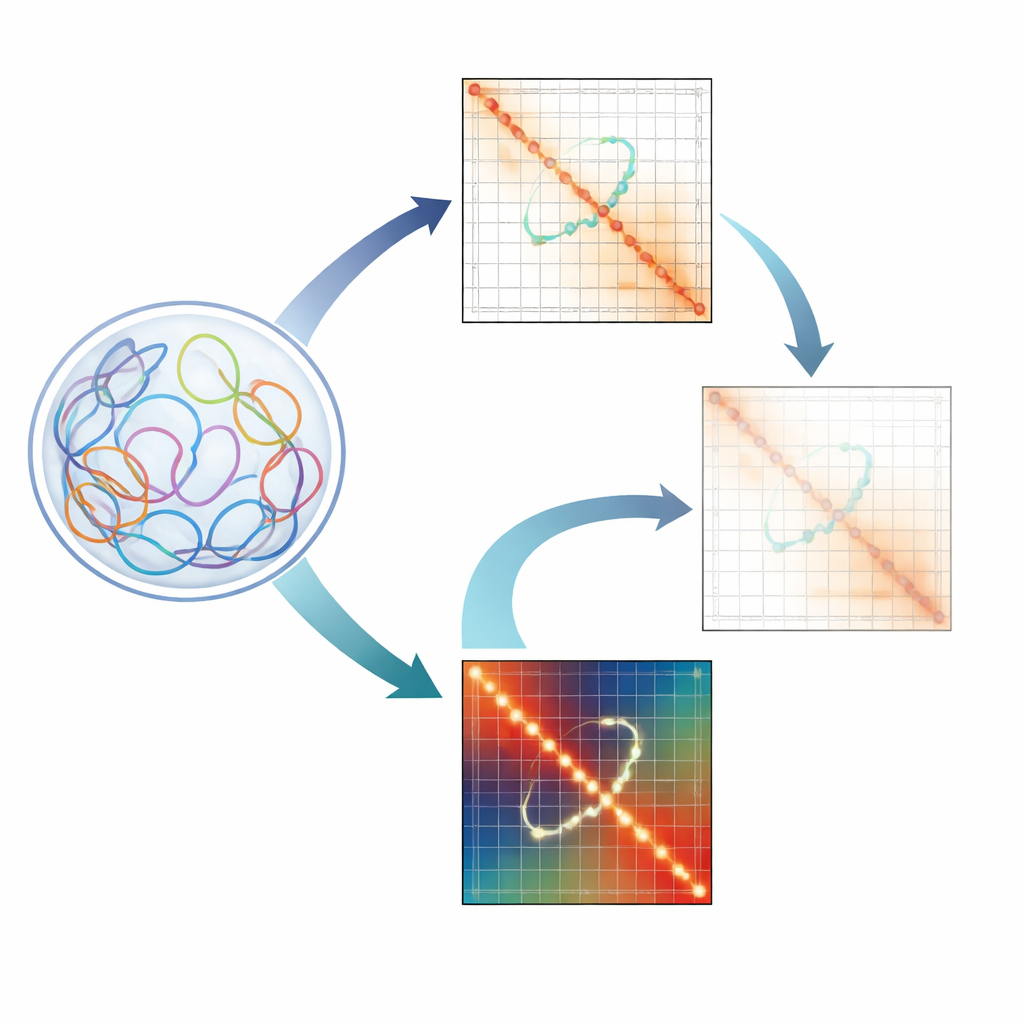
Por Que Pequenos Laços de DNA Importam
Nossos genomas não estão organizados como cordas retas de letras. Em vez disso, eles se amontoam em uma estrutura 3D complexa dentro do núcleo. Nesse estado dobrado, regiões distantes do DNA podem se encontrar, formando laços de cromatina. Alguns laços atuam como andaimes que ajudam a organizar bairros inteiros do genoma. Outros são laços regulatórios que conectam promotores de genes a potenciadores distantes que aumentam sua atividade. A interrupção desses laços regulatórios tem sido associada a distúrbios do desenvolvimento e a cânceres, portanto os cientistas estão ansiosos para mapeá-los em detalhe.
O Desafio de Ler Mapas 3D do Genoma
Técnicas como Hi-C e métodos relacionados capturam milhões a bilhões de contatos DNA–DNA e os resumem como mapas de calor, onde cada pixel reflete com que frequência duas regiões do genoma se encontram. No entanto, esses mapas estão carregados de peculiaridades técnicas: algumas regiões são mais fáceis de ler do que outras por causa da composição da sequência, de quão bem podem ser alinhadas ou de como são cortadas no experimento. Para limpar esses artefatos, pesquisadores usam métodos de normalização como ICE e KR que equilibram os mapas para que cada região aparente ter visibilidade igual. Embora essas ferramentas realcem características grandes, como domínios amplos e fortes laços estruturais, os autores mostram que elas, involuntariamente, atenuam os laços potenciador–promotor mais fracos, porém biologicamente cruciais.
Uma Nova Maneira de Limpar o Sinal
Raichu adota uma abordagem diferente para limpar os dados de contato da cromatina. Em vez de forçar cada região do genoma a parecer igualmente visível, ele modela cada interação como a soma de três componentes: uma queda geral na frequência de contatos com o aumento da distância ao longo do cromossomo, um viés específico de cada local e um sinal remanescente específico daquele contato particular. Usando um algoritmo de otimização, Raichu estima o padrão de viés que melhor explica os dados observados mantendo fixa a tendência global dependente da distância. Os contatos são então ajustados dividindo-se por esses valores de viés. Isso preserva a decadência global natural das interações enquanto corrige seletivamente distorções técnicas, deixando sinais mais claros de contatos específicos reais no DNA.
Revelando Milhares de Laços Regulatórios Perdidos
Quando os autores aplicaram Raichu a conjuntos de dados humanos e de camundongo profundamente sequenciados, o método revelou quase o dobro de laços de cromatina em comparação com os métodos padrão, ao mesmo tempo em que recuperou quase todos os laços conhecidos previamente. Os laços adicionais detectados por Raichu apresentaram forte enriquecimento por marcas bioquímicas de potenciadores e promotores ativos e por ligação de fatores de transcrição que controlam a atividade gênica. Muitos desses laços foram apoiados independentemente por outras tecnologias 3D do genoma e até por imagem de alta resolução, confirmando que refletem proximidade física real no núcleo. Importante, Raichu manteve essa vantagem mesmo quando os dados foram rarefeitos para simular profundidades de sequenciamento mais baixas, ao estudar métodos de mapeamento especializados como Micro-C e captura regional Micro-C, e até ao agrupar pequenos números de células únicas.
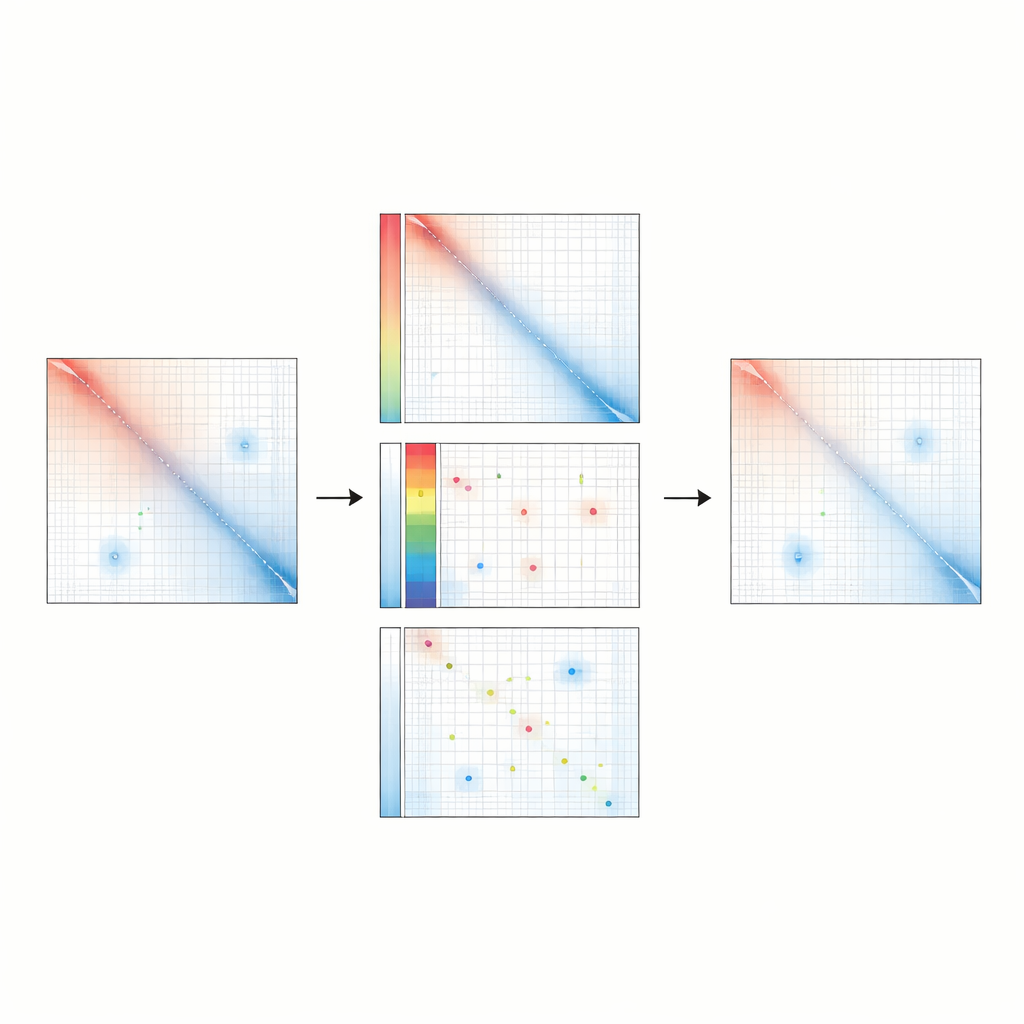
Revelando Mudanças Sutis e Padrões Evolutivos
Porque o Raichu é especialmente sensível a laços regulatórios, ele é melhor em detectar diferenças significativas entre condições que de outra forma poderiam parecer semelhantes. Em um modelo celular humano engenheirado que carrega uma variante de risco para leucemia, Raichu revelou novos laços que surgiram apenas no estado de risco, conectando genes-chave aos seus potenciadores e alinhando-se com mudanças na atividade gênica. Entre progenitores neurais de camundongo e humano, Raichu detectou milhares de laços potenciador–promotor conservados entre as espécies e que frequentemente conectavam potenciadores distantes a genes envolvidos no desenvolvimento cerebral. Esses achados sugerem que muitos contatos regulatórios importantes estavam escondidos à vista de todos, mascarados por abordagens de normalização anteriores.
O Que Isso Significa para Pesquisas Genômicas Futuras
Para um leitor leigo, a mensagem-chave é que a forma como processamos grandes conjuntos de dados genômicos pode influenciar dramaticamente a biologia que observamos. Ao repensar a etapa de limpeza dos mapas 3D do genoma, o Raichu restaura sinais fracos, porém importantes, que ligam interruptores gênicos aos seus alvos. Isso facilita rastrear como a dobra do DNA controla a atividade gênica na saúde e na doença, desde células isoladas até tecidos inteiros e entre espécies. À medida que mais estudos adotarem o Raichu, os pesquisadores podem esperar mapas mais ricos da comunicação potenciador–promotor e uma imagem mais clara de como mudanças na arquitetura do genoma contribuem para o desenvolvimento, o câncer e outras condições complexas.
Citação: Wang, X., Shi, D., Xue, F. et al. Boosting the detection of enhancer-promoter loops via normalization methods for chromatin interaction data. Nat Commun 17, 2299 (2026). https://doi.org/10.1038/s41467-026-69082-z
Palavras-chave: Organização 3D do genoma, loops potenciador-promotor, Análise de dados Hi-C, normalização da cromatina, regulação gênica