Clear Sky Science · pt
Uma estratégia sintética combinatória para desenvolver agentes de entrega de proteínas de edição genômica direcionados à retina de camundongos
Nova esperança para tratar a cegueira hereditária
Muitas formas de cegueira hereditária começam com um único gene defeituoso nas células fotossensíveis na parte posterior do olho. Ferramentas modernas de edição genética, como o CRISPR, podem, em princípio, corrigir esses erros, mas levar a maquinaria de edição de forma segura até as células certas tem sido um grande obstáculo. Este estudo descreve uma nova forma de transportar poderosos editores gênicos diretamente para a retina de camundongos usando partículas especialmente projetadas semelhantes a gorduras, levantando a perspectiva de tratamentos de dose única que restaurariam a visão em pessoas com doenças oculares genéticas.
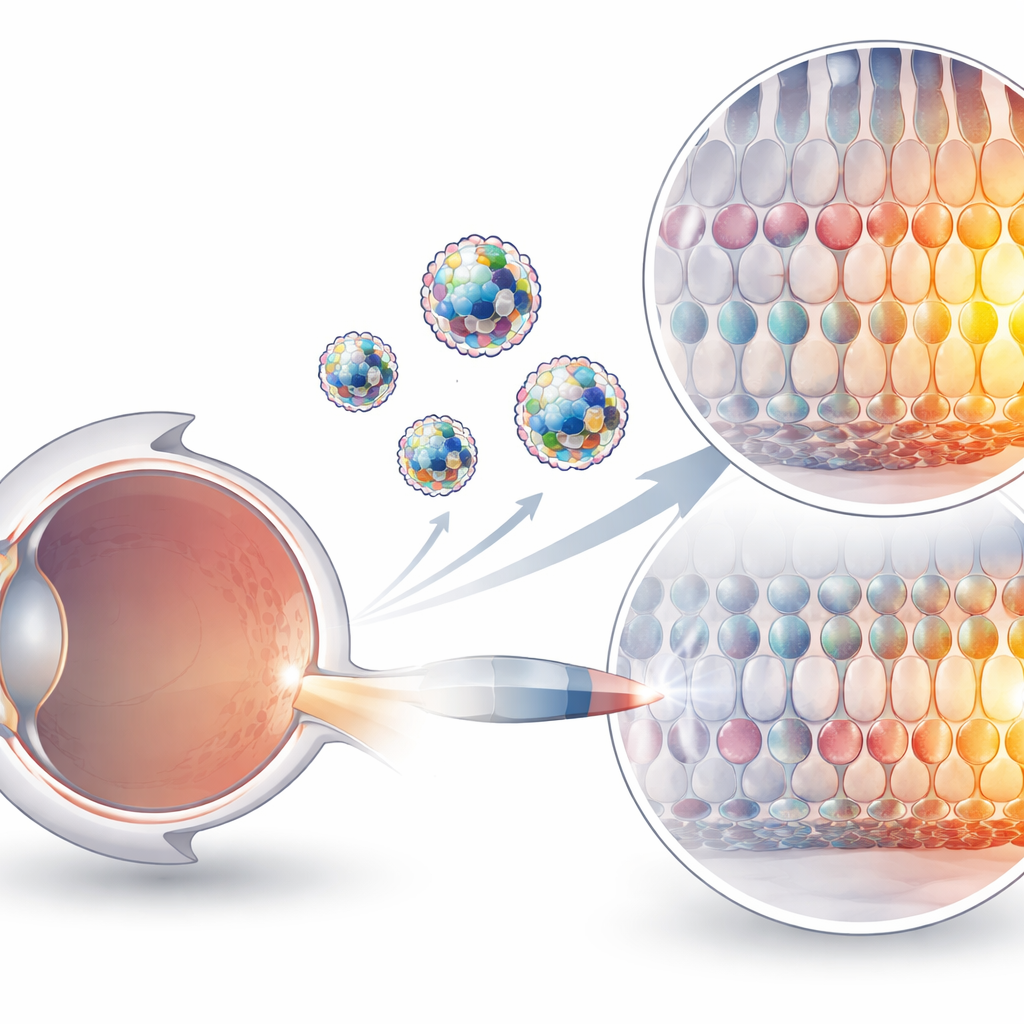
Por que é tão difícil entregar editores gênicos
Ferramentas baseadas em CRISPR agora podem mudar letras individuais do DNA sem cortar as duas fitas, um avanço que as torna atraentes para tratar desordens genéticas. Mas essas ferramentas são complexas máquinas proteína–RNA, eletricamente carregadas e frágeis no organismo. Métodos de entrega atuais dependem em grande parte de vírus modificados ou de partículas que carregam os planos genéticos para o editor em vez do próprio editor. Vírus podem provocar reações imunes e têm limites estritos de tamanho, enquanto entregar RNA mensageiro funciona muito bem no fígado, mas permanece ineficiente em muitos outros tecidos, incluindo o olho. Injetar diretamente os complexos proteína–RNA pré-montados é conceitualmente mais limpo e seguro, porém eles carecem de um veículo adequado para ajudá-los a atravessar membranas celulares e alcançar seus alvos.
Um transportador inspirado em corante para proteínas
Os pesquisadores recorreram a um ponto de partida inesperado: Coomassie Brilliant Blue, um corante azul-escuro comumente usado em laboratórios de biologia e já aprovado para certas cirurgias oculares. Esse corante adere fortemente a muitas proteínas diferentes. A equipe ligou quimicamente “cabeças” de Coomassie a “caudas” semelhantes a gorduras para criar uma família de novas moléculas chamadas lipidoides. Em água, esses lipidoides tendem a se agrupar em partículas, com as partes oleosas enterradas no interior e os grupos de Coomassie expostos externamente, onde podem se agarrar às proteínas. Ao variar o comprimento, o ramificação e a carga das caudas, os cientistas construíram dezenas de compostos candidatos projetados para se ligar a proteínas de edição gênica de um lado e interagir com membranas celulares do outro.
Testando a entrega de proteínas para células oculares
Para ver quais desenhos realmente funcionavam, o grupo primeiro usou uma proteína teste simples chamada Cre recombinase, que inverte um interruptor genético de fluorescência de verde para vermelho ou de vermelho para verde em células e camundongos transgênicos. Vários lipidoides de Coomassie transportaram Cre de forma eficiente para células cultivadas, convertendo grandes frações das células de verde para vermelho. Quando injetados sob a retina de camundongos repórteres, compostos selecionados desencadearam mudanças de cor impressionantes tanto na camada de pigmento que sustenta a visão quanto nos fotorreceptores sensíveis à luz, mostrando que as proteínas alcançaram justamente as células mais afetadas em muitas doenças que causam cegueira. Esses experimentos iniciais também revelaram que mudanças sutis na estrutura do lipidoide poderiam alterar quais tipos celulares eram alvo, sugerindo que versões futuras podem ser ajustadas para camadas retinianas específicas.
Potencializando a edição gênica e resgatando a visão
Em seguida, a equipe carregou seu sistema com um editor de base de adenina, uma variante refinada do CRISPR que pode corrigir a mutação de uma única letra que causa perda de visão em camundongos rd12, um modelo de cegueira infantil severa. Por si só, o complexo proteína–RNA do editor penetrava mal nas células. Um lipidoide, apelidado de CBB11, melhorou a entrega, mas tendia a formar aglomerados em solução. Para estabilizá-lo, os pesquisadores incorporaram o CBB11 em lipossomos pequenos e bem definidos — esferas ocas feitas de vários tipos de lipídios, incluindo componentes usados clinicamente em vacinas de mRNA. Nessas formulações, o CBB11 na superfície do lipossomo agarrava a parte proteica do editor, enquanto outros lipídios ajudavam a ligar o RNA guia, criando uma concha cooperativa que mantinha todo o complexo na superfície da partícula.
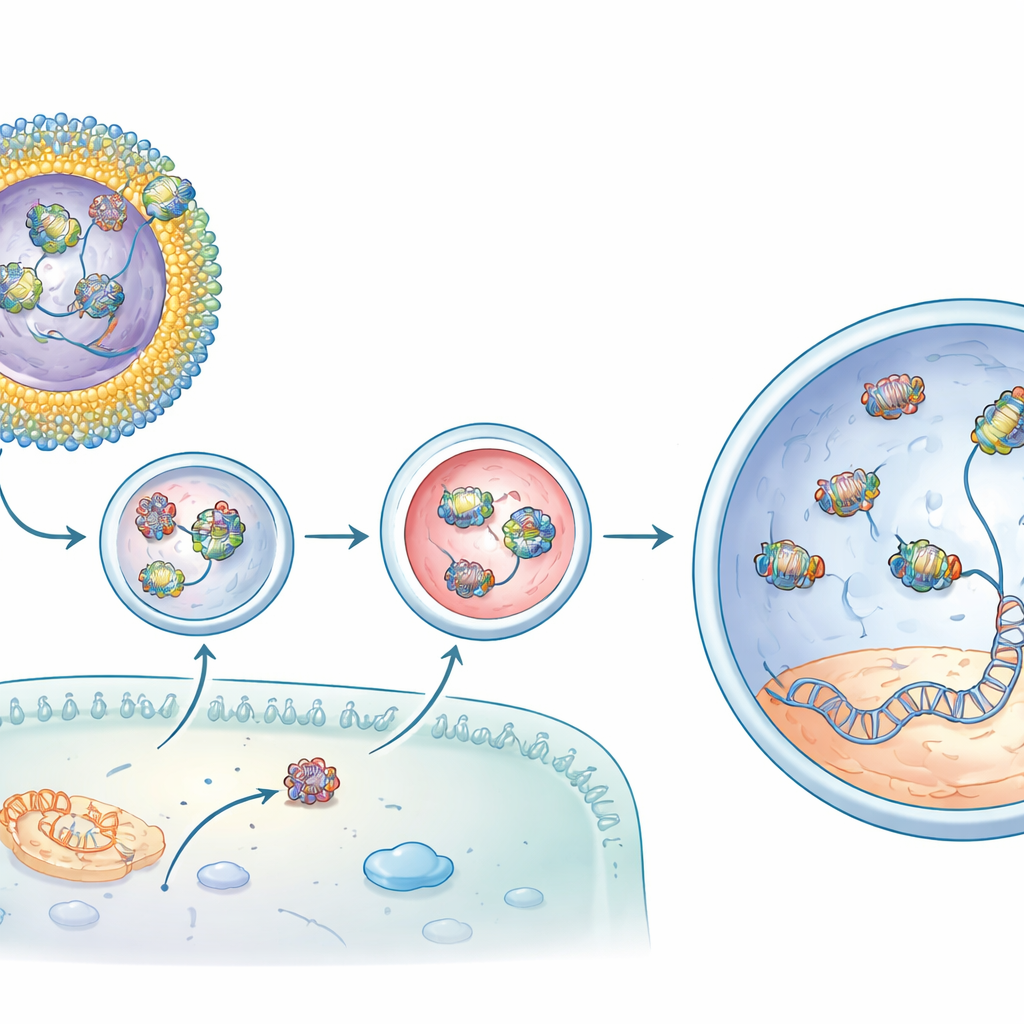
Da reparação molecular à restauração das respostas à luz
Quando esses lipossomos contendo CBB11 e carregados com o editor de base foram injetados sob a retina de camundongos rd12, os resultados foram impressionantes. Em comparação com o editor injetado isoladamente, a formulação otimizada aumentou a correção desejada do DNA no gene alvo em mais de uma ordem de magnitude e produziu níveis ainda mais altos de RNA mensageiro corrigido. Análises químicas mostraram a recuperação do pigmento retiniano sensível à luz que está ausente na doença. Mais convincente, registros elétricos dos olhos dos animais revelaram que suas células bastonetes recuperaram grande parte da capacidade de responder à luz fraca — até cerca de três quartos do sinal de um camundongo normal nos melhores casos. Alterações fora do alvo em outras partes do genoma estavam em níveis de fundo, sugerindo que a edição foi tanto potente quanto precisa.
O que isso pode significar para futuras terapias oculares
Para um não especialista, a mensagem principal é que os autores construíram um “ônibus de transporte” reutilizável para proteínas de edição gênica que funciona diretamente no olho vivo. Ao decorar partículas seguras, semelhantes às de vacinas, com um corante que prende proteínas, eles criaram um sistema capaz de capturar diferentes editores em sua superfície, entregá-los em células retinianas, corrigir mutações causadoras de doenças e restaurar a visão de forma mensurável em camundongos após um único tratamento. Embora sejam necessários mais estudos para avaliar plenamente a segurança, melhorar o direcionamento e adaptar o método para uso humano, essa plataforma aponta para medicamentos de precisão de dose única no futuro para doenças retinianas hereditárias e possivelmente outras condições genéticas em que reparos localizados do DNA possam fazer a diferença entre cegueira e visão.
Citação: Zhang, J., Hołubowicz, R., Smidak, R. et al. A combinatorial synthetic strategy for developing genome-editing protein-delivery agents targeting mouse retina. Nat Commun 17, 2479 (2026). https://doi.org/10.1038/s41467-026-69077-w
Palavras-chave: terapia gênica retiniana, edição de bases CRISPR, lipossomos, entrega de proteínas, cegueira hereditária