Clear Sky Science · pt
Percepções sobre a estrutura e a modulação do TWIK-2 humano
Por que esse minúsculo portão em nossas células importa
Nas profundezas de nossas células, portões microscópicos feitos de proteína controlam o fluxo de átomos carregados, determinando como os nervos disparam, como os vasos sanguíneos se contraem e como nosso sistema imunológico reage. Um desses portões, chamado TWIK-2, foi associado à hipertensão pulmonar e à inflamação nociva, mas até agora os cientistas sabiam muito pouco sobre sua construção ou como controlá‑lo com medicamentos. Este estudo revela a estrutura detalhada do TWIK-2 humano, mostra seu comportamento elétrico e descreve como ele poderia ser alvo para desenvolver novos fármacos anti‑inflamatórios.
Um canal discreto com grandes implicações para a saúde
O TWIK-2 pertence a uma grande família de canais de potássio do tipo “vazamento” que ajudam a definir a voltagem de repouso das células permitindo que íons de potássio atravessem a membrana celular. Enquanto outros membros dessa família, como os canais TREK e TASK, foram amplamente estudados e associados à dor e ao humor, o TWIK-2 permaneceu obscuro porque é difícil de registrar e se expressa mal em sistemas laboratoriais padrão. Ainda assim, estudos em animais e células ligaram o TWIK-2 à hipertensão pulmonar, lesão pulmonar aguda, perda auditiva e ativação de um complexo imune chamado inflamassoma NLRP3, que dirige inflamação danosa em sepse e outras doenças. Entender como o TWIK-2 funciona é, portanto, essencial tanto para a biologia básica quanto para o desenho de terapias direcionadas.
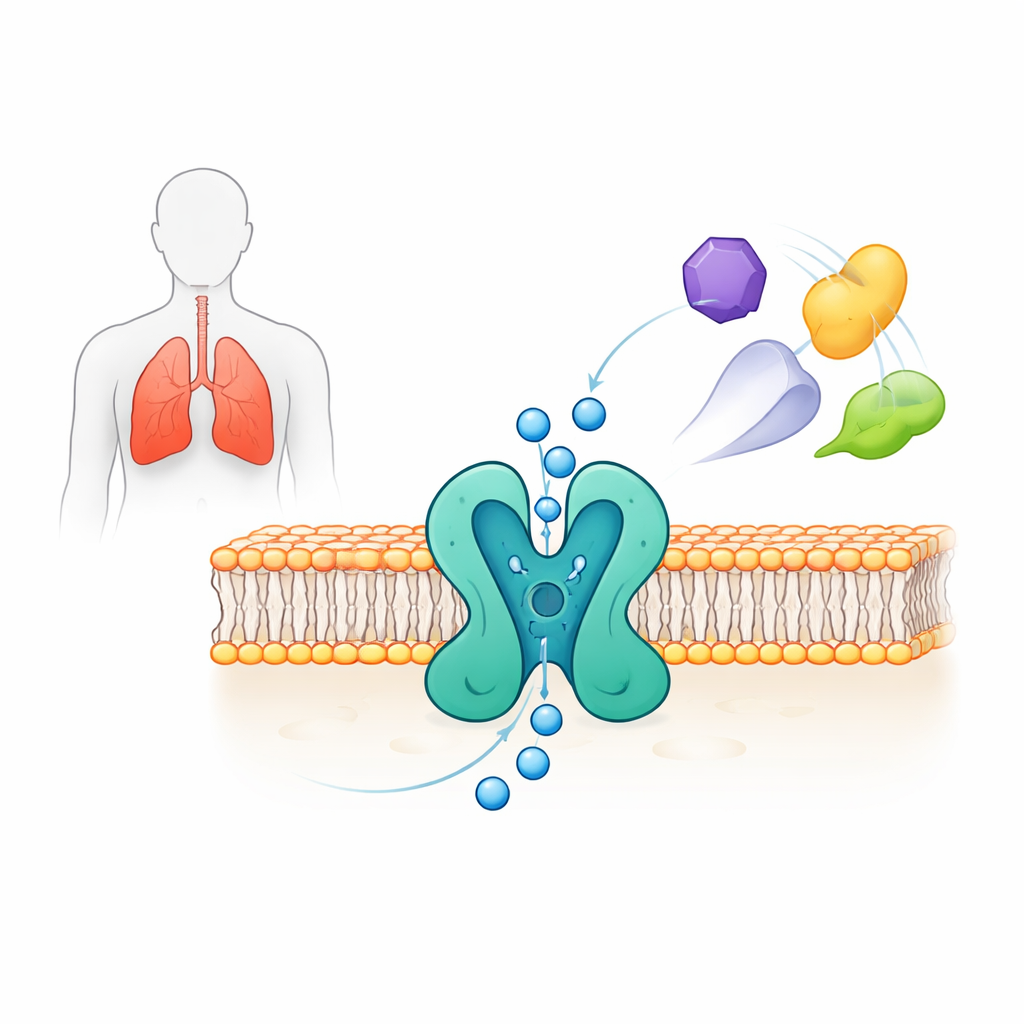
Vendo o portão em detalhe atômico
Os pesquisadores expressaram o TWIK-2 humano de comprimento total em linhas celulares humanas e usaram crio‑microscopia eletrônica de partícula única para determinar sua estrutura tridimensional com resolução de cerca de 3,7 angstroms. O canal forma um conjunto em duas partes que, juntas, criam um poro central pelo qual os íons de potássio passam. Cada metade contém quatro segmentos de transmembrana e dois “hélices de poro” que moldam uma região estreita chamada filtro de seletividade, onde o potássio é distinguido de outros íons. Acima do poro, duas estruturas arqueadas em forma de “tampa” criam dois caminhos de entrada separados para íons vindos do exterior da célula. A estrutura também revela assimetrias sutis entre os dois lados do poro que conferem ao TWIK-2 um arranjo pseudo‑quádruplo — uma marca dessa família de canais.
Lípidos ocultos e uma via iônica finamente ajustada
Ao longo do caminho de condução iônica, a equipe mapeou como os íons de potássio se movem do interior da célula, através de um “punho” hidrofóbico, pelo filtro de seletividade e para fora, sob a tampa. O ponto mais estreito ainda é largo o bastante para que o potássio viaje em fila indiana. Embora a proteína tenha sido purificada sem lipídios adicionados, os mapas de crio‑EM mostraram densidades em forma de tubo aninhadas perto da parte inferior do poro e em bolsos laterais entre hélices. Esses sinais provavelmente representam lipídios ou caudas de detergente que aderiram ao TWIK-2 durante a purificação, sugerindo que gorduras naturais da membrana podem alojar‑se nessas fendas e alterar sutilmente a forma das hélices próximas. Tais deslocamentos, especialmente em uma hélice chamada M4 e nas alças do filtro de seletividade, acredita‑se que ajustem se o canal está aberto, fechado ou em um estado intermediário.
Explorando o portão com mutações e bloqueadores
Para conectar estrutura e função, os cientistas usaram um sistema automatizado de patch‑clamp para medir correntes de células que expressavam TWIK-2 normal ou versões com aminoácidos específicos alterados. Eles descobriram que o TWIK-2 é fortemente dependente de voltagem mas, ao contrário de seu parente TWIK-1, em grande parte insensível a mudanças na acidez externa. Mutações em duas treoninas conservadas na base do filtro de seletividade fizeram o canal abrir mais rapidamente e conduzir mais corrente, sugerindo que esses sítios atuam como dobradiças-chave que estabilizam o estado fechado. Alterações na entrada e na saída do poro modificaram a rapidez com que o canal ligava e desligava, revelando quão controlado é o caminho iônico. A equipe então testou quatro pequenas moléculas conhecidas por modular canais relacionados. Duas delas, ML365 e NPBA, bloquearam potently o TWIK-2, enquanto as outras não tiveram efeito. Ao comparar como várias mutações alteraram a sensibilidade aos fármacos, os autores inferem que esses compostos provavelmente se ligam logo abaixo do filtro de seletividade e em cavidades próximas, e que diferentes drogas usam modos de ligação sobrepostos porém distintos.
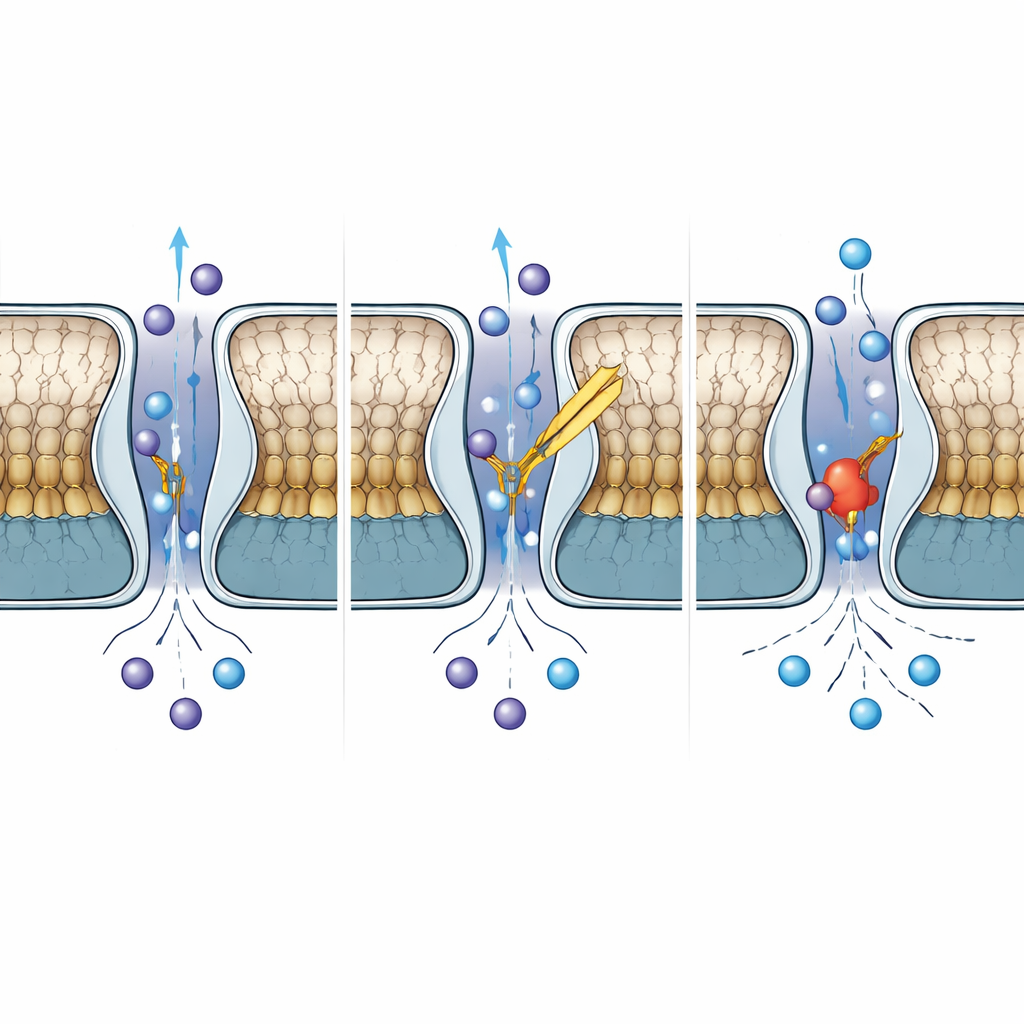
Como o TWIK-2 difere de seus parentes próximos
Embora o TWIK-2 compartilhe mais da metade de sua sequência com o TWIK-1, seus comportamentos divergem de maneiras importantes. Quando os autores compararam o TWIK-2 com estruturas publicadas do TWIK-1 em pH neutro e ácido, descobriram que a região da tampa do TWIK-2 se assemelha à forma inibida por ácido do TWIK-1, mas seu filtro de seletividade permanece disposto como a forma condutora, aberta. Uma única histidina no TWIK-1, conhecida por detectar prótons e se projetar para o poro para bloquear o fluxo iônico em pH baixo, é substituída por uma tirosina no TWIK-2. Mesmo quando a equipe reintroduziu uma histidina nessa posição no TWIK-2, o canal não se tornou sensível ao pH, mostrando que o controle por pH nesses canais depende de uma rede mais ampla de resíduos e movimentos, e não apenas de um aminoácido “interruptor”.
Da estrutura para terapias futuras
Tomado em conjunto, este trabalho fornece a primeira imagem em alta resolução do TWIK-2 humano e mapeia como características estruturais específicas moldam seu fluxo iônico, resposta à voltagem e suscetibilidade a bloqueadores de pequena molécula. A descoberta de que compostos existentes podem inibir seletivamente o TWIK-2, combinada a uma plataforma automatizada robusta de triagem, abre a porta para buscas em grande escala por drogas mais seguras e potentes. Como a atividade do TWIK-2 em células imunes foi ligada a inflamação descontrolada, especialmente nos pulmões, esses fármacos poderiam formar a base de novos tratamentos anti‑inflamatórios que atuem reduzindo com sutileza este minúsculo porém poderoso portão na membrana celular.
Citação: Ma, Q., Hernandez, C.C., Navratna, V. et al. Insights into the structure and modulation of human TWIK-2. Nat Commun 17, 2201 (2026). https://doi.org/10.1038/s41467-026-69072-1
Palavras-chave: canal de potássio TWIK-2, canais K2P de dois poros, estrutura de canal iônico por crio‑EM, moduladores de canais de potássio, inflamação pulmonar