Clear Sky Science · pt
Proteômica espacial unicelular do cólon e modelos murinos ligam disfunção mitocondrial à deficiência de plasmócitos secretantes de IgA dimérica na doença de Crohn
Por que os anticorpos intestinais importam na doença de Crohn
A doença de Crohn é mais conhecida por crises dolorosas de inflamação intestinal, mas muito antes dos sintomas dispararem, mudanças sutis podem ocorrer na forma como o sistema imunológico protege o intestino. Este estudo faz uma pergunta simples, mas importante: pessoas com doença de Crohn em remissão ainda produzem o tipo certo de anticorpos para manter os micróbios intestinais sob controle pacífico? Ao combinar amostras de pacientes, perfilamento tecidual de alta resolução, análises metabólicas e modelos murinos, os autores revelam uma fraqueza oculta no escudo de anticorpos do intestino que está ligada à produção de energia celular.
Um revestimento protetor que fica aquém do necessário
Nossos intestinos dependem de um anticorpo especial chamado IgA secretora, liberado no muco que reveste o intestino. A IgA, especialmente em sua forma “dupla”, chamada IgA dimérica, reveste bactérias e outros micróbios, ajudando a mantê‑los na superfície em vez de profundamente no tecido. Neste trabalho, os pesquisadores examinaram biópsias do cólon, sangue e fezes de pessoas com doença de Crohn em remissão e de controles não inflamados. No tecido do cólon, pacientes com Crohn apresentaram, na verdade, mais células B e células produtoras de anticorpos e níveis mais altos de genes e proteínas relacionados à IgA. Ainda assim, quando a equipe mediu IgA nas fezes, encontrou o oposto do que se poderia esperar: a IgA secretora no lúmen intestinal estava significativamente reduzida. 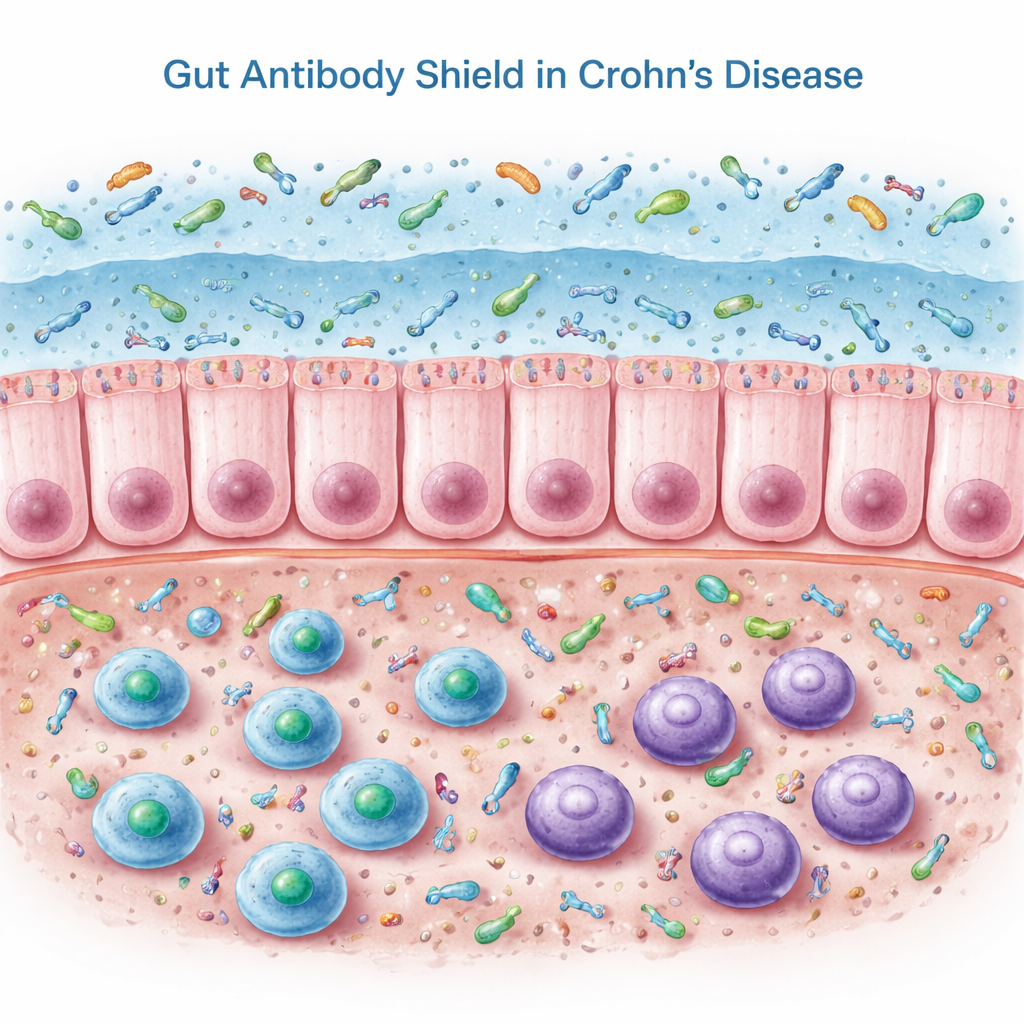
Presa no meio do caminho: células produtoras de anticorpos que não amadurecem completamente
As células que secretam IgA — plasmócitos — normalmente amadurecem por estágios definidos, de precursores ativos e de curta duração até especialistas de longa vida que produzem grandes quantidades de IgA dimérica. Usando proteômica espacial unicelular, que mapeia muitos proteínas em células individuais dentro do tecido intacto, os autores puderam distinguir subconjuntos de plasmócitos imaturos e totalmente maduros no cólon. Em pacientes com Crohn, plasmablastos precoces e plasmócitos imaturos estavam expandidos, enquanto os plasmócitos mais maduros estavam reduzidos. Análises bioquímicas confirmaram que a razão entre IgA dimérica e monomérica era menor nos cólons de Crohn, e cada célula produtora de anticorpos secretava, em média, menos IgA dimérica. Quando a equipe isolou células B de memória recomutadas do cólon e as induziu a se tornarem plasmócitos em cultura, células de pacientes com Crohn não conseguiram aumentar marcadores chave de maturação e produziram menos IgA total e dimérica, embora a produção de IgG tenha permanecido amplamente normal. Isso sugere um bloqueio intrínseco no programa de maturação especificamente para plasmócitos secretantes de IgA.
Fábricas de energia sob pressão
Para entender o que impulsiona esse bloqueio, os pesquisadores voltaram sua atenção ao metabolismo celular. Eles descobriram que plasmócitos no tecido de Crohn expressavam níveis mais altos de CD38, uma enzima na superfície celular que consome NAD+, um combustível central para a produção de energia mitocondrial. Genes envolvidos na fosforilação oxidativa mitocondrial — a principal via pela qual as células geram ATP a partir de nutrientes — foram amplamente regulados para baixo no tecido colônico de pacientes com Crohn, e os padrões de metabólitos plasmáticos foram compatíveis com uma mudança afastada da respiração mitocondrial eficiente. Em experimentos ex vivo, plasmócitos derivados de Crohn consumiram pouco glicose, liberaram menos lactato e mostraram expressão reduzida de genes de energia mitocondrial, indicando um estado metabolicamente “quiescente” ou enfraquecido. 
Pistas de modelos murinos e da dieta
Modelos murinos forneceram suporte adicional. Camundongos com uma mutação mitocondrial definida que prejudica o complexo V, a enzima produtora de ATP, apresentaram menos plasmócitos maduros em tecidos linfoides associados ao intestino, expressão reduzida de marcadores de plasmócitos no cólon e níveis mais baixos de IgA monomérica e dimérica no tecido colônico. Por outro lado, camundongos saudáveis alimentados com uma dieta sem glicose e rica em proteínas — que aumenta a atividade mitocondrial no cólon — desenvolveram mais células produtoras de IgA e maior IgA fecal. Esses experimentos complementares ligam diretamente o desempenho mitocondrial à capacidade dos plasmócitos de amadurecer e manter uma barreira robusta de IgA no intestino.
O que isso significa para pessoas com doença de Crohn
De forma geral, o estudo desenha um quadro em que a doença de Crohn, mesmo durante a remissão clínica, está associada a uma superabundância de células da linhagem B imaturas no cólon e a uma escassez de plasmócitos totalmente maduros, energeticamente exigentes, que secretam IgA dimérica no muco. O intestino pode parecer calmo, mas seu escudo de anticorpos é mais fino e menos eficaz. Ao vincular esse defeito à disfunção mitocondrial — possivelmente impulsionada em parte pela atividade aumentada de CD38 — o trabalho sugere que terapias destinadas a restaurar o metabolismo energético celular ou a ajustar a sinalização de CD38 poderiam ajudar a reconstruir a barreira mucosal de IgA. Para os pacientes, isso levanta a possibilidade de que tratamentos futuros não apenas suprimam a inflamação quando ela aparecer, mas também fortaleçam as defesas anticorpos de primeira linha do intestino para evitar que crises surjam desde o início.
Citação: Raschdorf, A., de Almeida, L.N., Solbach, P. et al. Colonic spatial single-cell proteomics and murine models link mitochondrial dysfunction to dimeric IgA-secreting plasma cell deficiency in Crohn’s disease. Nat Commun 17, 1590 (2026). https://doi.org/10.1038/s41467-026-69069-w
Palavras-chave: Doença de Crohn, anticorpos intestinais, IgA, mitocôndrias, imunidade intestinal