Clear Sky Science · pt
FidlTrack: rastreamento de partículas únicas com consciência estrutural e alta fidelidade resolve o movimento molecular intracelular em organelas que monitoram o processamento da APP
Observando moléculas individuais dentro de células vivas
Dentro de cada célula, inúmeras moléculas estão constantemente em movimento, colidindo, ligando-se e separando-se. Microscópios modernos podem seguir moléculas uma a uma, prometendo uma visão detalhada de como a vida funciona em suas menores escalas. Mas quando muitas moléculas se movem rapidamente em espaços estreitos e sinuosos, como o retículo endoplasmático ou mitocôndrias, suas trajetórias se emaranham e ficam fáceis de interpretar de forma errada. Este artigo apresenta o FidlTrack, uma nova abordagem para desfazer esse emaranhado para que os pesquisadores possam confiar no que observam ao rastrear moléculas únicas em tempo real.
Por que rastrear movimentos minúsculos é tão difícil
O rastreamento de partículas únicas funciona acompanhando o mesmo ponto brilhante ao longo de muitos quadros de um filme. Em uma superfície celular relativamente plana, onde moléculas se movem devagar e estão separadas, isso é administrável. No interior da célula, porém, as moléculas difundem muito mais rápido e se aglomeram em tubos e lâminas estreitos e curvos. Entre quadros, o mesmo ponto pode ter se deslocado uma longa distância, e vários pontos idênticos podem estar ao alcance. O software tradicional precisa “adivinhar” qual ponto no quadro seguinte é a mesma molécula, e essas suposições podem facilmente estar erradas. Pior, trajetórias corretas e incorretas podem parecer muito semelhantes, tornando difícil saber em quais partes dos dados é possível confiar.
Projetando experimentos para dados honestos
Os pesquisadores primeiro construíram um simulador realista que gera filmes de “verdade fundamental” de moléculas em difusão, onde os caminhos reais são conhecidos. Eles usaram esses conjuntos de dados sintéticos para testar sistematicamente como fatores-chave afetam a confiabilidade do rastreamento: quão rápido as moléculas se movem, quantas aparecem em cada imagem, com que frequência as imagens são coletadas e quão longe uma molécula pode pular entre quadros. A partir disso, criaram mapas que mostram, para cada situação, quais configurações maximizam a fração de movimentos corretamente reconstruídos. Esses mapas revelam que, para moléculas de movimento lento em densidades moderadas, o rastreamento pode ser muito confiável, mas para moléculas rápidas em altas densidades, os erros crescem rapidamente e adicionar mais moléculas deixa de aumentar a informação útil.
Identificando e cortando passos duvidosos
Em seguida, a equipe abordou uma ideia sutil, porém poderosa: ambiguidade. Um movimento é chamado de ambíguo quando mais de um possível ponto seguinte se encontra ao alcance, forçando o algoritmo a escolher entre vários vínculos plausíveis. Usando suas simulações, os autores mostraram que uma grande parcela dos erros de rastreamento surge desses passos ambíguos. Eles definiram um Escore de Ambiguidade que conta com que frequência tais situações ocorrem e então exploraram o que acontece se todos os passos ambíguos forem removidos após o rastreamento. Essa poda sacrifica alguns dados e encurta trajetórias, mas aumenta fortemente a confiabilidade geral do que permanece e melhora as estimativas da velocidade de movimento das moléculas. Aplicado a filmes reais de um marcador no retículo endoplasmático, a ambiguidade foi maior em regiões lotadas próximas ao núcleo celular, e a remoção de vínculos ambíguos limpou essas áreas sem prejudicar regiões mais simples.
Deixando a arquitetura celular guiar o rastreamento
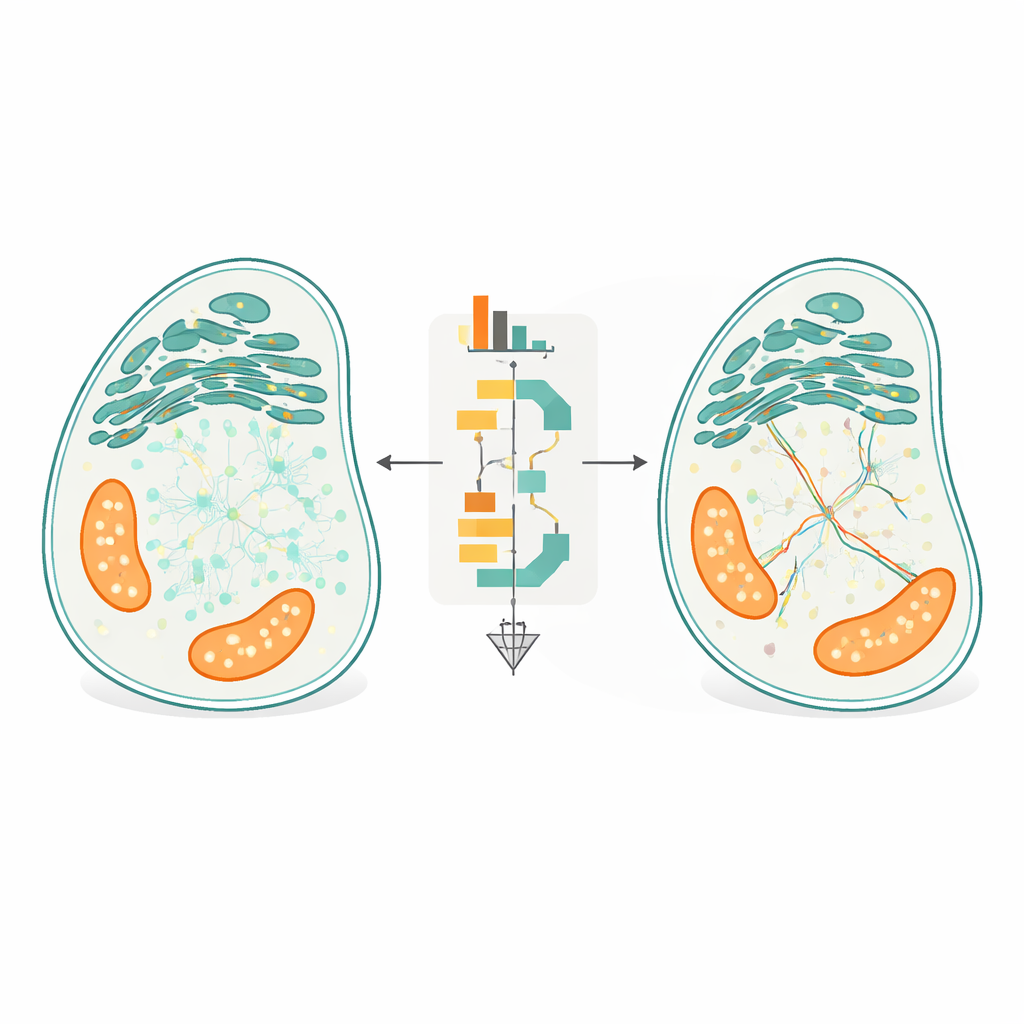
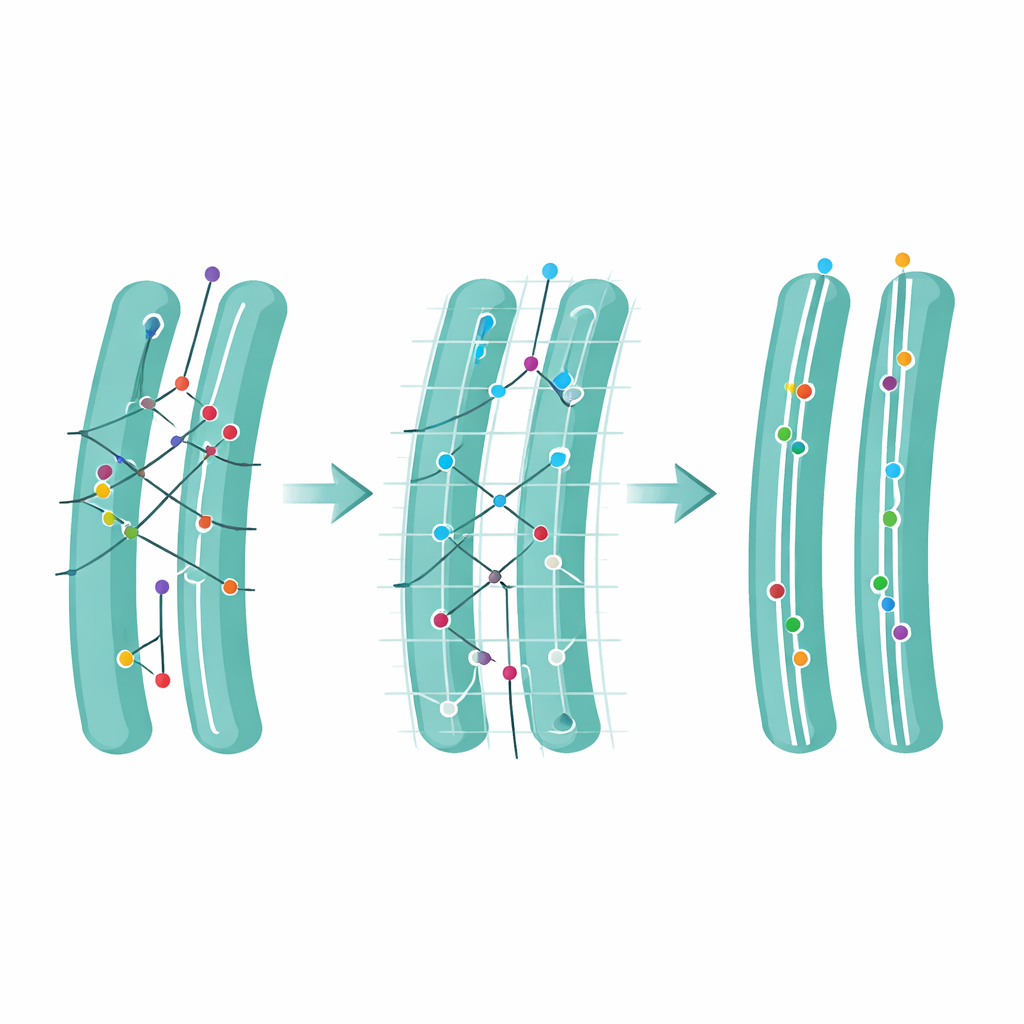
A inovação central do FidlTrack é o rastreamento “consciente da estrutura”. Em vez de tratar cada ponto como se se movesse em espaço vazio, o método usa imagens da arquitetura interna da célula — como os contornos do retículo endoplasmático, mitocôndrias ou projeções neuronais delgadas — para restringir onde as moléculas podem realisticamente viajar. A imagem da organela é convertida em um grafo de pixels conectados, e distâncias são medidas ao longo desse grafo em vez de linhas retas pelo espaço. Vínculos que exigiriam que uma molécula saltasse por um espaço entre dois túbulos separados podem assim ser sinalizados como impossíveis e rejeitados. Em simulações de tubos compactos e em filmes reais de processos neuronais e organelas, essa consciência estrutural reduziu ligações ambíguas em até metade e aumentou a quantidade de dados de movimento confiáveis e não ambíguos em várias vezes.
Revelando comportamentos celulares ocultos e eventos relevantes para doenças
Munidos dessas ferramentas — configurações otimizadas, filtragem de ambiguidade e consciência estrutural — os autores revisitaram várias questões biológicas que antes estavam fora de alcance. No retículo endoplasmático, eles conseguiram rastrear com clareza como proteínas se deslocam ao interagir com sítios de saída que canalizam cargas para o aparelho de Golgi, distinguindo “passagens rápidas” de permanências mais longas. Capturaram momentos raros em que a proteína relacionada à doença de Alzheimer, APP, é cortada pela enzima BACE1, visível como uma mudança súbita de um movimento lento, ligado à membrana, para uma difusão livre mais rápida. Também seguiram moléculas engenheiradas semelhantes a anticorpos no RE e, a partir de mudanças em seu movimento, inferiram quando estavam ligadas ao alvo versus quando derivavam livremente. Nesses casos diversos, o FidlTrack recuperou trajetórias mais confiáveis e realçou diferenças que o rastreamento padrão borrava ou subestimava.
O que isso significa para a biologia celular futura
Para não especialistas, a mensagem principal é que nem todas as trilhas de moléculas únicas são iguais: algumas são confiáveis, outras enganosas, e até agora era difícil distingui-las. O FidlTrack fornece uma forma prática e de código aberto tanto para medir quão confiável é um conjunto de dados quanto para melhorar essa confiabilidade ajustando as configurações experimentais, cortando passos ambíguos e usando a própria geometria da célula como guia. Isso torna possível observar moléculas navegando no interior intrincado da célula com maior confiança e detectar eventos raros ou sutis, desde triagem de proteínas até processamentos relevantes para doenças, que antes estavam enterrados no ruído.
Citação: Parutto, P., Yuan, Y., Davì, V. et al. FidlTrack: high-fidelity structure-aware single particle tracking resolves intracellular molecular motion in organelles sensing APP processing. Nat Commun 17, 2639 (2026). https://doi.org/10.1038/s41467-026-69067-y
Palavras-chave: rastreamento de partículas únicas, dinâmica intracelular, estrutura de organelas, movimento de proteínas, doença de Alzheimer