Clear Sky Science · pt
Tenascina C+ miofibroblastos agravam a hiperplasia neointimal vascular pela propagação das interações nervo-macrófago em camundongos
Quando os vasos sanguíneos cicatrizam do jeito errado
Procedimentos que reabrem artérias obstruídas, como angioplastia e cirurgia de bypass, salvam inúmeras vidas. Ainda assim, muitas vezes deixam um problema oculto: com o tempo, o vaso tratado pode cicatrizar para dentro, estreitando-se novamente e colocando os pacientes de volta em risco. Este estudo em camundongos revela uma conversa inesperada entre células de suporte, nervos e células do sistema imunológico na parede vascular que impulsiona esse excesso de cicatrização, e aponta para uma molécula chamada tenascina C como alvo promissor para interromper esse ciclo.
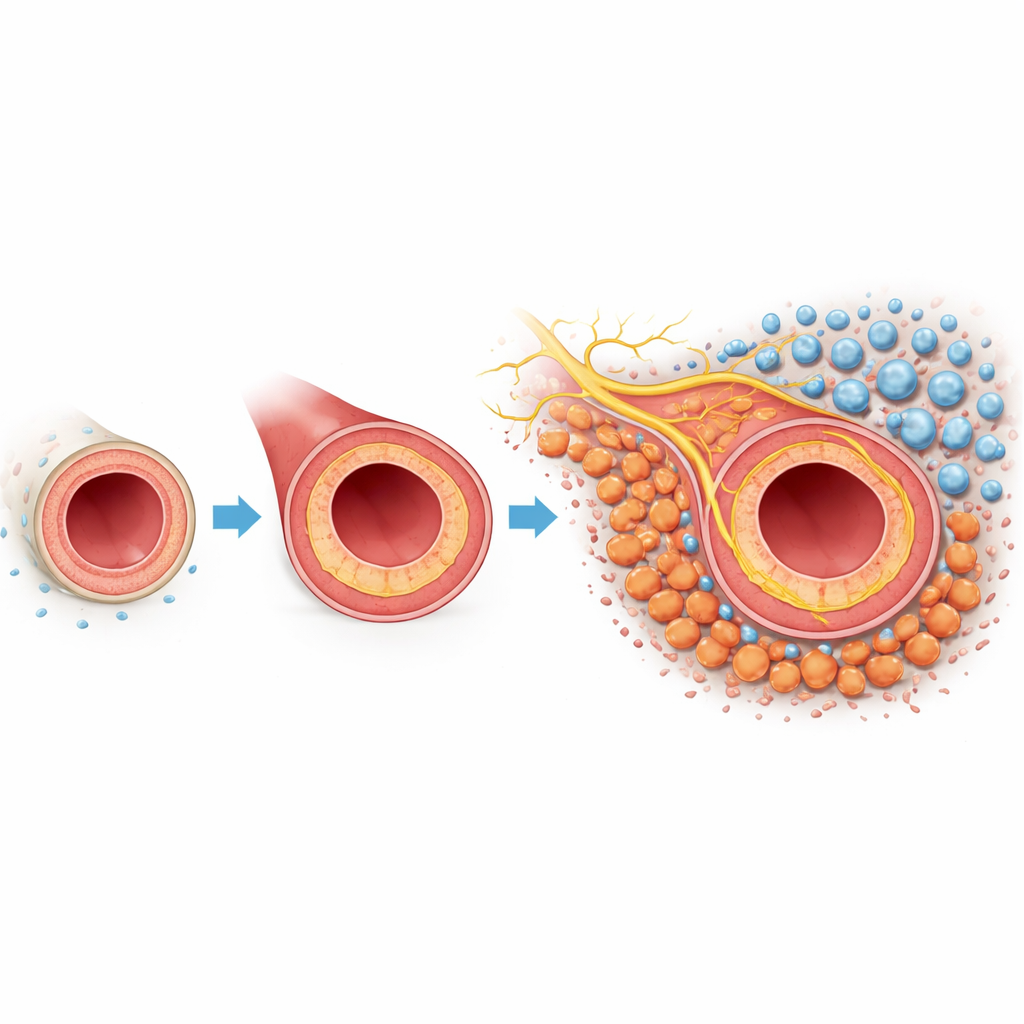
Um olhar mais atento ao problema da cicatrização nas artérias
Quando uma artéria é lesionada ou manipulada durante a cirurgia, o revestimento interno pode regenerar-se de forma excessiva. Esse crescimento para dentro, chamado hiperplasia neointimal, espessa a parede do vaso e reduz o canal por onde o sangue flui. A camada mais externa do vaso, a adventícia, contém fibroblastos—células de suporte que normalmente mantêm a estrutura do vaso. Neste modelo de camundongo, em que a artéria carótida foi parcialmente laçada para mimetizar a lesão, os pesquisadores usaram perfilagem genética de célula única e mapeamento espacial para catalogar cada tipo celular principal envolvido. Eles descobriram que os fibroblastos eram especialmente abundantes e mudaram seu comportamento dramaticamente após a lesão, sugerindo que essas células podem ser protagonistas centrais na resposta de cicatrização.
A ascensão das células formadoras de cicatriz ricas em tenascina C
Aprofundando-se na população de fibroblastos, a equipe descobriu um subconjunto distinto que apareceu apenas após a lesão. Essas células apresentavam características de miofibroblastos—altos níveis da proteína contrátil α-actina do músculo liso e outro marcador chamado periostina—indicando que haviam mudado para um modo de produção de cicatriz. Crucialmente, esse subconjunto também produzia grandes quantidades de tenascina C, uma proteína de matriz normalmente rara em tecidos adultos saudáveis, mas abundante em doenças e na reparação tecidual. Experimentos de laboratório mostraram que expor fibroblastos adventiciais normais ao fator de crescimento transformador beta ou a tenascina C adicional os impulsionava a se tornar esses miofibroblastos positivos para tenascina C. As células então secretavam ainda mais tenascina C, criando um circuito auto-reforçador através de um par específico de receptores de superfície, a integrina αvβ1, que expandia de forma sustentada a população formadora de cicatriz.
Nervos e células imunes mudam para o bairro
A história não terminou com a formação de cicatriz. Usando imagem 3D de conjunto inteiro e transcriptômica espacial, os pesquisadores observaram que os miofibroblastos ricos em tenascina C se agrupavam perto de fibras nervosas em brotamento e de células imunes chamadas macrófagos na parede externa do vaso. Artérias lesionadas mostraram nervos sensoriais densos e emaranhados e mais estruturas semelhantes a sinapses do que o normal, tanto em camundongos quanto em amostras de artérias humanas com hiperplasia neointimal. Os macrófagos nessas regiões apresentavam uma assinatura inflamatória, produzindo moléculas como IL-1β e TGF-β1 que podem alimentar ainda mais a cicatrização. Juntos, os dados desenharam um quadro de um microambiente reorganizado no qual células formadoras de cicatriz, nervos e macrófagos se entrelaçam fisicamente e influenciam uns aos outros.
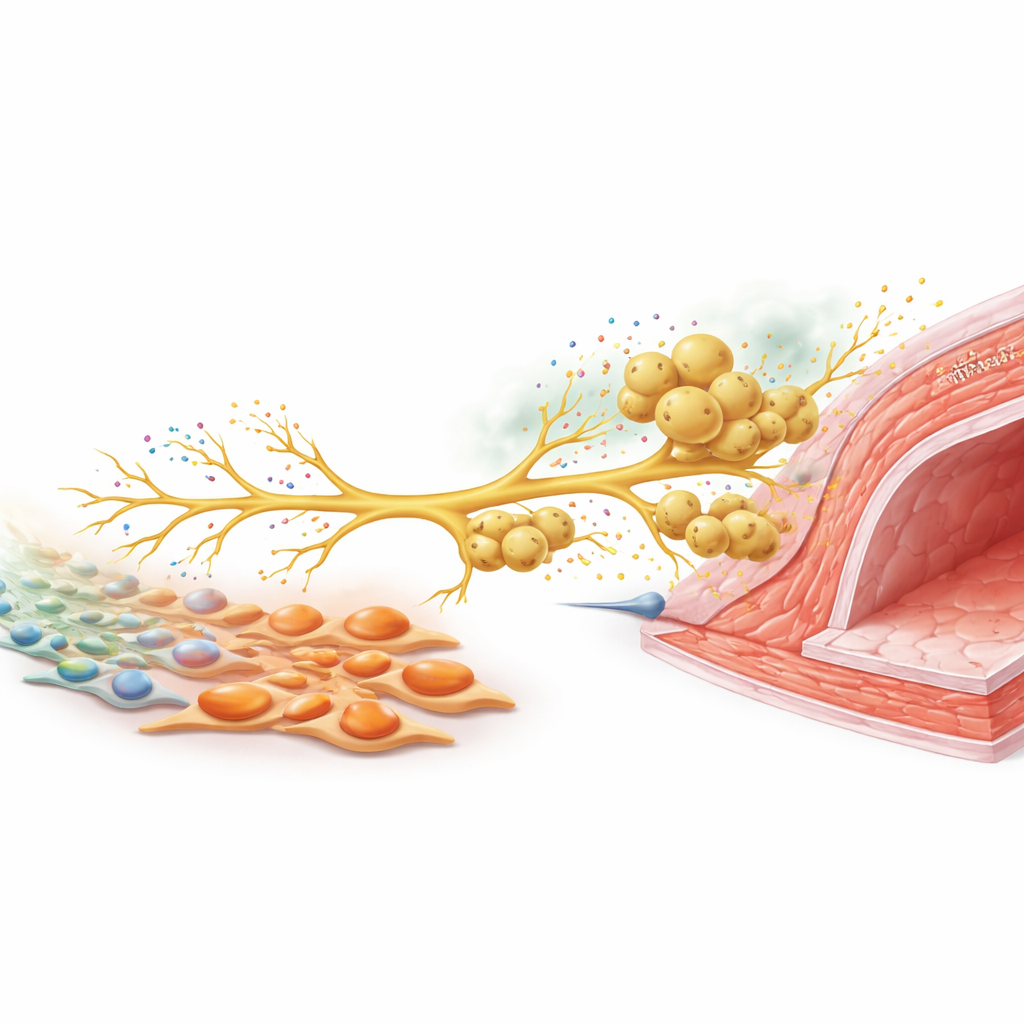
Um sinal nervoso que convoca mais defensores
Para entender como esses tipos celulares se comunicam, a equipe concentrou-se em nervos sensoriais que detectam estímulos lesivos. Em cultura, os miofibroblastos ricos em tenascina C aumentaram o crescimento de fibras nervosas a partir de neurônios dos gânglios da raiz dorsal. Em camundongos lesionados, esses neurônios sensoriais aumentaram a produção de CCL2, um sinal químico bem conhecido por atrair macrófagos. Quando neurônios e macrófagos foram cultivados juntos, os macrófagos migraram ao longo das fibras nervosas em crescimento, assim como faziam ao redor das artérias in vivo. Silenciar a CCL2 nos neurônios reduziu drasticamente o recrutamento de macrófagos. Em animais, reduzir a atividade dos nervos sensoriais com uma toxina, ou deletar seletivamente a tenascina C apenas nos fibroblastos, diminuiu tanto a densidade nervosa quanto os níveis de CCL2, o acúmulo de macrófagos e, por fim, o espessamento da parede vascular. Combinar ambas as intervenções não acrescentou benefício extra, sugerindo que atuam na mesma via.
Por que essa nova via é importante
Em conjunto, os achados revelam um círculo vicioso: a lesão faz com que fibroblastos se tornem miofibroblastos produtores de tenascina C; essas células remodelam a matriz e estimulam nervos sensoriais; nervos ativados liberam CCL2, que atrai macrófagos; e os macrófagos secretam fatores inflamatórios e fibróticos que agravam a cicatrização e estreitam a artéria. Ao identificar a tenascina C e seu eixo nervo–macrófago a jusante como motores centrais desse ciclo, o trabalho sugere que tratamentos que visem essa molécula ou seus parceiros de sinalização poderiam ajudar a manter as artérias reparadas abertas por mais tempo, oferecendo aos pacientes proteção mais duradoura após procedimentos cardiovasculares.
Citação: Tong, X., Shi, G., Fang, Z. et al. Tenascin C+ myofibroblasts exacerbate vascular neointimal hyperplasia by propagation of nerve-macrophage interactions in mice. Nat Commun 17, 2199 (2026). https://doi.org/10.1038/s41467-026-69062-3
Palavras-chave: hiperplasia neointimal, tenascina C, remodelamento vascular, nervos sensoriais, inflamação por macrófagos