Clear Sky Science · pt
Paclitaxel impulsiona a expansão de macrophages TREM2+ que explica sua eficácia terapêutica inferior em comparação ao Nab‑paclitaxel
Por que este estudo importa
Muitas mulheres com câncer de mama recebem quimioterápicos chamados taxanos, mais comumente paclitaxel ou uma versão mais recente ligada a pequenas partículas de albumina, conhecida como nab‑paclitaxel. Há muito tempo os médicos suspeitam que o medicamento mais novo frequentemente funciona melhor, mas os motivos não eram claros. Este estudo investiga dados de pacientes e experimentos em animais para mostrar que o paclitaxel convencional pode, involuntariamente, ajudar o câncer a se espalhar para os pulmões ao remodelar as células imunes do organismo, e aponta uma forma de bloquear esse efeito colateral prejudicial.
Dois medicamentos semelhantes, dois desfechos diferentes
Os pesquisadores primeiro compararam o desempenho no mundo real do paclitaxel e do nab‑paclitaxel em milhares de mulheres com câncer de mama. Ao reunir resultados de 17 estudos clínicos envolvendo 6.486 pacientes, constataram que o nab‑paclitaxel produzia taxas maiores de redução tumoral e mais frequente desaparecimento completo do câncer na mama e nos linfonodos próximos antes da cirurgia. Essa vantagem foi especialmente forte em pacientes tratadas após falhas de terapias anteriores. Ainda assim, ambos os medicamentos foram administrados em doses semelhantes e projetados para atacar células tumorais em divisão de forma muito parecida, sugerindo que algo além do efeito citotóxico direto difere entre eles.
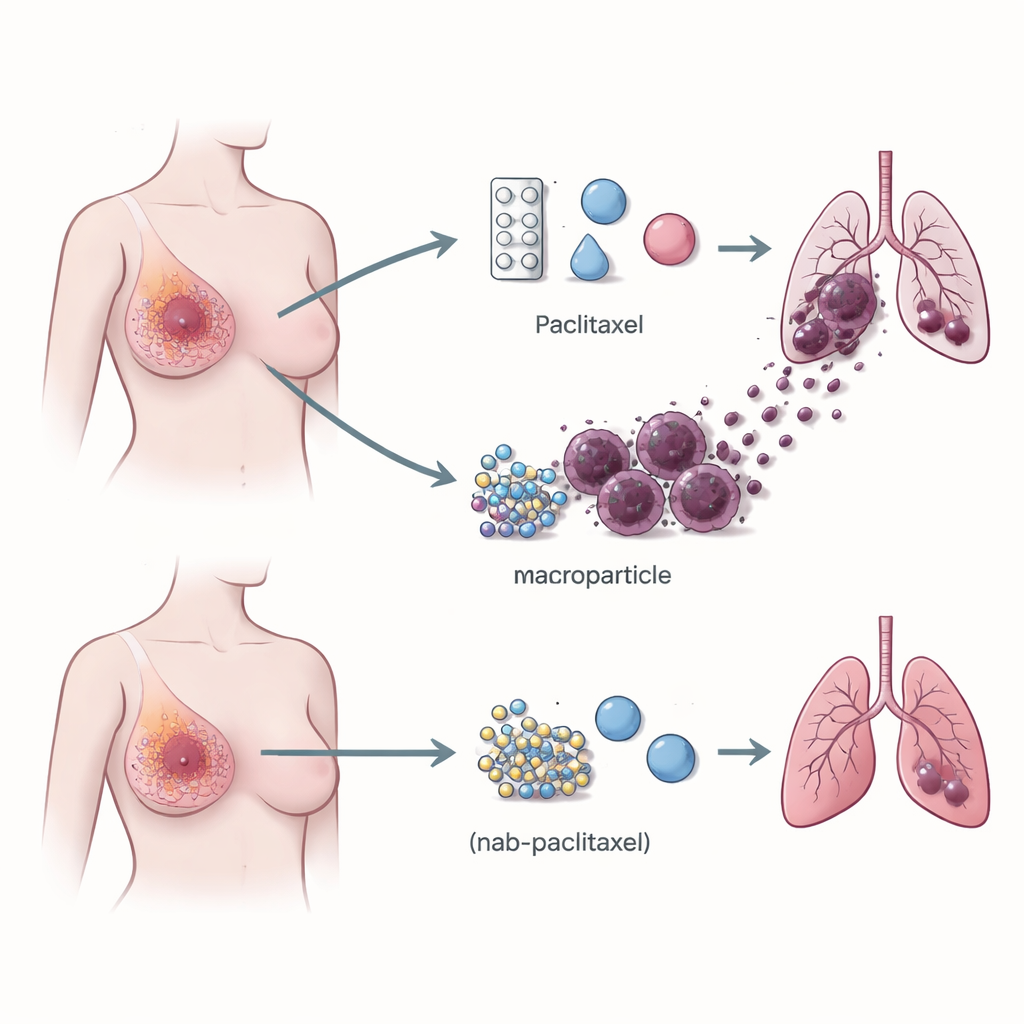
Células imunes que ajudam o câncer a viajar
A atenção voltou‑se para o ambiente imune do tumor — a mistura de leucócitos que pode tanto combater o câncer quanto, frequentemente de forma surpreendente, ajudá‑lo a crescer. Utilizando sequenciamento de RNA de célula única, que lê a atividade gênica em milhares de células individuais, a equipe comparou tumores de pacientes tratados com paclitaxel versus nab‑paclitaxel. Eles descobriram que tumores tratados com paclitaxel continham muitos mais macrófagos que exibem um receptor chamado TREM2 na superfície. Esses macrófagos TREM2‑positivos concentravam‑se nas bordas do tumor e eram muito mais abundantes em pacientes que mais tarde desenvolveram metástases pulmonares do que naquelas cujo câncer permaneceu localizado. O padrão se manteve em grupos maiores de pacientes e em modelos murinos, estabelecendo uma forte ligação entre esse tipo de macrófago e o risco de disseminação do câncer.
Quando o tratamento reduz tumores, mas alimenta a disseminação
Em camundongos com tumores mamários, o paclitaxel fez o que se espera: retardou ou encolheu os tumores primários. Mas, ao mesmo tempo, aumentou o número de focos tumorais nos pulmões e ampliou a população de macrófagos TREM2‑positivos nos tumores e na corrente sanguínea. O nab‑paclitaxel, em contraste, reduziu o tamanho do tumor sem estimular metástase pulmonar ou expandir esses macrófagos, embora fosse igualmente eficaz em encolher o tumor primário. Quando o gene TREM2 foi deletado em camundongos, ou quando o TREM2 foi reduzido com oligonucleotídeos antisenso (curtos trechos de DNA que silenciam genes específicos), o paclitaxel ainda encolheu tumores primários, mas perdeu em grande parte sua capacidade de promover a disseminação para os pulmões. Isso mostra que os macrófagos que exibem TREM2 não são apenas espectadores; são parceiros necessários na metástase induzida por paclitaxel.
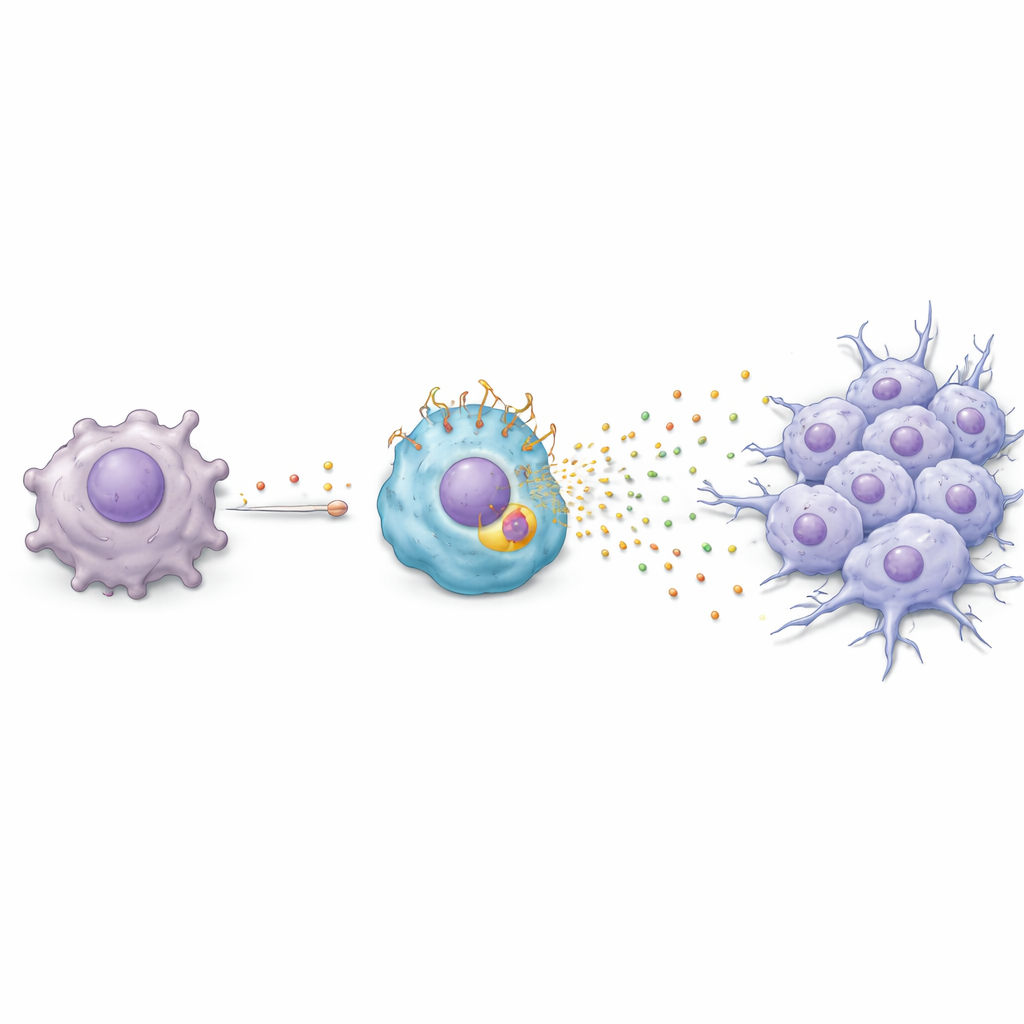
Uma reação em cadeia química do tumor até a célula imune
A equipe então investigou como o paclitaxel faz com que macrófagos assumam esse estado nocivo rico em TREM2. Descobriram uma reação em cadeia: o paclitaxel leva as células tumorais a ativarem um gene de resposta ao estresse chamado ATF3, que por sua vez aumenta a produção de um fator de crescimento chamado FGF2. As células cancerosas liberam então FGF2 no ambiente, onde ele atua sobre macrófagos próximos. Nesses macrófagos, o FGF2 ativa outro regulador, EGR1, que eleva os níveis de TREM2. Uma vez alto, o TREM2 faz com que os macrófagos passem a secretar um coquetel de proteínas — incluindo Serpin E1, HGF, CCL3 e CXCL2 — que empurram as células tumorais para uma forma mais móvel e invasiva conhecida como transição epitélio‑mesênquima. Em placas de cultura e em camundongos, essa comunicação química tornou as células tumorais mais propensas a migrar e invadir, passos-chave no caminho para a metástase.
Transformando uma espada de dois gumes em uma ferramenta mais segura
De forma geral, a mensagem principal é que o paclitaxel pode agir como uma espada de dois gumes: enquanto ataca os tumores, também instrui certas células imunes a ajudar o câncer a escapar para órgãos distantes. O nab‑paclitaxel parece evitar desencadear esse erro imune específico. A notícia encorajadora é que bloquear o TREM2 — ou partes da cadeia de sinalização FGF2–EGR1–TREM2 — pode separar os benefícios de encolhimento tumoral do paclitaxel dos riscos de promoção de metástase em modelos animais. Se estratégias semelhantes se mostrarem seguras e eficazes em pessoas, os médicos poderão continuar usando um quimioterápico familiar e amplamente disponível enquanto reduzem sua tendência a favorecer a disseminação do câncer, levando a melhores desfechos de longo prazo para as pacientes.
Citação: Xing, Y., Zhong, R., Li, Q. et al. Paclitaxel drives TREM2+ macrophage expansion underlying its inferior therapeutic efficacy compared to Nab-paclitaxel. Nat Commun 17, 2272 (2026). https://doi.org/10.1038/s41467-026-69060-5
Palavras-chave: câncer de mama, paclitaxel, microambiente tumoral, macrófagos, metástase