Clear Sky Science · pt
Reposicionamento confiável do interatoma de anticorpos dentro da célula
Transformando anticorpos em pequenas ferramentas dentro das nossas células
Anticorpos são famosos como armas de precisão na corrente sanguínea, direcionando‑se a vírus e outras ameaças. Mas a maior parte da ação em muitas doenças, incluindo Alzheimer, Parkinson e alguns tipos de câncer, ocorre dentro das células, onde anticorpos convencionais raramente alcançam ou funcionam bem. Este estudo mostra como reconstruir sistematicamente anticorpos existentes em "intrabodies" menores que funcionam de forma confiável dentro de células humanas vivas, abrindo caminho para novos diagnósticos, ferramentas de pesquisa e, potencialmente, futuras terapias que atuam diretamente no cerne dos processos patológicos.
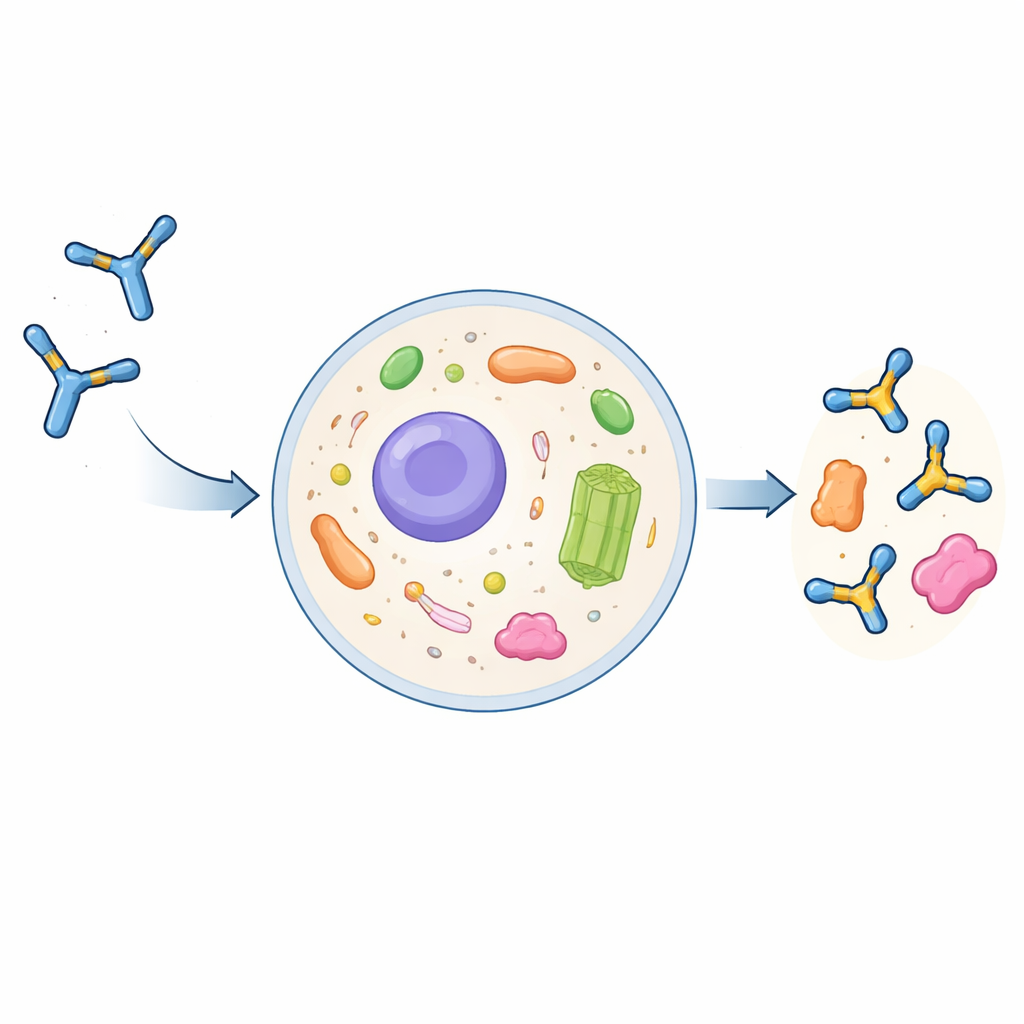
Por que anticorpos convencionais têm dificuldade dentro das células
Anticorpos em tamanho integral são proteínas grandes em forma de Y, evoluídas para atuar fora das células. Eles são montados e quimicamente modificados na via secretora da célula e então liberados na corrente sanguínea. Se forem recapturados pelas células, normalmente acabam em compartimentos de degradação em vez do fluido interior da célula, o citoplasma. Cientistas podem reduzir anticorpos às suas partes essenciais de reconhecimento, chamadas fragmentos variáveis de cadeia única (scFvs), e expressá‑los como intrabodies dentro das células. No entanto, esses intrabodies frequentemente se agregam, tornam‑se insolúveis e perdem a capacidade de se ligar aos alvos. Até agora, não existia uma receita geral e confiável para converter um anticorpo convencional em um intrabody com bom comportamento.
Encontrando as regras de projeto para intrabodies solúveis
Os pesquisadores começaram medindo o quanto 45 intrabodies diferentes permaneciam dissolvidos quando produzidos em células humanas. Compararam sistematicamente muitas características das proteínas — como hidrofobicidade global, qualidade estrutural prevista e propriedades das alças de ligação — para ver quais explicavam melhor se um intrabody permanecia solúvel. Um fator simples sobressaía: a carga elétrica global em pH próximo ao fisiológico. Intrabodies com carga líquida fortemente negativa tinham muito mais probabilidade de permanecer solúveis, enquanto aqueles com carga neutra ou positiva tendiam a se agregar. Outros preditores sofisticados, incluindo pontuações de confiança estrutural do sistema AlphaFold, não se correlacionaram com solubilidade. Isso permitiu à equipe construir um modelo prático baseado em carga que pode estimar quanto de um intrabody será detectado na fração solúvel de um extrato celular.
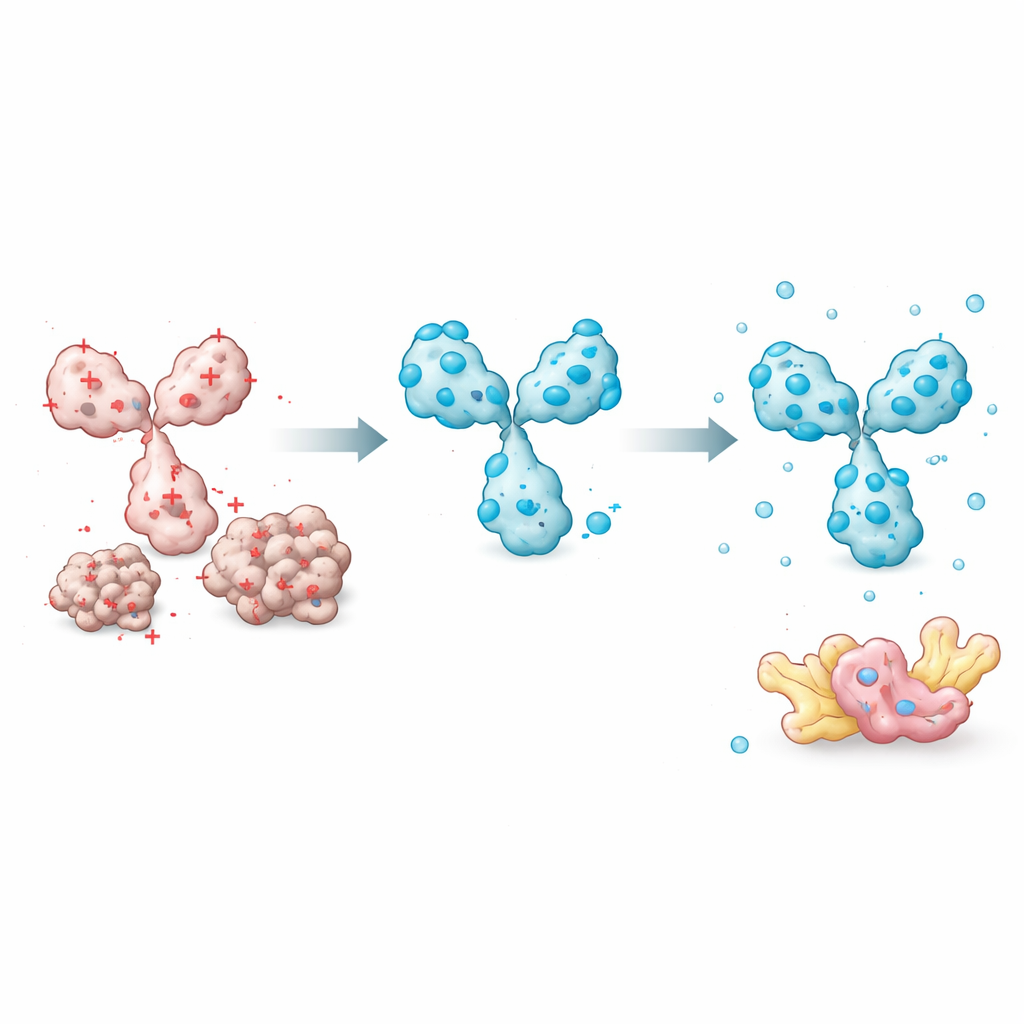
Reengenheirando conectores e domínios para melhor desempenho
Munidos dessa visão, o grupo concentrou‑se em características que podiam facilmente ajustar sem perturbar o reconhecimento do alvo pelo intrabody. Um elemento chave é o pequeno peptídeo "linker" que conecta os dois domínios variáveis. A maioria dos projetos existentes usa linkers neutros que não alteram a carga. Ao inserir aminoácidos carregados negativamente nessas posições, os pesquisadores puderam reduzir a carga global do intrabody, melhorando dramaticamente a solubilidade enquanto preservavam a ligação ao alvo. Eles também descobriram que a ordem dos domínios variáveis (se a parte pesada ou a leve vem primeiro) e posições específicas do arcabouço fora das alças de ligação influenciam quão facilmente a proteína se dobra e se mantém dissolvida. Escolher uma ordem de domínios que protege regiões mais frágeis e introduzir mutações de troca de carga cuidadosamente posicionadas aumentou ainda mais o desempenho.
Usando inteligência artificial para construir intrabodies em escala
Para ir além do método de tentativa e erro individual, os autores combinaram suas regras simples de carga com software avançado de design de proteínas baseado em aprendizado profundo. Partindo de espinhas dorsais (backbones) de anticorpos conhecidos, usaram uma abordagem de "dobramento inverso" para sugerir novas sequências que ainda adotassem a forma desejada, mas exibissem características de superfície — especialmente padrões de carga — que favorecessem estabilidade e solubilidade. Restringiram mudanças nas alças de ligação críticas para preservar o reconhecimento, enquanto permitiam que o algoritmo redesenhasse as superfícies circundantes. Testes mostraram que muitos desses intrabodies guiados por IA não apenas eram altamente solúveis, como também mais estáveis termicamente que variantes projetadas por humanos, mantendo a capacidade de se ligar a alvos relevantes para doenças, como SOD1 mal dobrada, p53, α‑sinucleína e outras proteínas associadas à neurodegeneração.
Construindo uma biblioteca de capturadores de proteínas dentro da célula
Aplicando essas regras e ferramentas em larga escala, a equipe reformulou computacionalmente 672 anticorpos em intrabodies previstos para funcionar bem dentro de células. Essas moléculas projetadas cobrem mais de 60 alvos intracelulares diferentes, incluindo proteínas envolvidas nas doenças de Alzheimer, Parkinson e Huntington, bem como fatores relacionados ao câncer e modificações pós‑tradução como fosforilação e acetilação. Em experimentos, intrabodies selecionados pescavam com sucesso formas específicas de proteínas ligadas à doença, como SOD1 mutante ou conformações particulares de α‑sinucleína, enquanto ignoravam as versões normais. Todas as sequências foram liberadas abertamente, e os autores disponibilizam uma ferramenta web que permite a outros estimar a solubilidade de intrabodies a partir da sequência usando o mesmo modelo baseado em carga.
O que isso significa para futuras medicinas e pesquisas
Em termos práticos, este trabalho transforma a vasta coleção existente de anticorpos — muitos já estudados na clínica — em um conjunto de ferramentas que pode ser adaptado de forma confiável para uso dentro das células. Seguindo um conjunto direto de regras de projeto, os pesquisadores agora podem criar intrabodies que têm grande probabilidade de funcionar na primeira tentativa, economizando tempo e custos. Para um leitor leigo, a mensagem principal é que os cientistas encontraram um modo simples de "reconfigurar" nossos melhores detectores proteicos para que funcionem no interior denso de células vivas, onde muitas doenças têm início. Isso pode acelerar o desenvolvimento de novas maneiras de rastrear, estudar e, eventualmente, tratar condições impulsionadas por proteínas mal dobradas ou com funcionamento defeituoso.
Citação: O’Shea, C.M., Shahzad, R., Aghasoleimani, K. et al. Reliable repurposing of the antibody interactome inside the cell. Nat Commun 17, 2222 (2026). https://doi.org/10.1038/s41467-026-69057-0
Palavras-chave: intrabodies, engenharia de anticorpos, solubilidade de proteínas, doença neurodegenerativa, inteligência artificial na biologia