Clear Sky Science · pt
Regulando a água interfacial para transferência de oxigênio a ligações benzílicas C(sp3)–H via covalência tungstênio-oxigênio ativada por níquel
Transformando água e óleo em produtos químicos úteis
Químicos há muito buscam uma forma mais limpa de converter moléculas simples à base de óleo em ingredientes de maior valor para plásticos, medicamentos e produtos do dia a dia. Este estudo mostra como “ajustar” cuidadosamente a camada fina de água que toca um eletrodo pode permitir que a água comum forneça oxigênio a hidrocarbonetos resistentes, reduzindo desperdício e consumo de energia no processo.
Por que o oxigênio da água importa
Muitos produtos químicos industriais são obtidos ao incorporar oxigênio a hidrocarbonetos — moléculas compostas principalmente por carbono e hidrogênio. Hoje em dia isso frequentemente envolve agentes oxidantes fortes e altas temperaturas, que consomem muita energia e geram emissões que aquecem o clima. A água é uma fonte de oxigênio barata, segura e abundante, mas convencê-la a ceder esse oxigênio diretamente a ligações carbono–hidrogênio robustas normalmente exige tensões muito altas. Nestas condições severas, a maior parte da eletricidade é desperdiçada na formação de oxigênio gasoso em vez de produzir compostos úteis.
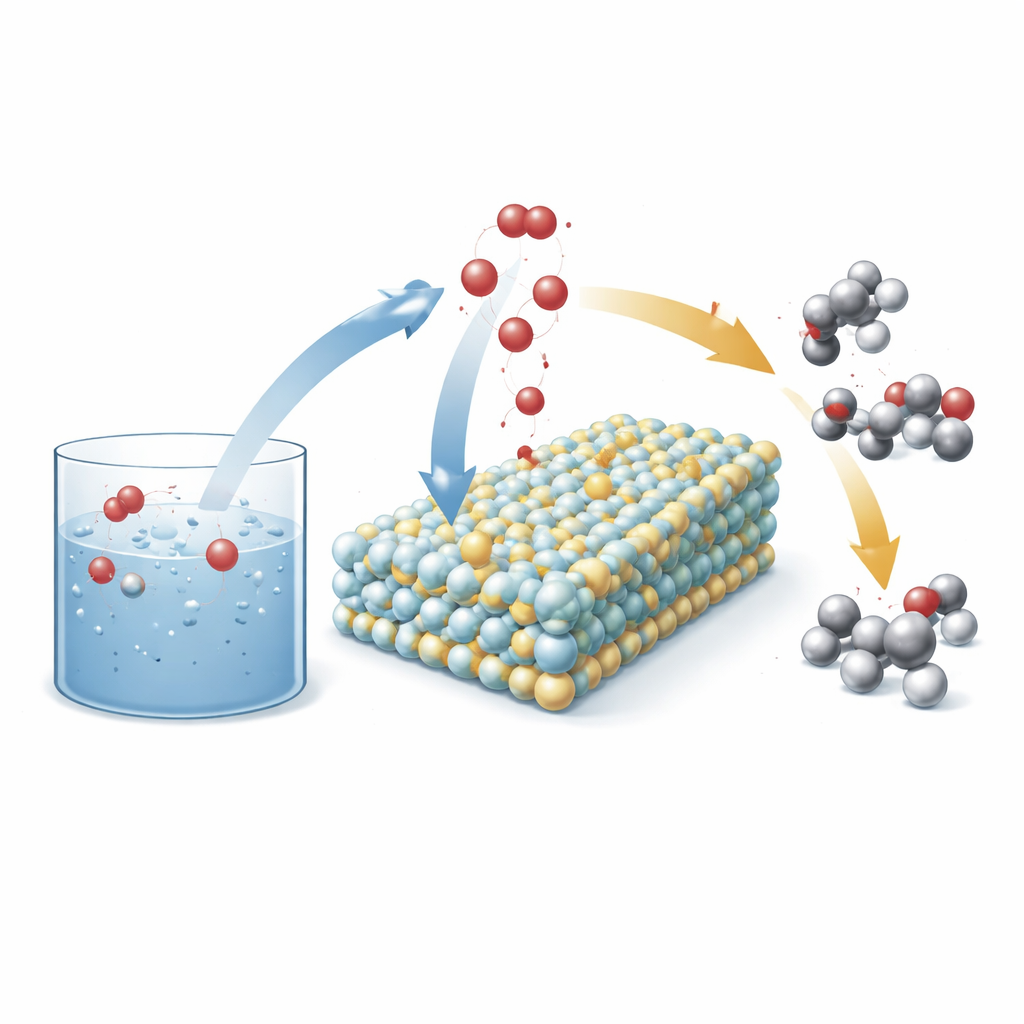
Um eletrodo inteligente que reorganiza a água
Os pesquisadores projetaram um novo tipo de ânodo (o eletrodo positivo em uma célula eletroquímica) construído a partir de partículas minúsculas de carboneto de tungstênio que se transformam durante a operação em um material amorfo de tungstênio–oxigênio. Nesse arcabouço, eles dispersam átomos isolados de níquel. Em condições de reação, oxigênio da água migra para o sólido, convertendo-o em uma superfície de óxido de tungstênio ativada por níquel com muitos sítios reativos expostos. Essa superfície reconstruída então serve como plataforma onde água e moléculas de hidrocarboneto se encontram e trocam oxigênio de maneira controlada, favorecendo produtos valiosos como álcoois e cetonas em vez de ácidos superoxidados e outros subprodutos.
Afrouxando a “gaiola” de água na superfície
Uma descoberta chave é que átomos de níquel alteram sutilmente a forma como as moléculas de água se organizam junto ao eletrodo. Normalmente, a água em uma superfície carregada forma uma densa rede de ligações de hidrogênio, como uma malha apertada que retarda o movimento. Simulações computacionais e medições infravermelhas sensíveis mostram que, nas regiões dopadas com níquel, essa rede se torna mais frouxa, com menos ligações de hidrogênio e mais moléculas de água “livres”. Isso abre canais pelos quais a água pode difundir mais facilmente até os sítios reativos de tungstênio–oxigênio. Como resultado, fragmentos portadores de oxigênio da água alcançam a superfície mais rapidamente e com maior frequência, alimentando a reação em vez de escapar como oxigênio gasoso.
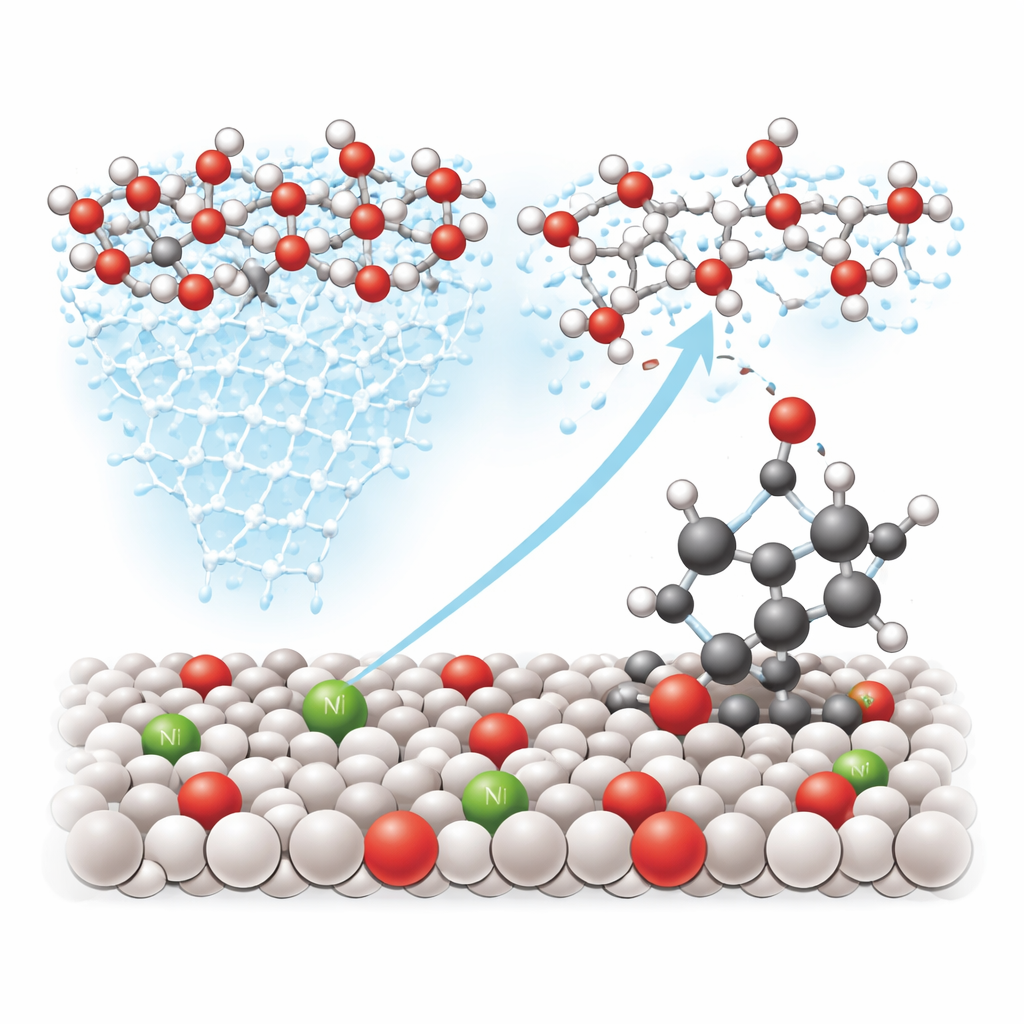
Guiando o oxigênio para as ligações certas
Além de melhorar o tráfego na superfície, o níquel também ajusta a estrutura eletrônica dos átomos de tungstênio vizinhos, tornando certos pontos particularmente aptos a capturar e ativar a água. Experimentos com isótopos — versões especiais de oxigênio e hidrogênio que podem ser rastreadas — mostram que o oxigênio ativo vem de água recentemente rompida, e não do corpo do óxido em si. “Instantâneos” espectroscópicos capturam uma ponte de curta duração entre tungstênio, oxigênio e o carbono benzílico em moléculas como o etilbenceno. Cálculos teóricos confirmam que, na superfície modificada com níquel, é mais fácil para um átomo de oxigênio atacar esse sítio carbono–hidrogênio do que seguir a rota habitual de divisão da água que produz oxigênio gasoso, direcionando efetivamente a reação para produtos oxigenados úteis.
Eficiência, seletividade e durabilidade
Nos testes, o eletrodo ativado com níquel converte uma variedade de ligações carbono–hidrogênio benzílicas em álcoois e cetonas com eficiências farádicas — a fração da carga elétrica que vai para a química desejada — tipicamente acima de 50%, alcançando mais de 56% em casos otimizados. O sistema opera por muitos ciclos sem perda de atividade, mantendo sua estrutura níquel–tungstênio. Por usar água como única fonte de oxigênio e evitar oxidantes químicos adicionados, oferece eficiência energética competitiva e custos de material mais baixos em comparação com outros métodos avançados. Embora o escopo atual esteja focado em sítios benzílicos, o princípio subjacente — usar aditivos atômicos para remodelar a água interfacial e redirecionar caminhos de reação — aponta para um conjunto mais amplo de ferramentas para oxidações dirigidas por eletricidade, mais verdes, de ligações carbono–hidrogênio de outra forma inertes.
O que isso significa para uma química mais limpa
Este trabalho demonstra que pequenas mudanças em escala atômica podem ter efeitos desproporcionais sobre o comportamento da água em um eletrodo e sobre onde seu oxigênio vai parar. Ao usar átomos de níquel tanto para afrouxar a estrutura da água interfacial quanto para ajustar finamente os sítios reativos, os autores transformam a água em um doador de oxigênio eficiente para ligações de hidrocarbonetos difíceis de ativar, ao mesmo tempo em que suprimem a formação indesejada de oxigênio gasoso. A longo prazo, estratégias como essa podem ajudar a redesenhar a química de oxidação na indústria química, tornando-a mais eficiente em termos energéticos e mais favorável ao clima ao usar eletricidade e água em vez de oxidantes agressivos e reagentes de origem fóssil.
Citação: Leng, BL., Lin, X., Dong, HY. et al. Regulating interfacial water for oxygen transfer to benzylic C(sp3)–H bonds via Ni-activated tungsten-oxygen covalency. Nat Commun 17, 2355 (2026). https://doi.org/10.1038/s41467-026-69054-3
Palavras-chave: eletrocatalise, oxidação da água, ativação de C–H benzílico, óxido de tungstênio dopado com níquel, química verde