Clear Sky Science · pt
RNA-Seq dupla in vivo descobre efetores-chave da ruptura da barreira epitelial por um patógeno extracelular
Como alguns micróbios passam despercebidos pelas nossas cercas celulares
Nossos órgãos são revestidos por células compactas que funcionam como muros, mantendo sangue, micróbios e toxinas onde devem ficar. Ainda assim, certos germes escapam entre essas células e se espalham pelo corpo. Este estudo revela em detalhes vívidos como a bactéria que causa a leptospirose, uma doença grave e de alcance mundial, alcança silenciosamente órgãos como fígado e rins e usa um truque engenhoso envolvendo o cálcio dentro de nossas células para abrir essas barreiras protetoras.
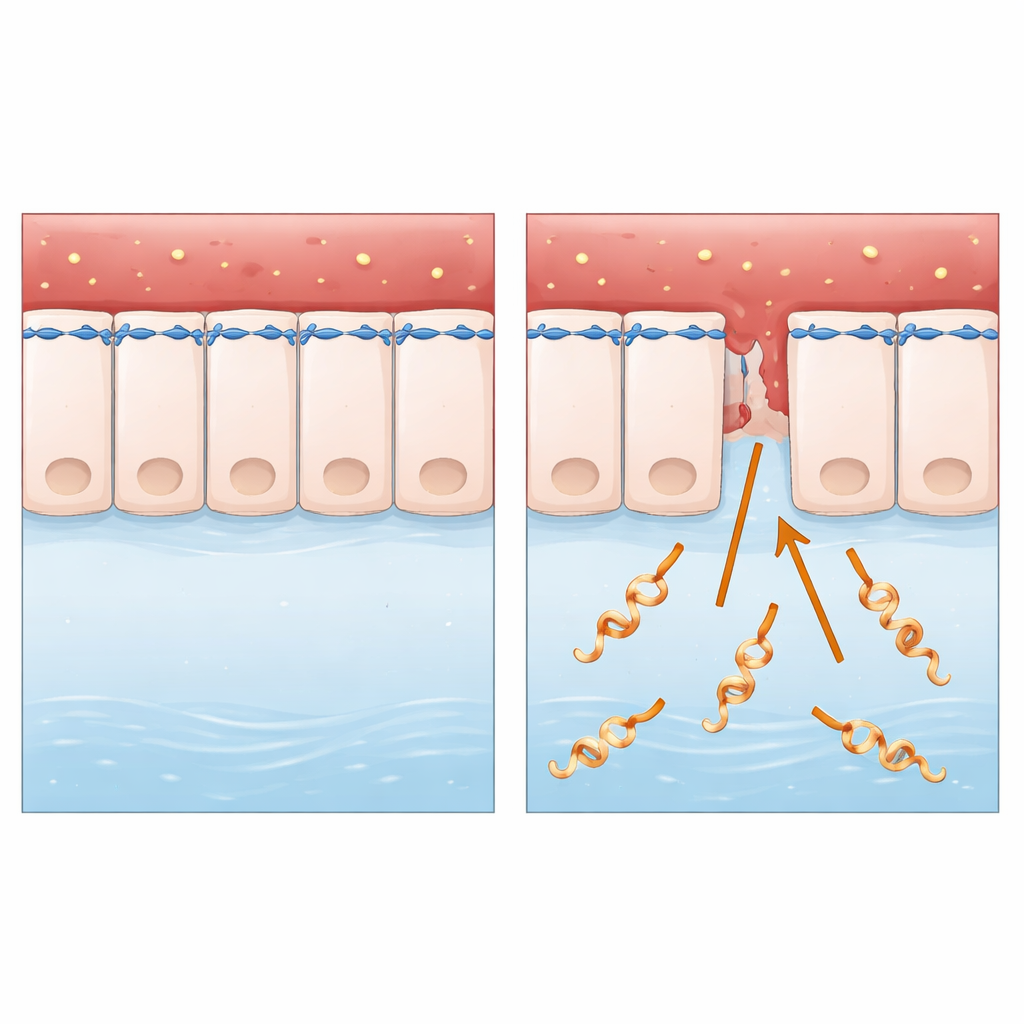
Um invasor sorrateiro de tecidos animais e humanos
A pesquisa foca em Leptospira interrogans, uma bactéria em forma de espiral transmitida principalmente de animais para humanos por água ou solo contaminados. Após entrar por pequenas lesões na pele ou mucosas, ela viaja pela corrente sanguínea e pode desencadear doença grave, incluindo falência hepática e renal e hemorragias internas. Ao contrário de muitos micróbios bem estudados, Leptospira vive fora das células e não possui algumas das “armas moleculares” clássicas que os cientistas costumam procurar. Isso a tornou um caso‑teste ideal para uma pergunta básica: como uma bactéria aparentemente simples e de vida livre consegue atravessar camadas celulares intactas com tanta eficiência?
Observando genes do hospedeiro e do micróbio em diálogo ao mesmo tempo
Para capturar o processo de infecção dentro de um animal vivo, a equipe usou RNA‑Seq dupla em hamsters, um modelo para leptospirose aguda. Esse método revela quais genes estão ligados ou desligados tanto no hospedeiro quanto no patógeno simultaneamente. Os cientistas infectaram hamsters e coletaram tecido de fígado e rim um e três dias depois. No início, apesar do alto número de bactérias, as células dos animais mal alteraram sua atividade gênica, sugerindo que Leptospira inicialmente passa despercebida pelo sistema imune. No terceiro dia, porém, ambos os órgãos mostraram forte reação, especialmente o fígado: genes envolvidos em inflamação, junções célula‑a‑célula e o arcabouço interno das células foram fortemente alterados, apontando para uma remodelação ativa das barreiras teciduais.
Desfazendo o zíper celular de fora para dentro
As camadas celulares são vedadas por junções apertadas e aderentes, que ligam células vizinhas e as ancoram a um anel de actina e miosina, o mesmo par proteico que ajuda a contrair músculos. Microscopia de células epiteliais humanas infectadas com Leptospira mostrou mudança de forma, abertura de lacunas entre células e enfraquecimento ou deslocamento de proteínas-chave das junções. Importante: as células não morriam, o que significa que a barreira estava sendo desmontada, não destruída. Os pesquisadores também observaram sinais de estresse nas fábricas de dobramento de proteínas das células, mas bloquear esse estresse não restaurou as junções, indicando outro culpado.
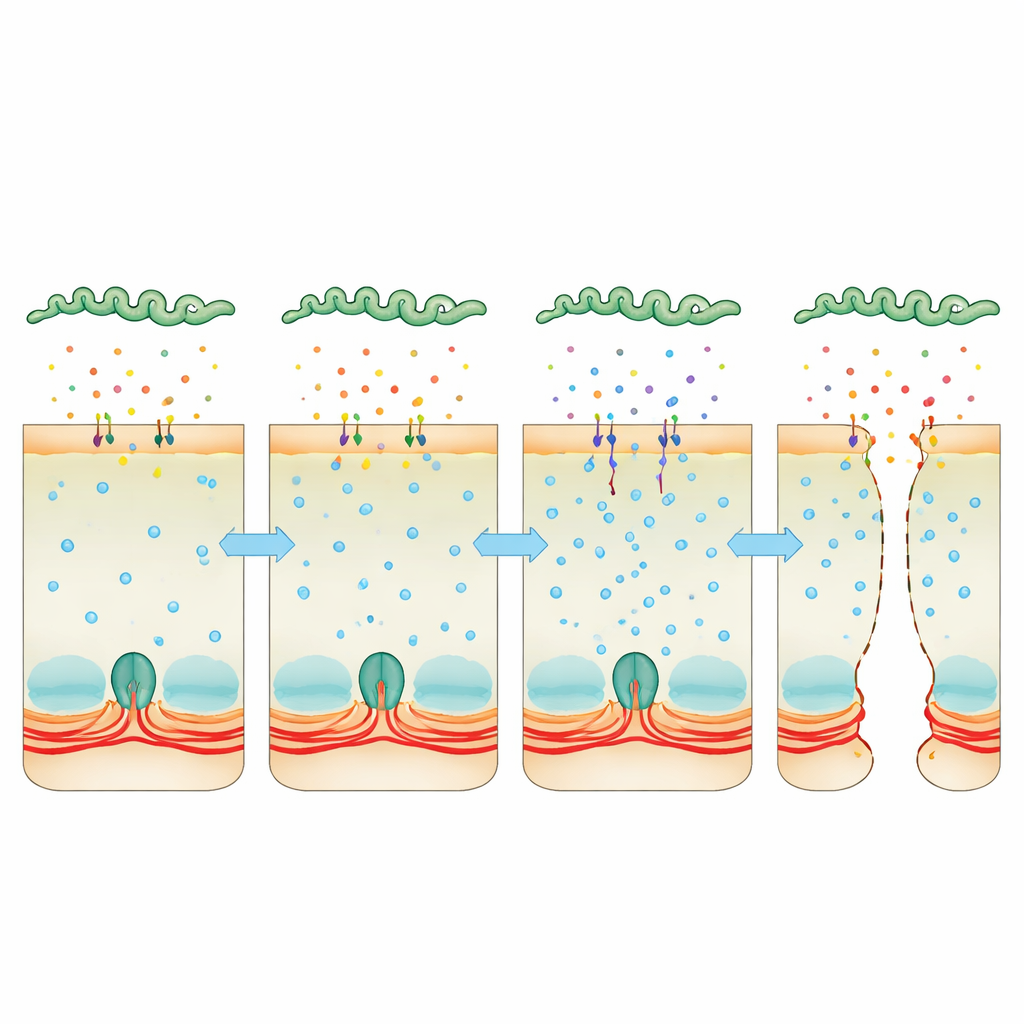
Sequestrando o cálcio como uma alavanca escondida
A atenção voltou‑se para o cálcio, um sinal universal dentro das células que pode apertar ou relaxar o anel de actina‑miosina. As células infectadas acumularam mais cálcio, e isso esteve ligado a maior atividade da quinase da cadeia leve da miosina, uma enzima que faz o anel contrátil puxar as junções. Quando a equipe usou um composto que sequestra cálcio, ou fármacos que inibem a calmodulina ou essa quinase, as camadas celulares permaneceram mais intactas e as bactérias tiveram mais dificuldade em passar. Ao mesmo tempo, o sequenciamento profundo do RNA bacteriano revelou que, dentro do hospedeiro, Leptospira aumenta fortemente a produção de duas proteínas “Modificadoras de Virulência” que se assemelham a toxinas. Essas proteínas são secretadas para o ambiente, ligam‑se às células do hospedeiro e são encontradas dentro delas. Quando as bactérias careciam de uma ou ambas essas proteínas, tinham muito menos capacidade de atravessar camadas celulares ou causar doença letal, e seu caldo secretado não elevava mais os níveis de cálcio nem desmontava as junções com a mesma eficiência.
O que isso significa para a doença e defesas futuras
No conjunto, os resultados delineiam uma história clara. Após entrar no corpo quase sem ser detectada, Leptospira começa a secretar proteínas Modificadoras de Virulência semelhantes a toxinas. Essas proteínas ligam‑se às células epiteliais e perturbam o equilíbrio de cálcio no interior, o que por sua vez ativa uma via contrátil que separa o “zíper” celular que mantém as células vizinhas unidas. À medida que as junções apertadas e aderentes se afrouxam, aparecem lacunas microscópicas que permitem às bactérias passar entre as células, colonizar órgãos e desencadear doença severa. Ao identificar esse mecanismo dirigido pelo cálcio e as proteínas bacterianas por trás dele, o estudo abre caminho para novas estratégias — como bloquear essas proteínas ou sua via de sinalização — para reforçar nossas cercas celulares e limitar a disseminação da leptospirose e possivelmente de outras infecções que exploram táticas semelhantes.
Citação: Giraud-Gatineau, A., Haustant, G., Monot, M. et al. In vivo dual RNA-Seq uncovers key effectors of epithelial barrier disruption by an extracellular pathogen. Nat Commun 17, 2274 (2026). https://doi.org/10.1038/s41467-026-69033-8
Palavras-chave: leptospirose, barreira epitelial, sinalização por cálcio, toxinas bacterianas, interações hospedeiro–patógeno