Clear Sky Science · pt
nDIA-MS aprimorado com supercharging permite perfilamento global de mudanças na solubilidade do proteoma induzidas por fármacos
Por que o comportamento das proteínas importa além de simples contagens
Medicamentos podem alterar não apenas quanto de uma proteína uma célula produz, mas também para onde essa proteína vai e se ela fica livre ou se agrega às estruturas celulares. Essas mudanças no “onde” e no “como” as proteínas existem dentro das células estão intimamente ligadas a doenças como câncer e neurodegeneração, mas são difíceis de medir em larga escala. Este estudo apresenta uma maneira rápida e poderosa de escanear milhares de proteínas humanas ao mesmo tempo para ver como sua solubilidade — se estão em um estado mais livre ou mais preso — muda quando as células são expostas a dois fármacos experimentais amplamente usados.
Uma forma mais rápida e precisa de observar proteínas
Os autores partem de uma tecnologia central da biologia moderna: espectrometria de massas, uma técnica que pesa e conta fragmentos proteicos. Métodos padrão já são excelentes em informar quanto de cada proteína está presente, mas têm dificuldade em revelar mudanças no estado proteico, como associação ao DNA ou formação de agregados densos. Aqui, os pesquisadores refinam uma versão da espectrometria de massas chamada aquisição de dados independente com janela estreita (nDIA-MS). Ao adicionar pequenos auxiliares químicos, chamados reagentes de supercharging, ao líquido que transporta os peptídeos pelo instrumento, eles aumentam as cargas elétricas desses fragmentos e reforçam muito o sinal.
Após testar dois aditivos de supercharging comuns, dimetilsulfóxido (DMSO) e m-nitrobenzil álcool (mNBA), eles descobriram que 3% de DMSO proporciona o maior aumento global de sinal e o maior número de proteínas detectadas, enquanto o mNBA é melhor em aumentar o número e a carga de fragmentos peptídicos individuais. Com a configuração otimizada, a equipe consegue identificar cerca de 9.600 proteínas humanas a partir de apenas um micrograma de um digest padrão de células em uma corrida de 15 minutos — uma combinação notável de velocidade e profundidade para experimentos rotineiros. Esse desempenho prepara o terreno para usar nDIA-MS não apenas para quantificar proteínas, mas para sondar como seu estado físico responde ao estresse.
Transformando solubilidade em um indicador de mudança celular
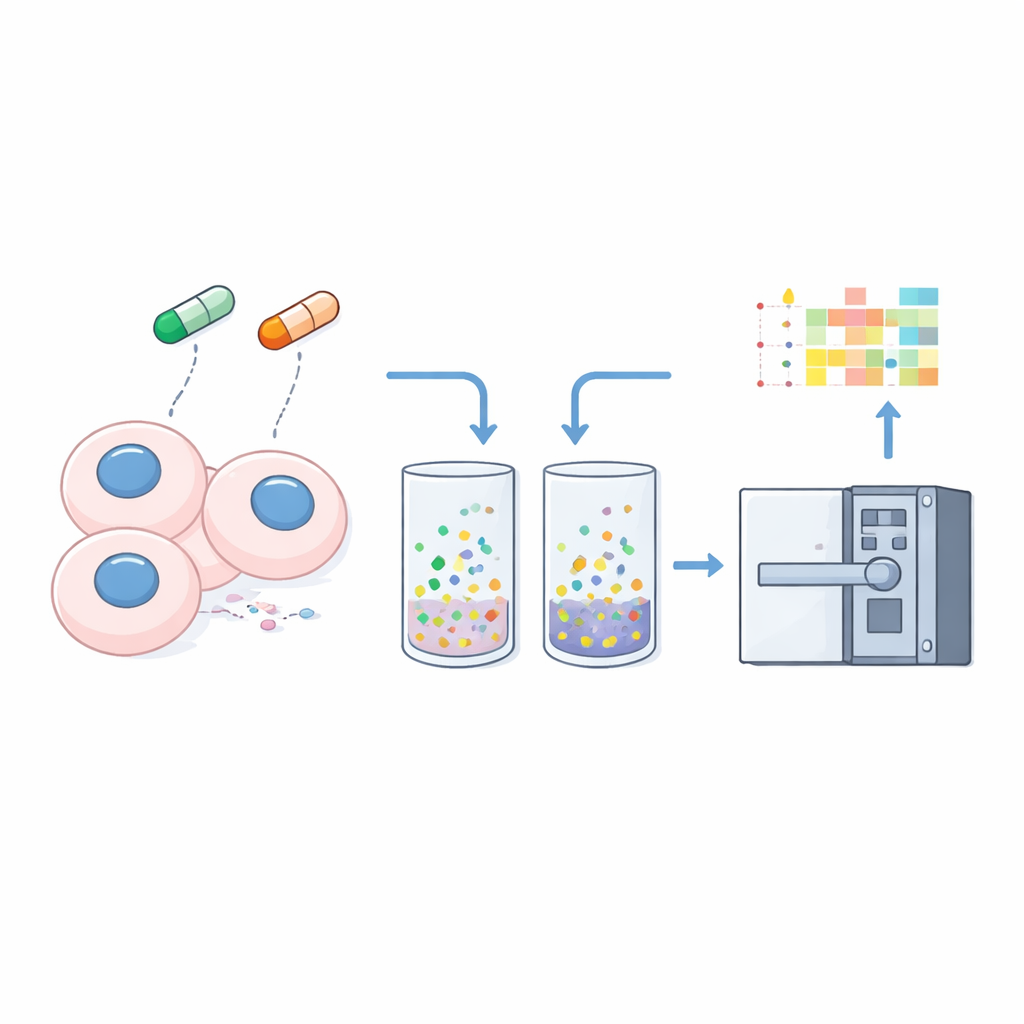
Para transformar a solubilidade em um sinal mensurável, os pesquisadores pré-tratam suavemente as células com um detergente leve que extrai proteínas livremente solúveis, deixando para trás material fortemente ligado ao DNA, membranas ou outras estruturas. Eles analisam tanto o lisado total quanto esse pellet “insolúvel” de três linhagens de células cancerígenas usando o método nDIA-MS otimizado. Comparando a abundância de cada proteína no pellet em relação à amostra de célula inteira, calculam uma simples “razão de insolubilidade” — valores mais altos sugerem associação mais forte a estruturas celulares, valores mais baixos sugerem um estado mais solúvel e livre.
A equipe então expõe as células por apenas uma hora a dois fármacos: MG132, um bloqueador do proteassoma que impede as células de degradarem proteínas indesejadas, e ML-792, um inibidor da ativação da SUMO que interfere em um sistema chave de marcação proteica. Essa exposição curta é deliberada; visa capturar mudanças rápidas e iniciais no comportamento proteico antes que alterações na expressão gênica se manifestem plenamente. Mesmo nessa janela breve, eles conseguem quantificar mudanças de solubilidade e abundância para 8.694 proteínas e confirmar que sua fracionamento separa claramente proteínas tradicionalmente solúveis, como tubulina, de proteínas ligadas à cromatina, como histonas.
Fármacos que remodelam o panorama proteico da célula
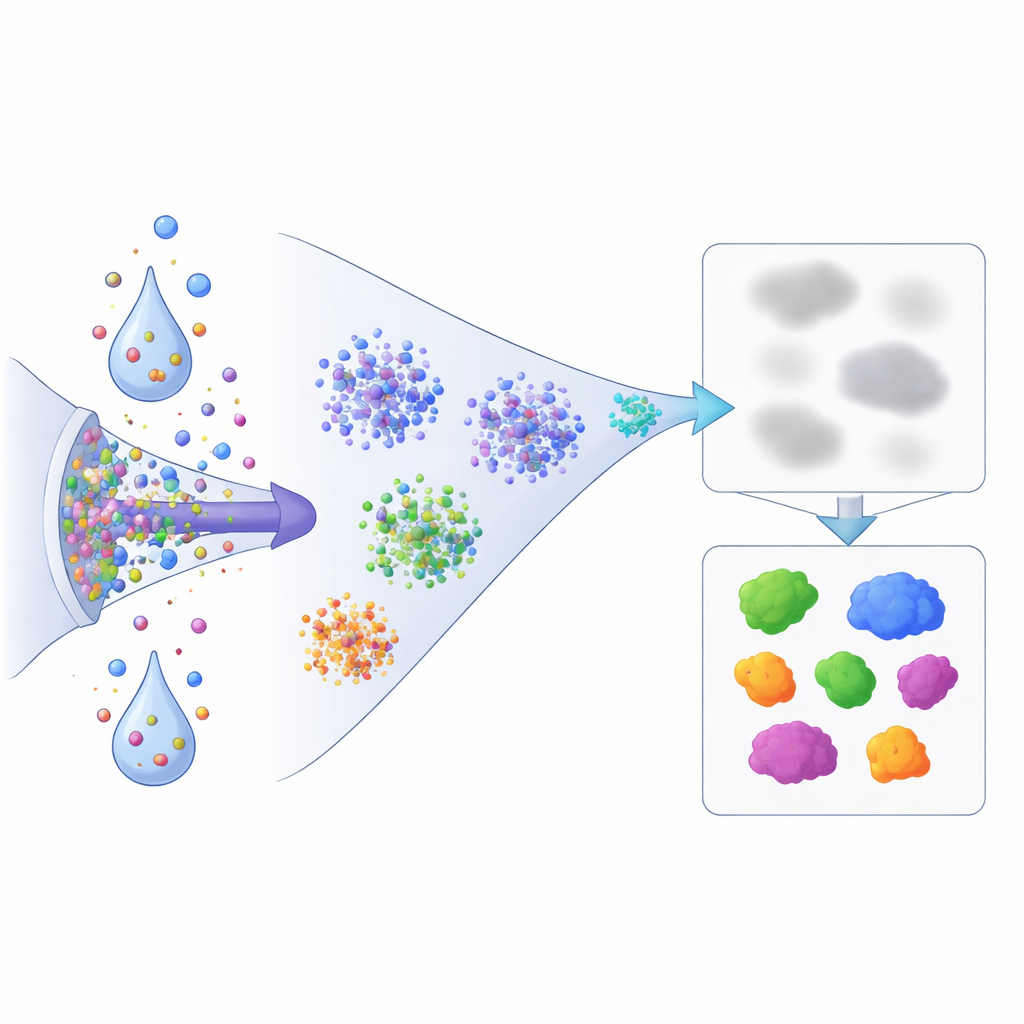
MG132 e ML-792 produzem remodelagens amplas, porém distintas, da solubilidade proteica. O MG132 torna mais de mil proteínas mais insolúveis e mais de seiscentas mais solúveis nas três linhagens celulares. Muitas proteínas afetadas atuam na interseção do controle de qualidade proteica, resposta a danos no DNA, regulação gênica e autofagia — o sistema de autolimpeza da célula. Por exemplo, componentes do complexo ativador do proteassoma e adaptadores que ajudam a marcar proteínas defeituosas tornam-se menos solúveis, sugerindo que, quando a degradação é bloqueada, fatores-chave de controle de qualidade ficam presos em estruturas como cromatina ou membranas celulares. Proteínas de autofagia e jogadores da resposta a danos, incluindo o regulador de estresse HSF1, também se deslocam para estados mais insolúveis, semelhantes a condensados, consistente com a formação de corpos de estresse nucleares.
O ML-792, em contraste, atinge fortemente proteínas envolvidas na transcrição e no próprio sistema SUMO. Centenas de proteínas tornam-se ou mais insolúveis ou mais solúveis quando a ativação da SUMO é bloqueada, e proteínas centrais da via SUMO migram para o pool solúvel, como esperado. O estudo destaca comportamentos notáveis: subunidades da RNA polimerase III tornam-se mais insolúveis, sugerindo alteração na importação nuclear ou na ligação à cromatina; represores-chave associados a corpos nucleares, como SP100 e DAXX, tornam-se mais solúveis, indicando que marcas de SUMO ajudam a mantê-los sequestrados nesses compartimentos. Quando ambos os fármacos são aplicados isoladamente ou em sequência, algumas proteínas, incluindo NAB2, SMAD2 e RB1, exibem mudanças de insolubilidade coordenadas ou até opostas, revelando uma interação sutil entre os sistemas de marcação por ubiquitina e SUMO no controle da localização proteica.
O que isso significa para a descoberta de medicamentos no futuro
Para não especialistas, a mensagem central é que proteínas não apenas aumentam ou diminuem em quantidade quando células são estressadas ou tratadas com fármacos; elas também se movem, se condensam e mudam o grau de associação com estruturas celulares. Este trabalho fornece uma forma em alta velocidade e em escala proteômica para observar essas mudanças acontecendo. Ao combinar um fluxo de trabalho de espectrometria de massas ajustado com uma comparação simples entre solúvel e insolúvel, os autores mostram que fármacos experimentais comuns reorganizam rapidamente o panorama interno de proteínas de maneiras que medições de abundância padrão deixariam passar. A abordagem abre a porta para mapear como candidatos a medicamentos remodelam estados proteicos por toda a célula, ajudando pesquisadores a descobrir alvos inesperados, vias de estresse e pontos de falha que podem ser cruciais para entender tanto a ação terapêutica quanto os efeitos colaterais.
Citação: Xiong, Y., Zhang, H., Tan, L. et al. Supercharging-enhanced nDIA-MS enables global profiling of drug-induced proteome solubility shifts. Nat Commun 17, 2350 (2026). https://doi.org/10.1038/s41467-026-69025-8
Palavras-chave: solubilidade do proteoma, espectrometria de massas, inibidor do proteassoma MG132, inibidor da SUMOilação ML-792, transições de estado proteico